Cho 20.4g nhôm oxoxit tác dụng với axit sunfuric
a) tính mH2SO4
b) tính klg muối
c)tính mH2O
Cho 2,7 g nhôm tác dụng hoàn toàn hết với 441 gam dung dịch axit sunfuric sau phản ứng thu được dung dịch muối nhôm sunfat a viết phương trình phản ứng b tính nồng độ phần trăm của dung dịch axit C tính thể tích của dung dịch muối
a) $2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
b)
n Al = 2,7/27 = 0,1(mol)
Theo PTHH :
n H2SO4 = 3/2 n Al = 0,15(mol)
=> C% H2SO4 = 0,15.98/441 .100% = 3,33%
c)
Theo PTHH :
n H2 = 3/2 n Al = 0,15(mol)
=> V H2 = 0,15.22,4 = 3,36(lít)
cho một lượng nhôm oxit tác dụng vừa đủ với 300 ml dd axit sunfuric 4,9 % (d = 1,08)
a tính khối lượng nhôm oxit cần dùng để tác dụng hết với lượng axit đã cho
b tính số g muối thu được sau phản ứng
Cho m gam nhôm tác dụng với lượng dư dung dịch axit sunfuric loãng (H2SO4) thu được muối nhôm sunfat và 3,36 lít khí hiđro (đktc).
a. Viết phương trình phản ứng?
b. Tính giá trị m =?
c. Tính khối lượng muối thu được sau phản ứng?
2Al+3H2SO4->Al2(SO4)3+3H2
0,1----------------------0,075----0,15
n H2=0,15 mol
=>mAl=0,1.27=2,7g
=>m Al2(SO4)3=0,075.342=25,65g
a) PTHH: \(2Al+3H_2SO_2\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_{Al}=\dfrac{2}{3}.0,15=0,1\left(mol\right)\)
\(m_{Al}=0,1.27=2,7\left(g\right)\)
c) \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
\(m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
2Al+3H2SO4->Al2(SO4)3+3H2
0,1----------------------0,075----0,15
n H2=0,15 mol
=>mAl=0,1.27=2,7g
=>m Al2(SO4)3=0,075.342=25,65g
Câu 7: Cho nhôm tác dụng với axit sunfuric sinh ra muối nhôm sunfat và 17,92 lít khí hidro đo ở đktc. Tính khối lượng axit phản ứng, muối sinh ra và kim loại phản ứng.
Câu 8: Cho nhôm oxit tác dụng với axit nitric sinh ra muối nhôm sunfat và 7,2g nước . Tính khối lượng axit phản ứng, muối sinh ra và kim loại phản ứng.
giúp mik với nha :)))
Câu 7 :
\(n_{H2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
\(\dfrac{8}{15}\) 0,8 \(\dfrac{4}{15}\) 0,8
\(n_{H2SO4}=\dfrac{0,8.3}{3}=0,8\left(mol\right)\)
⇒ \(m_{H2SO4}=0,8.98=78,4\left(g\right)\)
\(n_{Al2\left(SO4\right)3}=\dfrac{0,8.1}{3}=\dfrac{4}{15}\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=\dfrac{4}{15}.342=91,2\left(g\right)\)
\(n_{Al}=\dfrac{0,8.2}{3}=\dfrac{8}{15}\left(mol\right)\)
⇒ \(m_{Al}=\dfrac{8}{15}.27=14,4\left(g\right)\)
Chúc bạn học tốt
bài 8
Al2O3+6HNO3->2Al(NO3)3+3H2
\(\dfrac{2}{15}\)------------0,8-------\(\dfrac{4}{15}\)----------0,4 mol
n H2O=\(\dfrac{7,2}{18}\)=0,4 mol
=>m Al2O3=\(\dfrac{2}{15}\).102=13,6g
=>m HNO3=0,8.63=50,4g
=>m Al(NO3)3=\(\dfrac{4}{15}\).213=56,8g
Bài 7
2Al+3H2SO4->Al2(SO4)3+3H2
\(\dfrac{8}{15}\)------0,5-----------\(\dfrac{4}{15}\)--------0,8
n H2=\(\dfrac{17,92}{22,4}\)=0,8 mol
=>m Al= \(\dfrac{8}{15}\).27=14,4g
=>m HCl=0,5.36,5=18,25g
=>m Al2(SO4)3=\(\dfrac{4}{15}\).342=91,2g
Cho 27g Al tác dụng với dung dịch axit sunfuric (H2SO4) cho 171 g muối nhôm sunfat (Al2(SO4)3) và 3g hidro a)viết phương trình phản ứng b)tính khối lượng axit sunfuric đã dùng
a) \(PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b) Theo định luật bảo toàn khối lượng, ta có:
\(m_{Al}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2}\\ \Rightarrow27+m_{H_2SO_4}=171+3\\ \Rightarrow m_{H_2SO_4}=171+3-27=147\left(g\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2.
Dựa vào định luật bảo toàn khối lượng ta có:
\(m_{Al}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2}\)
\(27+m_{H_2SO_4}=171+3\)
=> \(m_{H_2SO_4}=171+3-27=147\left(g\right)\)
cho 108 gam al tác dụng với lượng dư axit sunfuric H2SO4 loãng,thu đc muối nhôm sunfu và khí H
a)viết PTHH xảy ra
b)tính KL axit tham gia phản ứng
c)tính thể tích khí H
Nhôm (III) oxit tác dụng với axit sunfuric theo phương trình phản ứng sau :
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tính lượng muối nhôm sunfat được tạo thành nếu đã sử dụng 49g axit sunfuric nguyên chất tác dụng với 60g nhôm oxit. Sau phản ứng chất nào còn dư ? Lượng dư của chất đó là bao nhiêu ?
Phương trình hóa học của phản ứng:
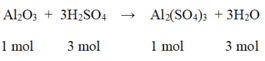
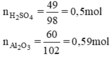
So sánh tỉ lệ 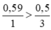 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
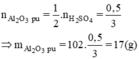
mAl2O3 (dư) = 60 - 17 = 43(g)
nAl = 5.4/27 = 0.2 mol
2Al + 3H2SO4 => Al2(SO4)3 + 3H2
0.2______________0.1________0.3
VH2 = 0.3*22.4 = 6.72 (l)
mAl2(SO4)3 = 0.1*342 = 34.2 g
Cho a gam nhôm (Al) tác dụng vừa đủ với dung dịch chứa 29,4 gam axit sunfuric H 2 S O 4 . Sau phản ứng thu được muối nhôm sunfat A l 2 S O 4 3 và khí hiđro H 2
Tính a gam nhôm đã tham gia phản ứng?