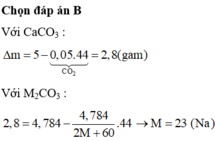Trên hai đĩa cân để hai cốc đựng hai dd HCl, H2SO4. Cân ở vị trí thăng bằng. Thêm vào cốc HCl 5g CaCO3, thêm vào cốc H2SO4 ag (a gam) Al, sau một thời gian, cân vẫn thăng bằng, hãy xác định giá trị của a?

Những câu hỏi liên quan
Trên hai đĩa cân để hai cốc đựng hai dd HCl, H2SO4. Cân ở vị trí thăng bằng. Thêm vào cốc HCl 5g CaCO3, thêm vào cốc H2SO4 ag (a gam) Al, sau một thời gian, cân vẫn thăng bằng, hãy xác định giá trị của a?
CaCO3 + 2HCl -> CaCl2 + CO2 + H2O
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
nCaCO3 = 0,05mol
=> nCO2 = nCaCO3 = 0,05mol
nAl = a/27mol
=> nH2 = 3/2nAl = a/18mol
Vì cân vẫn thăng bằng nên lượng khí thoát ra ở 2 cốc bằng nhau
=> mCO2 = mH2 => 0,05.44 = a/18.2 => a = 19,8g
Đúng 0
Bình luận (0)
trên hai đĩa cân để hai cốc nước đựng dung dịch HCl và H2SO4 sao cho cân ở vị trí cân bằng. Cho 25g CaCO3 vào cốc đựng dung dịch HCl, cho a(g) nhôm vào cốc đựng dung dịch H2SO4, cân vẫn ở vị trí thăng bằng. Tính a biết có các phản ứng xảy ra hoàn toàn theo phương trình hóa học sau: CaCo3+HCl=CaCl2+CO2+H2O, Al+H2SO4=Al2(SO4)3+H2
. Trên 2 đĩa cân để 2 cốc đựng dung dịch HCl và dung dịch H2SO4 sao cho cân ở vị trí thăng bằnga) Cho a gam Fe vào cốc đựng dung dịch H2SO4,cho b gam Al vào cốc đựng dung dịch HCl,cân ở vị trí thăng bằng.Tính tỉ lệ a/bb) Nếu cho a gam CaCO3 vào cốc đựng dung dịch HCl,cho b gam Na2SO3 vào cốc đựng dung dịch H2SO4,cân vẫn ở vị trí thăng bằng.Tính tỉ lệ a/bBiết PTPU xảy ra như sauCaCO3 + 2HCl -- CaCl2 + CO2 + H2ONa2SO3 + H2SO4 --- Na2SO4 + SO2 + H2O
Đọc tiếp
. Trên 2 đĩa cân để 2 cốc đựng dung dịch HCl và dung dịch H2SO4 sao cho cân ở vị trí thăng bằng
a) Cho a gam Fe vào cốc đựng dung dịch H2SO4,cho b gam Al vào cốc đựng dung dịch HCl,cân ở vị trí thăng bằng.Tính tỉ lệ a/b
b) Nếu cho a gam CaCO3 vào cốc đựng dung dịch HCl,cho b gam Na2SO3 vào cốc đựng dung dịch H2SO4,cân vẫn ở vị trí thăng bằng.Tính tỉ lệ a/b
Biết PTPU xảy ra như sau
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
Na2SO3 + H2SO4 ---> Na2SO4 + SO2 + H2O
a) Fe + H2SO4 \(\rightarrow\) FeSO4+ H2
2Al + 6HCl \(\rightarrow\) AlCl3 + 3H2
a+ mH2SO4- 2a /56= b + mHCl -1,5b/27
a/b=238/243
b) CaCO3 + 2HCl \(\rightarrow\) CaCl2 + CO2 + H2O
Na2SO3 + H2SO4 \(\rightarrow\) Na2SO4 + SO2 + H2O
a+ mHCl- 44a /100= b + mH2SO4 -64b/126
a/b=775/882
Đúng 1
Bình luận (0)
Giải rõ ra được không giúp với mình không hiểu lắm
Đúng 0
Bình luận (0)
Trên 2 đĩa cân để hai cốc đựng dung dịch HCl và H2SO4 sao cho cân ở vị trí thăng bằng:
- Hòa tan hết 15 gam Mg vào cốc đựng dung dịch HCl.
- Hòa tan hết a gam Fe vào cốc đựng dung dịch H2SO4.
Cân ở vị trí thăng bằng. Tính a.
- Thí nghiệm 1 : $n_{Mg} = \dfrac{15}{24} = 0,625(mol)$
$Mg + 2HCl \to MgCl_2 + H_2$
Theo PTHH : $n_{H_2} = n_{Mg} = 0,625(mol)$
$\Rightarrow m_{tăng} = m_{Mg} - m_{H_2} = 15 - 0,625.2 = 13,75(gam)$
- Thí nghiệm 2 :
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH : $n_{H_2} = n_{Fe} = \dfrac{a}{56}(mol)$
$m_{tăng} = a - \dfrac{a}{56}.2 = \dfrac{27a}{28}(gam)$
Mà cân ở vị trí cân bằng nên $13,75 = \dfrac{27a}{28} \Rightarrow a = 14,26(gam)$
Đúng 0
Bình luận (0)
BT: Cho 2 cốc đựng dung dịch HCl và H2SO4 vào 2 đĩa cân sao cho cân ở vị trí thăng bằng. Sau đó ta làm thí nghiệm như sau: - cho 21g MgCO3 vào cốc đựng dung dịch HCl. - cho m gam Al vào cốc dung dịch H2SO4. Cân vẫn ở vị trí thăng bằng, tính m, biết các phản ứng xảy ra hoàn toàn. Mọi người giải giúp em với ạ.
Cho 2 cốc đựng dung dịch HCl và H2SO4 vào 2 đĩa cân sao cho cân ở vị trí thăng bằng. Sau đó ta làm thí nghiệm như sau: - cho 21g MgCO3 vào cốc đựng dung dịch HCl. - cho m gam Al vào cốc dung dịch H2SO4. Cân vẫn ở vị trí thăng bằng, tính m, biết các phản ứng xảy ra hoàn toàn. Mọi người giải giúp em với ạ.
Giả sử mcốc 1 (bđ) = mcốc 2 (bđ) = a (g)
- Xét cốc 1:
\(n_{MgCO_3}=\dfrac{21}{84}=0,25\left(mol\right)\)
PTHH: MgCO3 + 2HCl --> MgCl2 + CO2 + H2O
0,25----------------------->0,25
=> mcốc 1 sau pư = a + 21 - 0,25.44 = a + 10 (g) (1)
- Xét cốc 2:
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)----------------------------->\(\dfrac{m}{18}\)
=> mcốc 2 sau pư = \(a+m-\dfrac{m}{18}.2=a+\dfrac{8}{9}m\left(g\right)\) (2)
(1)(2) => \(a+10=a+\dfrac{8}{9}m\)
=> m = 11,25 (g)
Đúng 1
Bình luận (0)
Trên 2 đĩa cân A và B có 2 cốc đựng dd H2SO4 (cốc A) và dd HCl (cốc B), cân ở vị trí cân bằng. Chi 13,44 gam kim loại Magie vào cốc A và 22 gam muối cacbonat của kim loại M hóa trị II vào cốc B. Sau khi phản ứng kết thúc, cân vẫn ở vị trí thăng bằng. Xác định kim loại hóa trị II, biết lượng axit trong 2 cốc đủ để tác dụng hết với kim loại và muối cacbonat
Đọc tiếp
Trên 2 đĩa cân A và B có 2 cốc đựng dd H2SO4 (cốc A) và dd HCl (cốc B), cân ở vị trí cân bằng. Chi 13,44 gam kim loại Magie vào cốc A và 22 gam muối cacbonat của kim loại M hóa trị II vào cốc B. Sau khi phản ứng kết thúc, cân vẫn ở vị trí thăng bằng. Xác định kim loại hóa trị II, biết lượng axit trong 2 cốc đủ để tác dụng hết với kim loại và muối cacbonat
\(n_{Mg}=\dfrac{13.44}{24}=0.56\left(mol\right)\)
TN1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.56................................0.56\)
TN2 :
\(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O\)
\(x............................x\)
Vì cân thăng bằng nên :
\(m_{Mg}-m_{H_2}=m_{MCO_3}-m_{CO_2}\)
\(\Rightarrow13.44-0.56\cdot2=22-44x\)
\(\Rightarrow x=0.22\)
\(M_{MCO_3}=\dfrac{22}{0.22}=100\left(g\text{/}mol\right)\)
\(\Rightarrow M=100-60=40\left(g\text{/}mol\right)\)
\(M:Ca\)
Đúng 2
Bình luận (0)
1.Trên hai đĩa cân A, B có 2 cốc đựng 2 dung dịch axit HCl (đĩa A), axit H2SO4 (đĩa B). Điều chỉnh lượng dung dịch ở hai đĩa để cân ở vị trí thăng bằng (hình vẽ).Cho 1,15 gam kim loại Na vào cốc đựng dung dịch HCl. Để cân về vị trí thăng bằng cần thêm bao nhiêu gam kim loại Mg vào cốc đựng dung dịch H2SO4?mn giải thích giúp mik với...
Đọc tiếp
1.Trên hai đĩa cân A, B có 2 cốc đựng 2 dung dịch axit HCl (đĩa A), axit H2SO4 (đĩa B). Điều chỉnh lượng dung dịch ở hai đĩa để cân ở vị trí thăng bằng (hình vẽ).
Cho 1,15 gam kim loại Na vào cốc đựng dung dịch HCl. Để cân về vị trí thăng bằng cần thêm bao nhiêu gam kim loại Mg vào cốc đựng dung dịch H2SO4?
mn giải thích giúp mik với...
Giả sử ban đầu mcốc A = mcốc B = m (g)
- Xét cốc A:
\(n_{Na}=\dfrac{1,15}{23}=0,05\left(mol\right)\)
PTHH: 2Na + 2HCl --> 2NaCl + H2
0,05-------------------->0,025
=> mcốc A (sau pư) = m + 1,15 - 0,025.2 = m + 1,1 (g)
- Xét cốc B
Gọi số mol Mg thêm vào là a (mol)
PTHH: Mg + 2HCl --> MgCl2 + H2
a---------------------->a
=> mcốc B (sau pư) = m + 24a - 2a = m + 22a (g)
Do mcốc A (sau pư) = mcốc B (sau pư)
=> m + 1,1 = m + 22a
=> a = 0,05 (mol)
=> mMg = 0,05.24 = 1,2 (g)
Đúng 2
Bình luận (0)
Cho 2 cốc đựng 2 dd HCl và H2SO4 loãng vào 2 đĩa cân sao cho cân ở vị trí thăng bằng. Sau đó làm thí nghiệm như sau: - cho 8,4g FE vào cốc đựng dung dịch HCl. - cho m g Al vào cốc đựng dd H2SO4. Cân ở vị trí cân bằng. Tính m?
- Xét cốc đựng HCl
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15-------------------->0,15
=> \(m_{tăng}=8,4-0,15.2=8,1\left(g\right)\) (1)
- Xét cốc đựng H2SO4:
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)---------------------------->\(\dfrac{m}{18}\)
=> \(m_{tăng}=m-\dfrac{m}{18}.2=\dfrac{8}{9}m\left(g\right)\) (2)
(1)(2) => \(\dfrac{8}{9}m=8,1\) => 9,1125 (g)
Đúng 1
Bình luận (0)
Hai cốc đựng dung dịch HCl (dư) đặt trên hai đĩa cân X,Y cân ở trạng thái thăng bằng. Cho 5 gam CaCO3 vào cốc X và 4,784 gam M2CO3 ( M: Kim loại kiềm ) vào cốc Y. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Xác định kim loại M? A. Cs B. Na C. K D. Li
Đọc tiếp
Hai cốc đựng dung dịch HCl (dư) đặt trên hai đĩa cân X,Y cân ở trạng thái thăng bằng. Cho 5 gam CaCO3 vào cốc X và 4,784 gam M2CO3 ( M: Kim loại kiềm ) vào cốc Y. Sau khi hai muối đã tan hoàn toàn, cân trở lại vị trí thăng bằng. Xác định kim loại M?
A. Cs
B. Na
C. K
D. Li