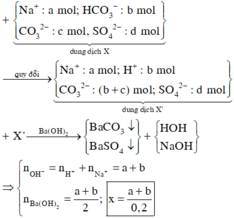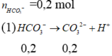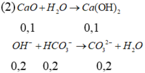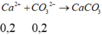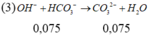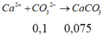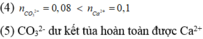dd A chứa các ion CO32-, SO42-, SO32-, 0.1 mol HCO3- và 0.3 mol Na+. Thêm V(l) dd Ba(OH)2 1M vào A thu lượng kết tủa lớn nhất. Tính V.

Những câu hỏi liên quan
Dung dịch X chứa các ion:
C
O
3
2
-
;
S
O
3
2
-
;
S
O
4
2
-
, 0,1 mol
H
C
O
3
-...
Đọc tiếp
Dung dịch X chứa các ion: C O 3 2 - ; S O 3 2 - ; S O 4 2 - , 0,1 mol H C O 3 - , 0,3 mol H S O 3 - và 1 mol K+. Thêm V lít dung dịch B a O H 2 1M vào X thì thu được lượng kết tủa lớn nhất. Giá trị nhỏ nhất của V là :
A. 0,15
B. 0,25.
C. 0,20
D. 0,30
Dung dịch X chứa a mol Na+, b mol NH4+, c mol HCO3-, d mol CO32, e mol SO42-. Thêm dần dần dung dịch Ba(OH)2 fM đến khi kết tủa đạt giá trị lớn nhất thì dùng hết V ml dung dịch Ba(OH)2. Cô cạn dung dịch sau phản ứng thì thu được khối lượng chất rắn là A. 35b gam. B. 40a gam. C. 20a gam. D. (40a + 35b) gam.
Đọc tiếp
Dung dịch X chứa a mol Na+, b mol NH4+, c mol HCO3-, d mol CO32, e mol SO42-. Thêm dần dần dung dịch Ba(OH)2 fM đến khi kết tủa đạt giá trị lớn nhất thì dùng hết V ml dung dịch Ba(OH)2. Cô cạn dung dịch sau phản ứng thì thu được khối lượng chất rắn là
A. 35b gam.
B. 40a gam.
C. 20a gam.
D. (40a + 35b) gam.
Dung dịch X chứa a mol Na+; b mol
H
C
O
3
-
; c mol
C
O
3
2
-
và d mol
S
O
4
2
-
. Để tạo kết tủa lớn nhất người ta p...
Đọc tiếp
Dung dịch X chứa a mol Na+; b mol H C O 3 - ; c mol C O 3 2 - và d mol S O 4 2 - . Để tạo kết tủa lớn nhất người ta phải dùng 100 ml dung dịch Ba(OH)2 x mol/l. Biểu thức tính x theo a và b là
![]()
![]()
![]()
![]()
Dung dịch A chứa : a mol Na+, b mol
HCO
3
-
, c mol Cl–, d mol
SO
4
2
-
. Để thu được kết tủa lớn nhất khi thêm 100 ml dung dịch Ba(OH)2 nồng độ xM. Giá trị của x là:
Đọc tiếp
Dung dịch A chứa : a mol Na+, b mol HCO 3 - , c mol Cl–, d mol SO 4 2 - . Để thu được kết tủa lớn nhất khi thêm 100 ml dung dịch Ba(OH)2 nồng độ xM. Giá trị của x là:
![]()
![]()
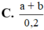
![]()
Cho 270ml dd Ba (OH)2 0.2M vào dd X chứa 0.025mol CO3 2-, 0.1 mol Na+, 0.25 mol NH4+, 0.3 mol Cl- và đun nóng nhẹ thu được dd Y. Khối lượng dd Y giảm đi bao nhiêu gam so với khối lượng các dd ban đầu
Dung dịch X chứa a mol Na+; b mol
H
C
O
3
-
; c mol
C
O
3
2
-
và d mol
S
O
4
2
-
. Để tạo kết tủa lớn nhất người ta phải dùng 100 ml dung dịch
B
a
O...
Đọc tiếp
Dung dịch X chứa a mol Na+; b mol H C O 3 - ; c mol C O 3 2 - và d mol S O 4 2 - . Để tạo kết tủa lớn nhất người ta phải dùng 100 ml dung dịch B a O H 2 x mol/l. Biểu thức tính x theo a và b là :
A. x = a + b 0 , 1
B. x = a + b 0 , 2
C. x = a + b 0 , 3
D. x = a + b 2
Chọn B
Chuyển ion H C O 3 - thành 2 ion ảo là C O 3 2 - và H+. Chuyển dung dịch X thành dung dịch ảo X’ gồm : a mol Na+; b mol H+, (b+c) mol C O 3 2 - và d mol S O 4 2 - . Cho B a O H 2 vào dung dịch X’ sẽ tạo ra kết tủa là B a S O 4 và B a C O 3 . Như vậy, các ion Na+ và H+ đã được thay thế bằng ion Ba2+. Áp dụng bảo toàn điện tích, ta có :
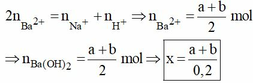
Đúng 0
Bình luận (0)
Dung dịch Y chứa các ion: Mg2+ (0,02 mol), Al3+ (0,01 mol), H+ (0,02 mol), Cl- (0,05 mol),
S
O
4
2
-
(x mol). Thêm vào dung dịch Y một lượng Ba(OH)2 sao cho khối lượng kết tủa tách ra khỏi dung dịch là lớn nhất. Tổng khối lượng kết tủa thu được là A. 3,4 gam. B. 6,6 gam. C. 5,82 gam. D. 4,66 gam.
Đọc tiếp
Dung dịch Y chứa các ion: Mg2+ (0,02 mol), Al3+ (0,01 mol), H+ (0,02 mol), Cl- (0,05 mol), S O 4 2 - (x mol). Thêm vào dung dịch Y một lượng Ba(OH)2 sao cho khối lượng kết tủa tách ra khỏi dung dịch là lớn nhất. Tổng khối lượng kết tủa thu được là
A. 3,4 gam.
B. 6,6 gam.
C. 5,82 gam.
D. 4,66 gam.
Theo định luật bảo toàn điện tích có:

Nên tổng khối lượng kết tủa thu được lớn nhất gồm 0,02 mol Mg(OH)2, 0,01 mol Al(OH)3 và 0,02 mol BaSO4
Đáp án B
Đúng 0
Bình luận (0)
Để khử tính cứng hoàn toàn một lượng nước các chứa: Na+ (0,1mol), Ca2+ (0,1 mol), Cl -(0,02 mol),
S
O
4
2
-
(0,04mol) và
H
C
O
3
-
. Người ta đưa ra các cách làm sau: (1)-Đun sôi rồi lọc bỏ kết tủa (2)-Thêm vào đó 5,6 gam CaO rồi lọc bỏ kết tủa (3)-Thêm vào đó 10 gam dd NaOH 30% rồi l...
Đọc tiếp
Để khử tính cứng hoàn toàn một lượng nước các chứa: Na+ (0,1mol), Ca2+ (0,1 mol), Cl -(0,02 mol), S O 4 2 - (0,04mol) và H C O 3 - . Người ta đưa ra các cách làm sau:
(1)-Đun sôi rồi lọc bỏ kết tủa
(2)-Thêm vào đó 5,6 gam CaO rồi lọc bỏ kết tủa
(3)-Thêm vào đó 10 gam dd NaOH 30% rồi lọc bỏ kết tủa
(4)-Thêm vào đó 100ml dd Na2CO3 0,3M và K2CO3 0,5M
(5)-Thêm vào đó lượng dư dd Na2CO3,
Chọn cách làm đúng:
A. 2, 3, 4
B. 1, 2, 5
C. 3, 4, 5
D. 1, 2, 4
HÒa tan hoàn tàon 6.98g hh X gồm cu,zns,mg vào đ chứa 0.3 mol h2so4 đặc nóng thu được dd Y( chỉ chứa các muối trung hòa) và 0.19 mol So2( chất khí duy nhất). Cho từ từ dd Ba(OH)2 vào đ y thì hết a mol thu dược khối lượng kết tủa lớn nhất m (g). Tìm a,m.
Hỗn hợp X chứa Cu x mol; ZnS y mol và Mg z mol
\(\rightarrow\)64x+97y+24z=6,98
Cho X tác dụng với H2SO4 đặc nóng thu được muối trung hòa là CuSO4; ZnSO4 và MgSO4
Bảo toàn S:
\(\rightarrow\)x+y+z=y +0,3 -0,19
Phản ứng:
Cu + 2HSO4 \(\rightarrow\) CuSO4 + SO2 + 2H2O
ZnS + 4H2SO4\(\rightarrow\) ZnSO4 + 4SO2 + 4H2O
Mg + 2H2SO4\(\rightarrow\) MgSO4 + SO2 + 2H2O
\(\rightarrow\)nSO2=nCu +4nZnS + nMg=x+4y+z=0,19
Giải được: x=0,06; y=0,02; z=0,05
Cho Ba(OH)2 vào muối thu được kết tủa lớn nhất
Ba(OH)2 + CuSO4\(\rightarrow\)Cu(OH)2 + BaSO4
Ba(OH)2 + ZnSO4 \(\rightarrow\) Zn(OH)2 + BaSO4
Ba(OH)2 + MgSO4 \(\rightarrow\) Mg(OH)2 + BaSO4
\(\rightarrow\) a=x+y+z=0,13 mol;
Kết tủa gồm BaSO4 0,13 mol; Cu(OH)2 0,06 mol; Zn(OH)2 0,02 mol; Mg(OH)2 0,05 mol
\(\rightarrow\)m=41,05 gam