Tính khối lượng CuSO4.5H2O cần thêm vào 500 gam dung dịch CuSO4 8% để thu được dung dịch CUSO4 15%z
Giúp e với ạ !!
Tính khối lượng CuSO4.5H2O cần thêm vào 500g dung dịch CuSO4 8% để thu được dung dịch CuSO4 15%?
\(m_{CuSO_4\left(8\%\right)}=500\cdot8\%=40\left(g\right)\)
\(n_{CuSO_4\cdot5H_2O}=a\left(mol\right)\)
\(\Rightarrow n_{CuSO_4}=a\left(mol\right)\)
\(m_{CuSO_4\left(15\%\right)}=160a+40\left(g\right)\)
\(m_{dd_{CuSO_4\left(15\%\right)}}=250a+500\left(g\right)\)
\(C\%_{CuSO_4}=\dfrac{160a+40}{250a+500}\cdot100\%=15\%\)
\(\Leftrightarrow a=\dfrac{2}{7}\)
\(m_{CuSO_4\cdot5H_2O}=\dfrac{2}{7}\cdot250=71.42\left(g\right)\)
a) Cần lấy bao nhiêu gam tinh thể CuSO4.5H2O và bao nhiêu gam dung dịch CuSO4 8% để điều chế được 280g dung dịch CuSO4 15%
b) Khối lượng riêng của một dung dịch CuSO4 là 1,206 g/ml. Đem cô cạn 414,594 ml dung dịch này thu được 140,625g tinh thể CuSO4.5H2O. Tính nồng độ C% và CM của dung dịch nói trên.
a)
Gọi $n_{CuSO_4.5H_2O} = a(mol) ; m_{dd\ H_2SO_4\ 8\%} = b(gam)$
Sau kho pha :
$m_{dd} = 250a + b = 280(1)$
$m_{CuSO4} = 160a + b.8\% = 280.15\%(2)$
Từ (1)(2) suy ra a = 0,14; b = 245(gam)
$m_{CuSO4.5H_2O} = 0,14.250 = 35(gam)$
b)
$n_{CuSO_4} = n_{CuSO_4.5H_2O} = \dfrac{140,625}{250} = 0,5625(mol)$
414,594 ml = 0,414594 lít
Suy ra :
$C_{M_{CuSO_4}} = \dfrac{0,5625}{0,414594} = 1,36M$
$m_{dd} = D.V = 1,206.414,594 = 500(gam)$
Suy ra :
$C\%_{CuSO_4} = \dfrac{0,5625.160}{500}.100\% = 18\%$
Tính khối lượng tinh thể CuSO4.5H2O cần dùng hòa tan hoàn toàn vào 400 gam dung dịch CuSO4 2% để thu được dung dịch CuSO4 1M ( D = 1,1 g/ml).
Gọi số mol CuSO4.5H2O cần lấy là x (mol) => nCuSO4 = x (mol)
Khối lượng CuSO4 2% có trong 400 gam dung dịch là:
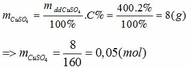
Tổng số mol CuSO4 sau khi hòa tan là: x + 0,05 (mol)
=> thể tích dung dịch sau khi hòa tan:

Từ (1) và (2)
=> (x+ 0,05).1000
=> 1100x + 55 = 160x + 400
=> 850x = 345
=> x ≈0, 406 (mol)
=> mCuSO4.5H2O = 0,406.250 = 101,47 (g)
Tính khối lượng CuSO4.H2O cần thêm vào 500 gam dung dịch CuSO4 8% để thu được dung dịch CuSO4 15%
\(n_{CuSO4}.H_2O=a\)
\(\rightarrow n_{CuSO4}=a,m_{CuSO4}.H_2O=178a\)
mCuSO4 trong dung dịch ban đầu\(=500.8\%=40\left(g\right)\)
Khối lượng dung dịch sau đó là 500+178a
Khối lượng CuSO4=160a+40
\(\rightarrow C\%_{CuSO4}=\frac{100a+40}{500+178a}=15\%\)
\(\rightarrow a=\frac{350}{1333}\)
->mCuSO4.H2O=178a=46,74
a
mCuSO4 = 500g.16% = 80g
nCuSO4 = nCuSO4.5H2O = 80 : 160 = 0,5mol
mCuSO4.5H2O = 0,5.250 = 125 g → mH2O = 500 - 125 = 375g
dùng bình có thể tích > 500ml
cho 125 gam CuSO4.5H2O và 375 gam nước cho vào bình khuấy đều
b
CuSO4 trong X = CuSO4 trong Y = 80g
mY = 500g - 100g = 400g → C% của Y = (80.100%) : 400 = 20 (%)
Sau khi CuSO4.5H2O tách ra khỏi Y, phần còn lại vẫn là dung dịch bão hòa nên khối lượng CuSO4 và H2O tách ra khỏi Y cũng phải theo tỉ lệ như dung dịch bão hòa = 20/80
Trong 10gam CuSO4.5H2O có 6,4g CuSO4 và 3,6g H2O
Khối lượng CuSO4 tách ra khỏi Y là 6,4 - m
m = 5,5
Dung dịch CuSO4 loãng được dùng làm thưốc diệt nấm. Để điều chế 800 gam dung dịch CuSO4 5% thì khối lượng CuSO4.5H2O cần dùng là?
A. 62,5 gam
B. 40,0 gam
C. 32,0 gam
D. 25,6 gam
Đáp án : A
nCuSO4 = nCuSO4.5H2O = 0,25 mol
=> mCuSO4.5H2O = 62,5g
Cần lấy bao nhiêu gam CuSO4.5H2O và bao nhiêu gam dung dịch CuSO4 4% để điều chế 500 gam dung dịch CuSO4 8%
Tính khối lượng SO3 cần thêm vào 500 gam dung dịch H2SO4 22,5 % để thu được dung dịch H2SO4 42,5%.
Mong đc giúp đỡ ạ
\(n_{SO_3}=a\left(mol\right)\)
\(m_{H_2SO_4}=500\cdot22.5\%=112.5\left(g\right)\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(a.................a\)
\(m_{H_2SO_4}=98a+112.5\left(g\right)\)
\(m_{dd_{H_2SO_4}}=80a+500\left(g\right)\)
\(C\%_{H_2SO_4}=\dfrac{98a+112.5}{80a+500}\cdot100\%=42.5\%\)
\(\Leftrightarrow a=1.5625\)
\(m_{SO_3}=125\left(g\right)\)
Số mol SO3 cần thân vào là x (mol)
Ta có: SO3 + H2O -> H2SO4
x x
mH2SO4 tạo thành là: 98x (gam)
mH2SO4 22,5% là: 500 x 22,5% = 112,5 (gam)
-> (98x + 112,5). 100/80x + 500 = 42,5
-> x = 1,5625
mSO3 = 1,5625 x 80 = 125 (gam)
Để thu được dung dịch CuSO4 16% cần lấy m1 gam tinh thể CuSO4.5H2O cho vào m2 gam dung dịch CuSO4 8%. Tỉ lệ m1/m2 là
\(n_{CuSO_4.5H_2O}=\frac{m_1}{250}\left(mol\right)\)
=> \(n_{CuSO_4\left(thêm\right)}=n_{CuSO_4.5H_2O}=\frac{m_1}{250}\left(mol\right)\)
\(=>m_{CuSO_4\left(thêm\right)}=\frac{m_1}{250}.160=\frac{16.m_1}{25}\left(g\right)\)
\(m_{CuSO_4\left(bđ\right)}=\frac{m_2.8}{100}=0,08.m_2\left(g\right)\)
=> \(C\%\) (dd mới) = \(\frac{\frac{16.m_1}{25}+0,08.m_2}{m_1+m_2}.100\%=16\%\)
=> \(\frac{m_1}{m_2}=\frac{1}{6}\)