Để trung hòa 0,826 gam oleum cần dùng 100ml dung dịch NaOH 0,75M. Công thức của oleum là:

Những câu hỏi liên quan
Để trung hòa 0,826g oleum cần dùng 100ml dung dịch NaOH 0,175M. Tính tỉ lệ số mol giữa SO3 và H2SO4 trong mẫu oleum đó, tức tìm công thức của oleum.
\(CT:H_2SO_4\cdot nSO_3\left(x\right)\)
\(n_{NaOH}=0.1\cdot0.175=0.0175\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.0175...0.0175\)
\(n_{H_2SO_4}=8.75\cdot10^{-3}\left(mol\right)\)
\(BTS:\)
\(n_{H_2SO_4}=x+xn=8.75\cdot10^{-3}\left(1\right)\)
\(m=98x+80xn=0.826\left(2\right)\)
\(\left(1\right),\left(2\right):\) \(x=7\cdot10^{-3},xn=1.75\cdot10^{-3}\)
\(\Rightarrow n=4\)
\(\dfrac{n_{SO_3}}{n_{H_2SO_4}}=4\)
\(CT:H_2SO_{_{ }4}\cdot4SO_3\)
Đúng 1
Bình luận (0)
Hòa tan 3,38 gam oleum A vào lượng nước dư ta được dung dịch A. Để trung hòa 1/20 lượng dung dịch A cần dùng 40 ml dung dịch NaOH 0,1M. Tìm công thức của oleum
CTPT oleum: H2SO4.nSO3 có x (mol)
H2SO4.nSO3 + nH2O → (n + 1)H2SO4
x → x(n + 1)
H2SO4 + 2NaOH → Na2SO4 + 2H2O
x(n + 1)→ 2x(n + 1)
=> (98 + 80n)x = 3,38 và 2x (n + 1) = 0,08
=> x = 0,01 và nx = 0,03
=> n = 3
Suy ra CTPT oleum: H2SO4.3SO3
Đúng 0
Bình luận (0)
Một loại oleum có công thức H2SO4.nSO3. Lấy 33,8 g oleum nói trên pha thành 100ml dung dịch A. Để trung hoà 25 ml dung dịch A cần dùng vừa đủ 100ml dung dịch NaOH 2M. Giá trị của n là
A. 1
B. 2
C. 3
D. 4
Đáp án C
Giải:
nH2SO4=1/2 nNaOH = 0,1 => nH2SO4 tạo thành = 0,4 H2SO4.nSO3+nH2O -> (n+1)H2SO4
=> noleum = 0,4/(n+1) => 98+80n = 33,8(n+1)/0,4 => n=3
Đúng 0
Bình luận (0)
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là A.
H
2
SO
4
.
nSO
3
B.
H
2
SO
4
.
5
SO
3
C.
H
2
SO...
Đọc tiếp
Hòa tan 6,76 gam oleum vào nước dung dịch Y, để trung hòa dung dịch Y cần 160 ml dung dịch NaOH 1M. Công thức phân tử tử oleum là
A. H 2 SO 4 . nSO 3
B. H 2 SO 4 . 5 SO 3
C. H 2 SO 4 . 3 SO 3
D. H 2 SO 4 . 4 SO 3
Đáp án C
Số mol NaOH là: n NaOH = 0 , 16 . 1 = 0 , 16 mol
Đặt công thức của oleum là H 2 SO 4 . nSO 3
Oleum tác dụng với H 2 O :
H 2 SO 4 . nSO 3 + nH 2 O → ( n + 1 ) H 2 SO 4 ( 1 )
Dung dịch Y là dung dịch H 2 SO 4 . Trung hòa dung dịch Y bằng dung dịch NaOH:
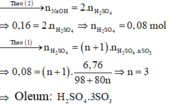
Đúng 0
Bình luận (0)
hòa tan 8,6 gam oleum X vào nước được dung dịch Y . Để trung hòa dung dịch Y cần 200 ml dung dịch NaOH 1M . Công thức của oleum X là gì ?
Gọi CT oleum là H2SO4.nSO3 a mol
Hòa tan vào H2O tổng nH2SO4=a+an mol
nNaOH cần=0,2 mol
SO3 + H2O =>H2SO4
an mol =>an mol
H2SO4 +2 NaOH =>Na2SO4 + 2H2O
0,1 mol<=0,2 mol
=>a+an=0,1
Mà m oleum=8,6=a(98+80n)
Giải hpt có a=1/30 và an=1/15
=>n=2
CT oleum H2SO4.2SO3
Đúng 0
Bình luận (0)
Cho 1,69 gam một oleum có công thức H2SO4.3SO3 vào nước dư thu được dung dịch X. Để trung hòa dung dịch X cần dùng vừa đủ V lít dung dịch NaOH 2M. Giá trị của V là: A. 20 B. 40 C. 80 D. 10
Đọc tiếp
Cho 1,69 gam một oleum có công thức H2SO4.3SO3 vào nước dư thu được dung dịch X. Để trung hòa dung dịch X cần dùng vừa đủ V lít dung dịch NaOH 2M. Giá trị của V là:
A. 20
B. 40
C. 80
D. 10
Đáp án : A
nOleum = 0,005 mol => nH2SO4 sau hòa tan = nS(Oleum) = 4nOleum = 0,02 mol
=> nNaOH = 2V = 2nH2SO4 = 0,04 mol => V = 0,02 lit = 20 ml
Đúng 0
Bình luận (0)
Hoà tan 3,38 gam oleum vào nước được dung dịch X. Để trung hoà dung dịch X cần 800ml dung dịch KOH 0,1 M. Công thức phân tử oleum đã dùng là A. H2SO4 .4SO3 B. H2SO4 .2SO3 C. H2SO4 .nSO3 D. H2SO4 .3SO3.
Đọc tiếp
Hoà tan 3,38 gam oleum vào nước được dung dịch X. Để trung hoà dung dịch X cần 800ml dung dịch KOH 0,1 M. Công thức phân tử oleum đã dùng là
A. H2SO4 .4SO3
B. H2SO4 .2SO3
C. H2SO4 .nSO3
D. H2SO4 .3SO3.
Đáp án D
Gọi công thức oleum là H2SO4.nSO3
=> Sau hòa tan vào H2O:
nH+ = 2nH2SO4 sau = 2(nH2SO4 + nSO3)
= 2(n+1)nOleum
=> nKOH = nH+ = 2(n+1) .3,38/(98+80n)
=0,08 mol
=> n = 3
Đúng 0
Bình luận (0)
axit H2SO4 100% hấp thụ SO3 tạo ra oleum theo phương trình H2SO4 + SO3 -> H2SO4.nSO3 . Hòa tan 6,76 gam gam oleum vào nước thành 200 ml dung dịch H2SO4 . 10 ml dung dịch trung hòa vừa hết 16 ml dung dịch NaOH 0,5 M a- tính n b- tính hàm lượng % SO3 trong oleum c- cần có bao nhiêu gam oleum có hàm lượng SO3 như trên để pha vào 100 ml dung dịch H2SO4 40% , d= 1,31 g/ml để tạo ra oleum có hàm lượng SO3 là 10%.
H2SO4 + nSO3 => H2SO4.nSO3
H2SO4.nSO3 + nH2O >> n+1H2SO4
H2SO4 + 2NaOH >> Na2SO4 + 2H2O
Số mol NaOH = 0,008 , số mol H2SO4 200ml = 0,008/2 . 200/10 =0,08
Theo (2) nH2SO4.nSO3 =0,08/n+1
MH2SO4.nSO3 =98 +80n = 6,76/0,08/n+1 =84,5n+ 84,5
13,5 =4,5n
=>n=3
%SO3=3.80/2.80+98 =71%
c,Theo câu b , hàm lượng % của SO3 có trong oleum trên là 71
Cứ 100g oleum có 71g SO3 và 29g H2SO4 Khi đó mdd = 1,31.100 = 131g
a g có 71a/100 ...............29a/100
Vì dd H2SO4 có C=40%
Cứ 100g dd có 40g H2SO4 và 60g H2O
=>131g >> 131.40/100 = 52,4g H2SO4 và 131.60/100 = 78,6 g H2O
Khi cho oleum vào dd H2SO4 thì SO3+H2O
SO3 + H2O >> H2SO4
Cứ 80g cần 18g >> 98g
Vậy ..x..g cần 78,6g >>..y..g
x= 78,6.80/18 = 349,3g
y= 78,6.98/18 = 427,9g
Trong loại oleum mới 10% thì mSO3 = 71a/100 -349,3g
và mH2SO4 = 29a/100 +52,4+ 427,9
=> 71a/100 -349,4 / 29a/100 +480,3 = 10/90
=> Bạn ấn máy tìm a nhé
Đúng 1
Bình luận (0)
Cho 4,98 gam oleum hòa tan vào nước thu được dung dịch A. Để trung hòa hết A cần 600ml Ba(OH)2 0,1M thu được m gam kết tủa.
a, Xác định công thức của oleum
b, Tính khối lượng kết tủa ?
c, Tính khối lượng oleum cần để hòa tan vào 500ml nước tạo thành dung dịch H2SO4 20%
H2SO4.nSO3+H2O --> (n+1)H2SO4
H2SO4+Ba(OH)2 -> BaSO4 + 2H2O
a.nBaSO4= 0,06 mol
=> nH2SO4=0,06 mol
ta có PT
\(\dfrac{4,98}{98+80n}=\dfrac{0,06}{n+1}\)
=> n=5. CT H2SO4.5SO3
b. mBaSO4= 0,06*233=13,98(g)
c)a mol H2SO4 5SO3
=> mol SO3 = 5a và H2SO4 a mol
SO3 + H2O --> H2SO4
5a--------5a----------5a
=> mol H2SO4 6a mol => mH2SO4 = 588a
=>
m dd sau hòa tan = mH2O + mA = 500 + 498a
Bảo toàn m H2SO4: 588a = 0,2(500 + 498a) => a => mA = 498a
Đúng 3
Bình luận (1)














