Hấp thụ hoàn toàn 2,24 lít khí SO2 (đktc) vào 200ml dd NaOH 1,5M
a, Viết pthh của các phản ứng có thể xảy ra
b, Tính khối lượng muối tạo thành sau phản ứng
Hấp thụ hoàn toàn 4.48 lít khí so2(đktc) vào dd chứa 10g NAOH. a.viết pthh của phản ứng có thể xảy ra. b.tính khối lượng muối tạo thành sau phản ứng
Hấp thụ hoàn toàn 12,8g SO2 vào 250ml dung dịch NaOH 1M.
Viết các phương trình hóa học của phản ứng có thể xảy ra.
Tính khối lượng muối tạo thành sau phản ứng

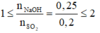 ⇒ phản ứng tạo 2 muối
⇒ phản ứng tạo 2 muối
Phương trình hóa học của phản ứng
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
Gọi nNa2SO3 = x mol; nNaHSO3 = y mol
nNaOH = 2x + y = 0,25.
nSO2 = x + y = 0,2.
Giải ra ta có: x = 0,05, y = 0,15.
mNaHSO3 = 0,15 x 104 = 15,6g.
mNa2SO3 = 0,05 x 126 = 6,3g.
Hấp thụ hoàn toàn 8,96 lít khí SO2 (đktc) vào 500ml dung dịch NaOH 1,2M. Tính khối lượng muối tạo thành sau phản ứng, tính nồng độ mol của muối sau phản ứng
hấp thụ hoàn toàn 12,8 gam SO vào 250 ml dung dịc NaOH 1M : a) viết phương trình hóa học của các phản ứng có thể xảy ra ; b) tính khối lượng muối tạo thành sau phản ứng .
a)NaOH+SO2 \(\rightarrow\) NaHSO3 (1)
NaOH+SO2 \(\rightarrow\) Na2SO3+H2O (2)
b)Ta có co số mol SO2 là : n = 12,8 / 64 = 0,2
số mol NAOH là : n =0,25 x 1 = 0,25
Ta có tỷ lệ :
n [NaOH]/ n [SO2] = 0,25/0,2 = 1,25
Nên sẽ xảy ra đồng thời 2 phản ứng 1 và 2
NaOH + SO2 = NaHSO3 (1)
x mol x mol x mol
2NaOH + SO2 = Na2So3 + H2O (2)
y mol y/2 mol y/2 mol
Từ (1)(2): Ta có hệ phương trình :
x+y = 0,25
x+y/2 = 0,2
Giải hệ trên ta có x = 0,15 mol
y= 0,1 mol
Khối lượng muối sau phản ứng sẽ bao gồm 2 muối là NaHSO3 và NA2SO3
Số mol Nahso3 = x = 0,15 mol
==> Khối lương NAHSO3 = 0,15 x 104 = 15,6 g
Số mol NA2SO3 = y/2 = 0,1 /2 = 0,05 mol
==> Khối lượng NA2SO3 = 0,05 x 126 = 6,3 g
Vậy khối lượng muối thu dc sau phản ứng là : 15,6 + 6,3 = 21,9 g
1. Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào 100ml dd NaOH. Sau phản ứng nung từ từ dung dịch thu đc 9,5g muối khan. Tính nồng độ mol của dd NaOH đã dùng
2. Người ta dẫn 2,24 lít CO2 qua bình đựng dd NaOH. Khí CO2 bị hấp thụ hoàn toàn. Sau phản ứng thu được muối nào tạo thành? khối lượng là bn?
1.nCO2=0,1 (mol )
TH1: Số mol của CO2 dư => Khối lượng muối khan tối đa tạo được là:
mmuối=0,1.84=8,4<9,5 (loại )
TH2: CO2 hết
Gọi số mol CO2 tạo muối Na2CO3;NaHCO3 lần lượt là x, y
2NaOH+CO2→Na2CO3+H2O
NaOH+CO2→NaHCO3
Ta có : \(\left\{{}\begin{matrix}x+y=0,1\\106x+84y=9,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
⇒nNaOH=2.0,05+0,05=0,15 (mol)
⇒CMNaOH=\(\dfrac{0,15}{0,1}\)=1,5M
Câu 2 thật ra anh thấy chưa chặt chẽ nha!
2. Vì CO2 bị hấp thụ hoàn toàn
=> CO2 hết, NaOH dư
nCO2 = 0,1 (mol)
CO2 + 2NaOH -------> Na2CO3 + H2O
\(n_{Na_2CO_3}=n_{CO_2}=0,1\left(mol\right)\)
=> \(m_{Na_2CO_3}=0,1.106=10,6\left(g\right)\)
Dẫn 6,72 lít khí Clo (đktc) vào dd chứa 120 g NaI. a) Viết pt phản ứng hóa học xảy ra. b) Tính khối lượng muối tạo thành trong dung dịch sau khi phản ứng xảy ra hoàn toàn.
Cl2+2NaI->2NaCl+I2
0,3-----0,6-----0,6----0,3 mol
n Cl2=\(\dfrac{6,72}{22,4}\)=0,3 mol
n NaI=\(\dfrac{120}{150}\)=0,8 mol
=>NaI dư
=>m NaCl=0,6.58,5=35,1g
=>m NaI dư=0,2.150=30g
\(n_{Mg}=0,3\left(mol\right)\)
\(n_{HCl}=0,3\left(mol\right)\)
\(PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\)
...............0,15......0,3..........0,15.....0,15......
- Thấy sau phản ứng HCl phản ứng hết, Mg còn dư ( dư 0,15 mol )
\(\Rightarrow\left\{{}\begin{matrix}m_M=m_{MgCl_2}=14,25\left(g\right)\\V=V_{H_2}=3,36\left(l\right)\end{matrix}\right.\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
\(n_{HCl}=0,2.1,5=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,3}{2}\), ta được Mg dư.
Theo PT: \(n_{MgCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,15.95=14,25\left(g\right)\\V_{H_2}=0,15.22,4=3,36\left(l\right)\end{matrix}\right.\)
Bạn tham khảo nhé!
Cíu TT Hấp thụ hoàn toàn 6,72 lít khí SO2 (đktc) vào 200ml dd KOH 2M. Viết ptpư và tính khối lượng muối tạo thành
Dẫn toàn bộ 2,24 lít khí cacbon đioxit ( CO 2 ) đo ở ( đktc) vào 200ml dung
dịch NaOH. Biết sau phản ứng xảy ra hoàn toàn ta thu được muối trung hòa.
a. Viết phương trình phản ứng xảy ra.
b. Tính nồng độ mol của dung dịch NaOH tham gia phản ứng.
c. Tính khối lượng muối trung hòa tạo thành.
( C = 12, O =16, Na = 23, H = 1)
\(a/ CO_2+2NaOH \to Na_2CO_3+H_2O\\ n_{CO_2}=0,1(mol)\\ b/\\ n_{NaOH}=0,1.2=0,2(mol)\\ CM_{NaOH}=\frac{0,2}{0,2}=1M\\ c/\\ n_{Na_2CO_3}=n_{CO_2}=0,1(mol)\\ m_{Na_2CO_3}=0,1.106==10,6(g)$\)
\(n_{CO2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) Pt : \(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O|\)
1 2 1 1
0,1 0,2 0,1
b) \(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
200ml = 0,2l
\(C_{M_{ddNaOH}}=\dfrac{0,2}{0,2}=1\left(M\right)\)
c) \(n_{Na2CO3}=\dfrac{0,2.1}{2}=0,1\left(mol\right)\)
⇒ \(m_{Na2CO3}=0,1.106=10,6\left(g\right)\)
Chúc bạn học tốt