Viết ptpu H2S tác dụng với O2 ( trường hợp đủ oxi)

Những câu hỏi liên quan
a) Viết ptpu của alanin b) Cho 26,7g alanin tác dụng vừa đủ với dd NaOH Viết ptpu, tính khối lượng muối thu được
Viết các phương trình hóa học xảy ra trong trường hợp sau: Cho H 2 S tác dụng với S O 2
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa khử là: A. 6 B. 3 C. 4 D. 5
Đọc tiếp
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa khử là:
A. 6
B. 3
C. 4
D. 5
Các chất tác dụng với H2SO4 đặc nóng là phản ứng oxi hóa khử gồm: FeSO4, H2S, HI, Fe3O4
Chú ý: AgNO3, Fe2O3 có mức oxi hóa tối đa, khi tác dụng với H2SO4 đặc nóng chỉ là phản ứng trao đổi.
Na2SO3 tác dụng với H2SO4 đặc nóng cũng là phản ứng trao đổi và sinh khí SO2. Đáp án C.
Đúng 0
Bình luận (0)
Cho các chất riêng biệt: Fe(NO3)2; NaI; K2SO3; Fe3O4; H2S; FeCO3; NaCl tác dụng với dung dịch H2SO4đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là. A. 6 B. 7 C. 5 D. 4
Đọc tiếp
Cho các chất riêng biệt: Fe(NO3)2; NaI; K2SO3; Fe3O4; H2S; FeCO3; NaCl tác dụng với dung dịch H2SO4đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là.
A. 6
B. 7
C. 5
D. 4
Các chất có phản ứng oxi hóa khử là Fe(NO3)2; NaI; K2SO3; Fe3O4; H2S; FeCO3
=> Đáp án A
Đúng 0
Bình luận (0)
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là A. 6. B. 3. C. 4. D. 5
Đọc tiếp
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là
A. 6.
B. 3.
C. 4.
D. 5
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là A. 6 B. 3. C. 4. D. 5
Đọc tiếp
Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, HI, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng. Số trường hợp xảy ra phản ứng oxi hóa - khử là
A. 6
B. 3.
C. 4.
D. 5
Để 14.8g hỗn hợp gồm Fe và Cu trong khí Oxi sau 1 thời gian thu được19.2g hỗn hợp X gồm CuO ,Fe2O3,FeO,Fe3O4 hỗn hợp X tác dụng vừa đủ với m g HCl a) Viết PTHH b) Tính V O2(ĐKTC) đã phản ứng c) Tính m
\(a) 4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3\\ 2Fe + O_2 \xrightarrow{t^o}2FeO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\)
b)
Bảo toàn khối lượng :
\(m_{kim\ loại} + m_{O_2} = m_{oxit}\\ \Rightarrow n_{O_2} = \dfrac{19,2-14,8}{32} = 0,1375(mol)\\ V_{O_2} = 0,1375.22,4 =3,08(lít)\)
c)
\(n_{O(oxit)} = 2n_{O_2} = 0,1375.2 = 0,275(mol)\\ 2H^+ + O^{2-} \to H_2O\\ n_{HCl} = n_{H^+} = 2n_O = 0,275.2 = 0,55(mol)\\ m = 0,55.36,5 = 20,075(gam)\)
Đúng 1
Bình luận (0)
Cho khí H2S tác dụng với các chất: dung dịch NaOH, khí clo, nước clo, dung dịch KMnO4/H+, khí oxi dư đun nóng, dung dịch FeCl3, dung dịch ZnCl2, Pb(NO3)2, KClO3. Số trường hợp xảy ra phản ứng và số trường hợp trong đó lưu huỳnh bị oxi hóa lên S+6 là A. 8 – B. 6 - C. 9 - 3 D. 6 -2
Đọc tiếp
Cho khí H2S tác dụng với các chất: dung dịch NaOH, khí clo, nước clo, dung dịch KMnO4/H+, khí oxi dư đun nóng, dung dịch FeCl3, dung dịch ZnCl2, Pb(NO3)2, KClO3. Số trường hợp xảy ra phản ứng và số trường hợp trong đó lưu huỳnh bị oxi hóa lên S+6 là
A. 8 –
B. 6 -
C. 9 - 3
D. 6 -2
Đáp án : A
Có 8 chất phản ứng trừ dung dịch ZnCl2
Các trường hợp S bị oxi hóa lên +6 là : nước clo
Đúng 0
Bình luận (0)
Cho khí H2S tác dụng lần lượt với: dung dịch NaOH, khí clo, nước clo, dung dịch KMnO4/H+; khí oxi dư đun nóng, dung dịch FeCl3, dung dịch ZnCl2. Số trường hợp xảy ra phản ứng là: A. 4 B. 5 C. 6 D. 7
Đọc tiếp
Cho khí H2S tác dụng lần lượt với: dung dịch NaOH, khí clo, nước clo, dung dịch KMnO4/H+; khí oxi dư đun nóng, dung dịch FeCl3, dung dịch ZnCl2. Số trường hợp xảy ra phản ứng là:
A. 4
B. 5
C. 6
D. 7
Chọn đáp án C
Số trường hợp xảy ra phản ứng là: dung dịch NaOH, khí clo, nước clo, dung dịch KMnO4/H+; khí oxi dư đun nóng, dung dịch FeCl3, dung dịch ZnCl2.
Các phương trình phản ứng:
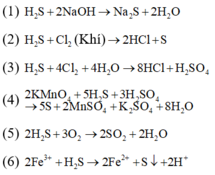
Đúng 0
Bình luận (0)







