Từ các chất ban đầu là:đá vôi,nước.Hãy trình bày phương pháp để điều chế hai oxit và hai đơn chất khí khác nhau từ các chất trên

Những câu hỏi liên quan
từ các chất ban đầu là đá vôi (CaCO3 ) , nước . hãy trình bày phương pháp điều chế 2 oxit và 2 đơn chất khí khác nhau từ các chất trên
CaCO3 -> (t°) CaO + CO2
2H2O -> (điện phân) 2H2 + O2
- Hai oxit: CaO (canxi oxit) và CO2 (cacbon đioxit)
- Hai đơn chất khí: H2 (hiđro) và O2 (oxi)
Đúng 0
Bình luận (0)
từ các chất ban đầu là đá vôi ( CaCO3 ) , nước . hãy trình bày phương pháp điều chế hai oxit và hai đơn chất khi khác nhau từ các chất trên 2) đốt cháy hoàn toàn a gam chất X cần phải dùng vừa đủ 10,08 lít O2 ở dktc . sau khi kết thúc phản ứng cháy , thu dc 13,2g CO2 và 7,2g H2O a) tính a và tìm công thức hh của X ( biết cthh của X trùng với công thức đơn giản nhất ).b) viết phương trình hóa học của phản ứng đốt cháy X
Đọc tiếp
từ các chất ban đầu là đá vôi ( CaCO3 ) , nước . hãy trình bày phương pháp điều chế hai oxit và hai đơn chất khi khác nhau từ các chất trên
2) đốt cháy hoàn toàn a gam chất X cần phải dùng vừa đủ 10,08 lít O2 ở dktc . sau khi kết thúc phản ứng cháy , thu dc 13,2g CO2 và 7,2g H2O a) tính a và tìm công thức hh của X ( biết cthh của X trùng với công thức đơn giản nhất ).b) viết phương trình hóa học của phản ứng đốt cháy Xcâu 1
-Nung CaCO3 :
CaCO3 -to-> CaO + CO2
+ Hai oxit : CaO ( oxit bazơ), CO2 (oxit axit)
- Điện phân H2O :
2H2O -đp-> 2H2 + O2
+Hai đơn chất khí là: H2 và O2
Chúc bạn học tốt <3
câu 2
HD:
Gọi CTHH của X là CxHyOz.
CxHyOz + (x + y/2 - z/4)O2 ---> xCO2 + y/2H2O
Số mol O2 = 10,08/22,4 = 0,45 mol. Khối lượng O2 = 32.0,45 = 14,4 g.
Áp dụng ĐLBTKL ta có: m + 14,4 = 13,2 + 7,2 (m là khối lượng của X). Thu được: m = 6 g.
Khối lượng C = 12.13,2/44 = 3,6 g; Khối lượng H = 2.7,2/18 = 0,8 g; khối lượng O = 6 - 3,6 - 0,8 = 1,6 g.
Như vậy: 12x:y:16z = 3,6:0,8:1,6 hay x:y:z = 0,3:0,8:0,1 = 3:8:1. suy ra X có CT: C3H8O.
Câu 2.
\(n_{CO_2}=\dfrac{13,2}{44}=0,3mol\Rightarrow m_C=0,3\cdot12=3,6g\)
\(n_{H_2O}=\dfrac{7,2}{18}=0,4mol\Rightarrow m_H=0,4\cdot2\cdot1=0,8g\)
\(n_{O_2}=\dfrac{10,08}{22,4}=0,45mol\)
BTKL: \(a+m_{O_2}=m_{CO_2}+m_{H_2O}\)
\(\Rightarrow a+0,45\cdot32=13,2+7,2\Rightarrow a=6g\)
Mà \(\Sigma n_{C+H}< n_X\Rightarrow\)CTHH chứa Oxi.
\(\Rightarrow m_O=6-\left(3,6+0,8\right)=1,6g\Rightarrow n_O=0,1mol\)
Gọi CTHH cần tìm là \(C_xH_yO_z\)
\(\Rightarrow x:y:z=0,3:0,8:0,1=3:8:1\)
\(C_3H_8O+\dfrac{9}{2}O_2\underrightarrow{t^o}3CO_2+4H_2O\)
Đúng 0
Bình luận (0)
giúp m câu này nhaBài 1: Từ quạng pirit sắt, nước biển và ko khí. Viết phương trình điều chế FeCl2, Fecl3, FeSO4, Fe(OH)2, Na2SO3, NaHSO4Bài 2 : Phân đạm hai lá có CTHH là NH4NO3 và phân đamj urê có CTHH là (NH2)2CO. Viết các PTPƯ điều chế 2 phân đạm ns trên từ ko khí nước và đá vôiBài 3: Từ hỗn hợp chất rắnCu(OH).MgO.FeS. Viết các PTPUW điều chế CuBài 4: a, Hãy kể tên các loại sắt quan trọng trong tự nhiên.Trong các loaijn quăng đó có 2 quạng ko phải quặng oxit, nung nóng hai quăng này thu được...
Đọc tiếp
giúp m câu này nha
Bài 1: Từ quạng pirit sắt, nước biển và ko khí. Viết phương trình điều chế FeCl2, Fecl3, FeSO4, Fe(OH)2, Na2SO3, NaHSO4
Bài 2 : Phân đạm hai lá có CTHH là NH4NO3 và phân đamj urê có CTHH là (NH2)2CO. Viết các PTPƯ điều chế 2 phân đạm ns trên từ ko khí nước và đá vôi
Bài 3: Từ hỗn hợp chất rắn
Cu(OH).MgO.FeS. Viết các PTPUW điều chế Cu
Bài 4: a, Hãy kể tên các loại sắt quan trọng trong tự nhiên.Trong các loaijn quăng đó có 2 quạng ko phải quặng oxit, nung nóng hai quăng này thu được hai chất khí A và B. Viết các PT điều chế, nêu các cách nhận biết A và B ( phương pháp hóa học)
b, Từ một quặng bất kì trên hãy viết các PTPUW điều chế Fe(OH)2 và Fe(OH)3
điều chế FeCl2
2NaCl + 2H2O=> 2NaOH + H2 + Cl2
H2 + Cl2 => 2HCl
FeS2 + 2HCl=> FeCl2 + H2S+S
điều chế FeCl3
2FeCl2 + Cl2 => 2FeCl3
điều chế FeSO4
4FeS2 + 11O2=>2Fe2O3 + 8So2
2SO2 + O2 => 2SO3
SO3 + H2O=> H2SO4
FeS2 + H2SO4 => FeSO4 + H2S + S
điều chế Fe(OH)2
FeSO4+ 2NaOH=> Na2SO4 + Fe(OH)2
điều chế Na2SO3
2NaOH + SO2 => Na2SO3 + H2O
điều chế NaHSO4
2NaOH + H2SO4=> Na2SO4 + 2H2O
Đúng 0
Bình luận (0)
Từ cc chất ban đầu là đá vôi CaCO3 , nước hãy trình bày phương pháp để điều chế hai oxit và hai đơn chất khí khác nhau từ các chất trên
-Nung CaCO3 :
CaCO3 -to-> CaO + CO2
+ Hai oxit : CaO ( oxit bazơ), CO2 (oxit axit)
- Điện phân H2O :
2H2O -đp-> 2H2 + O2
+Hai đơn chất khí là: H2 và O2
Chúc bạn học tốt <3
Đúng 0
Bình luận (0)
Nung nóng đá vôi và nước
CaCO3 => CaO + CO2
H2O => H2 + 1/2 O2
Nung đá vôi ta được hai oxit: Canxi oxit và cacbon đioxit
Còn nung nóng nước đến nhiệt độ cao thu được hai đơn chất khí là H2 và O2
Đúng 0
Bình luận (0)
Từ các hóa chất : KClO3, FeS và dd HCl, với các thiết bị và các chất xúc tác có đủ . Hãy viết các phương trình để điều chế 4 chất khí khác nhau
\(2KClO_3 \xrightarrow{t^o} 2KCl +3O_2\\ KClO_3 +6 HCl \to KCl + 3Cl_2 + 3H_2O\\ FeS + 2HCl \to FeCl_2 + H_2S\\ 4FeS + 7O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4SO_2\)
Đúng 2
Bình luận (0)
1.Viết phương trình hóa học điều chế các chất sau từ NaCl: NaClO; CaOCl2
2. Trình bày phương pháp hóa học phân biệt hai dung dịch: NaF và NaCl.
GIÚP MÌNH VỚI MÌNH ĐANG CẦN GẤP
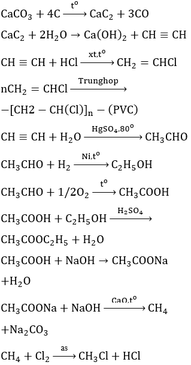
Từ đá vôi, than đá, các chất vô cơ cần thiết khác và các điều kiện khác có đủ. Viết phương trình phản ứng hóa học (ghi rõ điều kiện phản ứng nếu có) để điều chế: etylaxetat, poli vinylclorua, metyl clorua.
Có những chất sau: Sắt, lưu huỳnh, axit sunfuric loãng.
Hãy trình bày hai phương pháp điều chế hidro sunfua từ những chất đã cho.
Hai phương pháp điều chế H2S từ những chất trên
Fe + S → FeS(1)
FeS + H2SO4 → FeSO4 + H2S (2)
Fe + H2SO4 → FeSO4 + H2 (3)
H2 + S → H2S (4)
Đúng 0
Bình luận (0)
có những chất sau : sắt , lưu huỳnh , axit sunfuric loãng : a) hãy trình bày phương pháp điều chế hidro sunfua từ các chất trên ; b) viết các phương trình hóa học của phản ứng và cho biết vai trò của lưu huỳnh trong phản ứng .
PT:
Fe + S-->FeS (to)
FeS + H2SO4-->H2S + FeSO4
Vai trò:chất oxi hóa
Đúng 0
Bình luận (0)