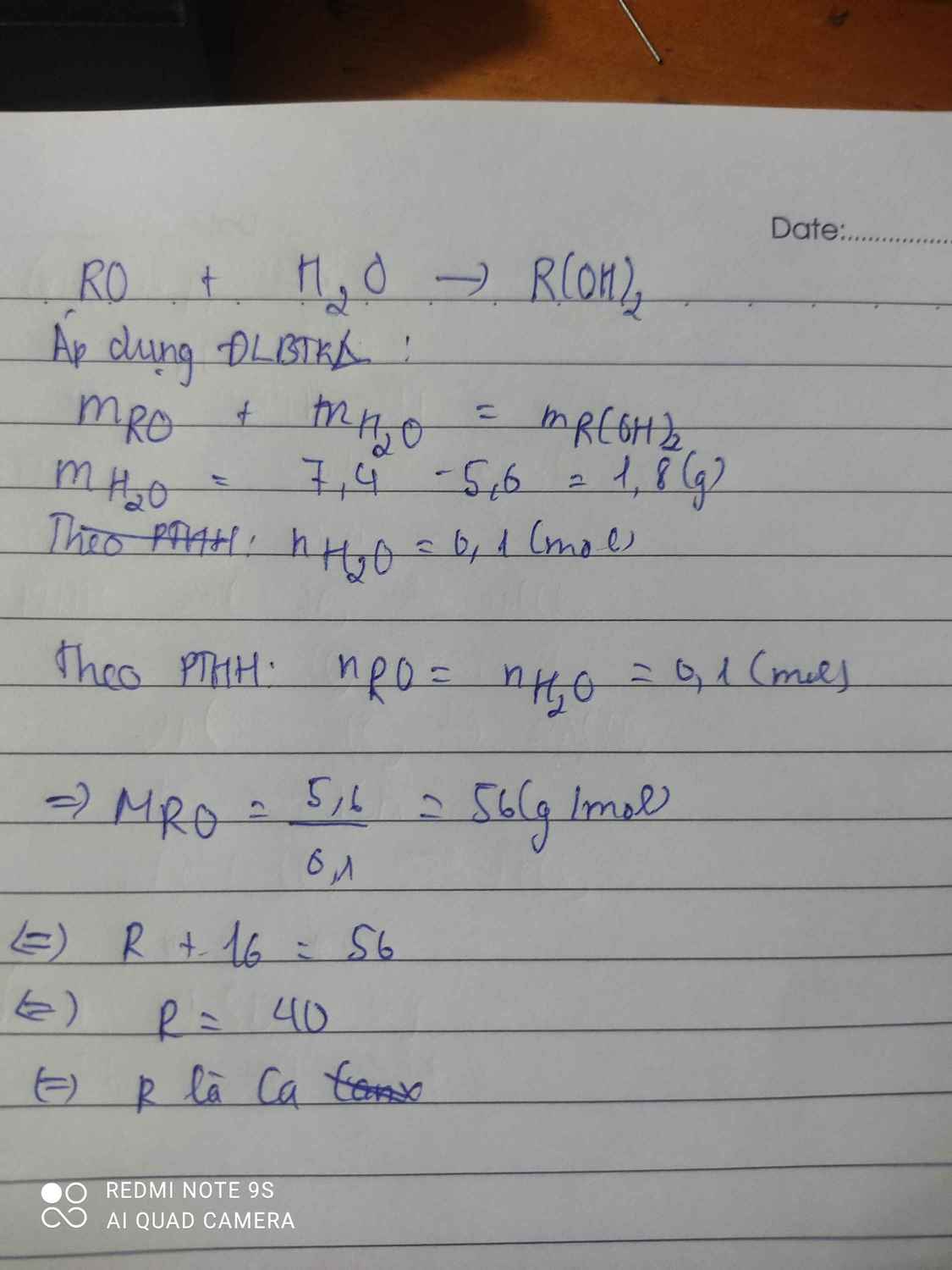Phân biệt các oxit khi hòa tan vào nước.

Những câu hỏi liên quan
a) Khi hòa tan muối ăn vào nước:
1, hãy phân biệt dung môi và dung dịch ?
2, để hòa tan được nhiều muối hơn vào cốc nước đó thì ta cần làm gì ?
GIÚP MÌNH VỚI
1,dung môi là nước dung dịch là nước muối
2,ko bt
Đúng 0
Bình luận (0)
1. Khi hòa tan muối ăn vào nước, nếu muối không tan hết bị lắng đọng xuống đáy có gọi là huyền phù không? Giải thích.
2. Phân biệt huyền phù và nhũ tương.
Đốt cháy 5,85 gam kali trong không khí, giả thiết chỉ thu đc kali oxit có khối lượng 6,58g. Tính hiệu xuất của phản ứng và nồng độ mol dung dịch khi đen hòa tan lượng oxit trên vào 200ml nước
\(n_{K_2O}=\dfrac{6,58}{94}=0,07\left(mol\right);n_K=\dfrac{5,85}{39}=0,15\left(mol\right)\)
PTHH: \(4K+O_2\xrightarrow[]{t^o}2K_2O\)
0,14<--------0,07
\(\Rightarrow H=\dfrac{0,14}{0,15}.100\%=93,33\%\)
PTHH: \(K_2O+H_2O\rightarrow2KOH\)
0,07------------->0,14
\(\Rightarrow C_{M\left(KOH\right)}=\dfrac{0,14}{0,2}=0,7M\)
Đúng 1
Bình luận (0)
a, Hòa tan 15,5g natri oxit vào 184,5g nước được dung dịch A
1: tính nồng độ % của dung dịch A
2: Lấy 120g dụng dịch A tác dụng với 150g dung dịch CuCl2 9%. Tính nồng độ % củ các các chất trong dung dịch sau khi tách bỏ kết tủa
Hòa tan hoàn toàn 12,4g oxit kim loại R hóa trị 1 vào nước dư, thu được 16g bazo. Timf oxit kim loại R ?
Hòa tan 3,1 g oxit kim loại hóa trị I vào nước được dung dịch chứa 4g kiềm. Xác định CTPT oxit kim lọa trên
Giả sử oxit kim loại cần tìm là A2O.
PT: \(A_2O+H_2O\rightarrow2AOH\)
Ta có: \(n_{A_2O}=\dfrac{3,1}{2M_A+16}\left(mol\right)\)
\(n_{AOH}=\dfrac{4}{M_A+17}\left(mol\right)\)
Theo PT: \(n_{AOH}=2n_{A_2O}\Rightarrow\dfrac{4}{M_A+17}=\dfrac{3,1.2}{2M_A+16}\)
\(\Rightarrow M_A=23\left(g/mol\right)\)
⇒ A là Na.
Vậy: Oxit đó là Na2O.
Bạn tham khảo nhé!
Đúng 2
Bình luận (1)
đốt cháy kim loại R trong khi oxi dư , được 3,1 gam oxit hòa tan hoàn toàn oxit của R vào nước thì thu được 4gam đioxit của R
a, xác định tên nguyên tố R , đọc tên oxit hiđroxit của R b, tính thể tích của oxi đã phản ứng ( ở đktc)a, Giả sử R có hóa trị n.
PT: \(R_2O_n+nH_2O\rightarrow2R\left(OH\right)_n\)
Theo ĐLBT KL, có: m oxit + mH2O = m hydroxit
⇒ 3,1 + 18nH2O = 4 ⇒ nH2O = 0,05 (mol)
Theo PT: \(n_{R_2O_n}=\dfrac{1}{n}n_{H_2O}=\dfrac{0,05}{n}\left(mol\right)\)
\(\Rightarrow M_{R_2O_n}=\dfrac{3,1}{\dfrac{0,05}{n}}=62n\) \(\Rightarrow2M_R+16n=62n\Rightarrow M_R=23n\)
Với n = 1 thì MR = 23 (g/mol)
→ R là Natri. Na2O: natri oxit. NaOH: natri hydroxit.
b, PT: \(4Na+O_2\underrightarrow{t^o}2Na_2O\)
Ta có: \(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Na_2O}=0,025\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,025.22,4=0,56\left(l\right)\)
Đúng 3
Bình luận (0)
Hòa tan 5,6g oxit kim loại hóa trị (II) vào nước thu được 7,4g bazơ.Tìm kim loại
Gọi oxit kim loại cần tìm là RO
\(n_{RO}=\dfrac{5,6}{M_R+16}\left(mol\right)\)
PTHH: RO + H2O --> R(OH)2
\(\dfrac{5,6}{M_R+16}\)---------->\(\dfrac{5,6}{M_R+16}\)
=> \(M_{R\left(OH\right)_2}=M_R+34=\dfrac{7,4}{\dfrac{5,6}{M_R+16}}=\dfrac{37}{28}\left(M_R+16\right)\left(g/mol\right)\)
=> MR = 40 (g/mol)
=> Kim loại là Ca
Đúng 3
Bình luận (0)
\(Đặt.oxit:AO\\ AO+H_2O\rightarrow A\left(OH\right)_2\\Ta.có:m_{H_2O}=m_{bazo}-m_{oxit}=7,4-5,6=1,8\left(g\right)\\ n_{H_2O}=n_{AO}=\dfrac{1,8}{18}=0,1\left(mol\right)\\ \Rightarrow M_{AO}=\dfrac{5,6}{0,1}=56\left(\dfrac{g}{mol}\right)=M_A+16\\ \Leftrightarrow M_A=40\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Canxi\left(Ca=40\right)\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung...
Đọc tiếp
1. Hoà tan 6,2 g natri oxit vào 193,8 g nước thì được dung dịch A. Tính nồng độ phần trăm của dung dịch A.
2. Hoà tan 23,5 g kali oxit vào nước được 0,5 lít dung dịch A. Tính nồng độ mol của dung dịch A.
3. Hòa tan hết 12,4 gam natrioxit vào nước thu được 500ml dung dịch A . Tính nồng độ mol của dung dịch A.
4. Hòa tan 12,6 gam natri sunfit vào dung dịch axit clohidric dư. Thể tích khí SO2 thu được ở đktc.
5. Hòa tan hết 5,6 gam CaO vào dung dịch HCl 14,6% . Tính khối lượng dung dịch HCl đã dùng.
Cho em xin cách giải chi tiết ạ em cảm ơn :DD
1)
$n_{Na_2O} = \dfrac{6,2}{62} = 0,1(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,2(mol)$
$m_{dd} = 6,2 + 193,8 = 200(gam) \Rightarrow C\%_{NaOH} = \dfrac{0,2.40}{200}.100\% = 4\%$
2)
$n_{K_2O} = \dfrac{23,5}{94} = 0,25(mol)$
$K_2O + H_2O \to 2KOH$
$n_{KOH} = 2n_{K_2O} = 0,5(mol) \Rightarrow C_{M_{KOH}} = \dfrac{0,5}{0,5} = 1M$
3) $n_{Na_2O} = \dfrac{12,4}{62} = 0,2(mol)$
$Na_2O + H_2O \to 2NaOH$
$n_{NaOH} = 2n_{Na_2O} = 0,4(mol)$
$C_{M_{NaOH}} = \dfrac{0,4}{0,5} =0,8M$
Đúng 3
Bình luận (1)
4)
$Na_2SO_3 + 2HCl \to 2NaCl +S O_2 + H_2O$
Theo PTHH :
$n_{SO_2} = n_{Na_2SO_3} = \dfrac{12,6}{126} = 0,1(mol)$
$V_{SO_2} = 0,1.22,4 = 2,24(lít)$
5) $n_{CaO} = \dfrac{5,6}{56} = 0,1(mol)$
$CaO + 2HCl \to CaCl_2 + H_2O$
Theo PTHH :
$n_{HCl} = 2n_{CaO} = 0,2(mol) \Rightarrow m_{dd\ HCl} = \dfrac{0,2.36,5}{14,6\%} = 50(gam)$
Đúng 3
Bình luận (1)
Bài 1 :
\(n_{Na2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
Pt : \(Na_2O+H_2O\rightarrow2NaOH|\)
1 1 2
0,1 0,2
\(n_{NaOH}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
⇒ \(m_{NaOH}=0,2.40=8\left(g\right)\)
\(m_{ddspu}=6,2+193,8=200\left(g\right)\)
\(C_{ddNaOH}=\dfrac{8.100}{200}=4\)0/0
Chúc bạn học tốt
Đúng 2
Bình luận (1)
Xem thêm câu trả lời