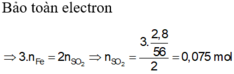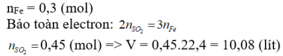Cho 5.6g Fe tác dụng hết với dung dịch H2SO4 đặc nóng dư sinh ra V SO2 ở đktc . Tính V SO2

Những câu hỏi liên quan
Hòa tan m gam Fe trong dung dịch H2SO4 loãng thì sinh ra 3,36 lít khí (đktc). Nếu cho m gam Fe tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít khí SO2 (đktc). Giá trị của V là A. 10,08. B. 5,04. C. 3,36. C. 3,36.
Đọc tiếp
Hòa tan m gam Fe trong dung dịch H2SO4 loãng thì sinh ra 3,36 lít khí (đktc). Nếu cho m gam Fe tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít khí SO2 (đktc). Giá trị của V là
A. 10,08.
B. 5,04.
C. 3,36.
C. 3,36.
Đáp án B
Xét giai đoạn m gam Fe tác dụng với dung dịch H2SO4 loãng:
Sơ đồ phản ứng :
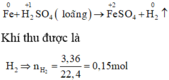
Các quá trình nhường, nhận electron :
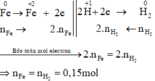
Xét giai đoạn m gam Fe tác dụng với H2SO4 đặc, nóng , dư:
Sơ đồ phản ứng:
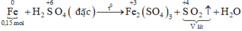
Các quá trình nhường, nhận electron:
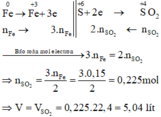
Đúng 0
Bình luận (0)
Cho 12,8 gam hỗn hợp X gồm Fe và FeO vào dung dịch H2SO4 loãng dư thấy có 2,24 lít H2 thoát ra.a-Tính số mol Fe và FeO.Biết khí đo ở đktc .(1đ)b-Cho toàn bộ lượng hỗn hợp X trên tác dụng với H2SO4 đặc nóng dư thu được V lít khí SO2 ở đktc .Tính V
\(n_{Fe}=a\left(mol\right),n_{FeO}=b\left(mol\right)\)
\(m_X=56a+72b=12.8\left(g\right)\)
\(n_{H_2}=n_{Fe}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(\Rightarrow a=0.1\)
\(b=\dfrac{12.8-56\cdot0.1}{72}=0.1\left(mol\right)\)
\(BTe:\)
\(3n_{Fe}+n_{FeO}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=\dfrac{3\cdot0.1+0.1}{2}=0.2\left(mol\right)\)
\(V_{SO_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(\)
Đúng 0
Bình luận (0)
Cho 2,8 gam Fe kim loại tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng dư, thu được dung dịch X và V lít SO2 ở đktc (sản phẩm khử duy nhất của S+6). Giá trị của V là: A. 2,24 B. 1,008 C. 1,12 D. 1,68
Đọc tiếp
Cho 2,8 gam Fe kim loại tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng dư, thu được dung dịch X và V lít SO2 ở đktc (sản phẩm khử duy nhất của S+6). Giá trị của V là:
A. 2,24
B. 1,008
C. 1,12
D. 1,68
Cho 16,8 gam Fe tác dụng với dung dịch H2SO4 đặc, nóng, thể tích khí SO2 thoát ra ở đktc là:
A.6,72 lít
B. 10,08 lít
C. 2,24 lít
D. 3,36 lít
Cho 36 gam hỗn hợp
F
e
,
F
e
O
,
F
e
3
O
4
tác dụng hoàn toàn với dung dịch
H
2
S
O
4
đặc, nóng dư thấy thoát ra 5,6 lít khí
S
O
2
ở đktc (sản phẩm khử duy nhất).Tính số mol
H
2
S
O
4
đã phản ứng.
Đọc tiếp
Cho 36 gam hỗn hợp F e , F e O , F e 3 O 4 tác dụng hoàn toàn với dung dịch H 2 S O 4 đặc, nóng dư thấy thoát ra 5,6 lít khí S O 2 ở đktc (sản phẩm khử duy nhất).Tính số mol H 2 S O 4 đã phản ứng.
cho 16,8 gam Fe tác dụng vừa đủ với dung dịch H2SO4 đặc nóng, thu được dung dịch A và V lít khí SO2(đktc) A) Tính V B) Cho dung dịch A tác dụng hoàn toàn với dung dịch NaOH thu được m gam kết tủa. Tính m
a, \(n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
BT e, có: 3nFe = 2nSO2 ⇒ nSO2 = 0,45 (mol)
⇒ VSO2 = 0,45.22,4 = 10,08 (l)
b, BTNT Fe, có: nFe(OH)3 = nFe = 0,3 (mol)
⇒ mFe(OH)3 = 0,3.107 = 32,1 (g)
Đúng 1
Bình luận (0)
Đốt 5,6g Fe bằng O2, thu được 7,2g hỗn hợp X gồm 4 chất. Cho X tác dụng với dung dịch H2SO4 đặc nóng, dư thu được Fe2(SO4)3 và V lít khí SO2 (đktc). Tính V.
Thanks in advance
BT O: \(n_O=\dfrac{7,2-5,6}{16}=0,1\left(mol\right)\)
=> \(n_X=n_O=0,1\left(mol\right)\)
\(Fe^o\rightarrow Fe^{3+}+3e\)
0,1 0,3
\(S^{+6}+2e\rightarrow S^{+4}\)
0,3 0,15
BT e: \(n_{SO_2}=\dfrac{0,3}{2}=0,15\Rightarrow V_{SO_2}=3,36\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 13,22 gam hỗn hợp Fe và Zn vào dung dịch HCl dư thu được 4,928 lít khí ở ĐKTC a) Tìm khối lượng của Zn b) Lấy 1/2 hỗn hợp trên tác dụng với H2SO4 đặc nóng dư thu được V ( lít ) SO2 sản phẩm khử duy nhất. Tìm V
\(n_{Fe}=a\left(mol\right),n_{Zn}=b\left(mol\right)\)
\(m=56a+65b=13.22\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{4.928}{22.4}=0.22\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(n_{H_2}=a+b=0.22\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=0.12\)
\(b=0.1\)
\(\text{Bảo toàn e : }\)
\(n_{Zn}+n_{Fe}=n_{SO_2}=\dfrac{0.12}{2}+\dfrac{0.1}{2}=0.11\left(mol\right)\)
\(V_{SO_2}=0.11\cdot22.4=2.464\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 10,38 gam hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lit khi (đktc).Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lit khí SO2 (đktc).a. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.b. Tính số mol axit tham gia phản ứng ở mỗi phần.
Đọc tiếp
Cho 10,38 gam hỗn hợp gồm Fe, Al và Ag chia làm 2 phần bằng nhau:
Phần 1: Tác dụng với dung dịch H2SO4 loãng dư thu được 2,352 lit khi (đktc).
Phần 2: Tác dụng với dung dịch H2SO4 đặc, nóng dư thu được 2,912 lit khí SO2 (đktc).
a. Tính khối lượng từng kim loại trong hỗn hợp ban đầu.
b. Tính số mol axit tham gia phản ứng ở mỗi phần.
a)
Gọi số mol Fe, Al, Ag trong mỗi phần là a, b,c (mol)
=> 56a + 27b + 108c = 5,19 (1)
Phần 1:
\(n_{H_2}=\dfrac{2,352}{22,4}=0,105\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----->a------------------>a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b------>1,5b------------------->1,5b
=> a + 1,5b = 0,105 (2)
Phần 2:
\(n_{SO_2}=\dfrac{2,912}{22,4}=0,13\left(mol\right)\)
PTHH: 2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
b----->3b-------------------->1,5b
2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------>3a--------------------->1,5a
2Ag + 2H2SO4 --> Ag2SO4 + SO2 + 2H2O
c-------->c------------------>0,5c
=> 1,5a + 1,5b + 0,5c = 0,13 (3)
(1)(2)(3) => a = 0,03 (mol); b = 0,05 (mol); c = 0,02 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=2.0,03.56=3,36\left(g\right)\\m_{Al}=2.0,05.27=2,7\left(g\right)\\m_{Ag}=2.0,02.108=4,32\left(g\right)\end{matrix}\right.\)
b)
- Phần 1:
\(n_{H_2SO_4}=a+1,5b=0,105\left(mol\right)\)
- Phần 2:
\(n_{H_2SO_4}=3a+3b+c=0,26\left(mol\right)\)
Đúng 3
Bình luận (0)