Nếu 1.00 lít nước hòa tan 350 lít khí hidro bromua (đktc) thì nồng độ phần trăm của dd axit bromhidric thu được là

Những câu hỏi liên quan
Ở điều kiện tiêu chuẩn, 1 lít nước hòa tan 350 lít khí HBr. Tính nồng độ phần trăm của dung dịch axit bromhiđric thu được.
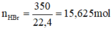
→ mHBr = 15,625 x 81 = 1265,625g;
VH2O = 1 lít ⇒ mH2O = 1000g.
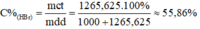
Đúng 0
Bình luận (0)
ở điều kiện tiêu chuẩn , 1 lít nước hòa tan 350 lít khí HBr . Tính nồng độ phần trăm của dung dịch axit bromhiđric thu được .
nHBr =\(\frac{350}{22,4}\) = 15,625 mol
→ mHBr = 15,625 x 81 =1265,625 g
C%HBr =\(\frac{1265,625.100}{1000+1265,625}\) = 55,86%
Đúng 0
Bình luận (0)
Ở điều kiện tiêu chuẩn, 1 lít nước hòa tan 350 lít khí HBr. Tính nồng độ phần trăm của dung dịch axit bromhidric thu được.
Hướng dẫn giải:
nHBr = = 15,625 mol
→ mHBr = 15,625 x 81 =1265,625 g
C%HBr = = 55,86%
Đúng 0
Bình luận (0)
hòa tan 16,8 lít khí H2S ở đktc vào 174,5 gam nước thì thu được dung dịch Axit H2S. tính nồng độ phần trăm của dung dịch?
\(n_{H_2S}=\dfrac{16,8}{22,4}=0,75\left(mol\right)\\\rightarrow m_{H_2S}=0,75.34=25,5\left(g\right)\\ m_{dd}=25,5+174,5=200\left(g\right)\\ \rightarrow C\%_{H_2S}=\dfrac{25,5}{200}.100\%=12,75\%\)
Đúng 1
Bình luận (0)
Ở điều kiện tiêu chuẩn, 1 lít nước hòa tan 350 lít khí HBr. Tính nồng độ phần trăm của dung dịch axit bromhidric thu được.
nHBr = 350 / 22,4 = 15,625 mol.
mHBr = 15,625 x 81 = 1265,625g.
C%HBr = 1265,625 x 100% / (1000 + 1265,625) \(\approx\) 55,86%.
Đúng 0
Bình luận (0)
Ở điều kiện tiêu chuẩn, 1 lít nước hoà tan được 492,8 lít khí HCl. Nồng độ phần trăm của dd axit clohidric thu đc là?
Cho 44.8 lít khí Hcl ở đktc hòa tan toàn vào 2gam nước thì thu được dd A
a/ Tính nồng độ phần trăm của dd A
b/ cho 50gam CaCO3 vào 250gam vào dd A đem đun nhẹ đến phản ứng xảy ra hoàn toàn thì thu đc dd B .Tính nồng độ phần trăm của các chất trong dd B
Hòa tan 6g hỗn hợp gồm Mg và MgO vào dd HCL 7.3% sau pứng thu được 2.20 lít khí H2 đktc và dd A
A tính thành phần phần trăm theo khối lượng nước của mỗi chất có trong hỗn hợp
B Tính nồng độ phần trăm dd HCL cần dùng
Hòa tan 10g hỗn hợp kim loại gồm fe và cu trong 200g dd axit sunfuric loãng.Sau phản ứng thu được 2,8 lít khí (đktc)
1) Viết PTHH
2) Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
3) Tính nồng độ phần trăm của axit tham gia phản ứng
Xem chi tiết
\(n_k=n_{H_2}=0,125\left(mol\right)\)
a,b, \(PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
.............0,125...0,125....................0,125...
\(\Rightarrow m_{Fe}=7\left(g\right)\)
Do Cu không phản ứng với H2SO4 .
\(\Rightarrow m_{Cu}=m_{hh}-m_{Fe}=10-7=3\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%Fe=70\%\\\%Cu=30\%\end{matrix}\right.\)
c, Có : \(m_{dd}=m_{Fe}+m_{ddH_2SO_4}-m_{H_2}=206,75\left(g\right)\)
\(\Rightarrow C\%=\dfrac{m_{H_2SO_4}}{m_{dd}}.100\%\approx5,925\%\)
Đúng 4
Bình luận (1)
Nhiệt phân hoàn toàn 27,3 gam hỗn hợp NaNO3 và Cu(NO3)2. Hỗn hợp khí thoát ra dẫn được vào 89,2 ml nước thì còn dư 1,12 lít khí ở đktc không bị hấp thụ (lượng O2 hòa tan không đáng kể). Nồng độ phần trăm của dung dịch axit thu được là (biết
D
H
2
O
1
g
/
ml
) A. 14,13% B. 18,90% C. 12,60% D. 9,45%
Đọc tiếp
Nhiệt phân hoàn toàn 27,3 gam hỗn hợp NaNO3 và Cu(NO3)2. Hỗn hợp khí thoát ra dẫn được vào 89,2 ml nước thì còn dư 1,12 lít khí ở đktc không bị hấp thụ (lượng O2 hòa tan không đáng kể). Nồng độ phần trăm của dung dịch axit thu được là (biết D H 2 O = 1 g / ml )
A. 14,13%
B. 18,90%
C. 12,60%
D. 9,45%



















