hợp chất Y có khối lượng phân tử là 160 amu , trong đó thanhd phần trăm khối lượng của Iron là 70%, còn lại là oxygen. Xác định công thức hoa học Y . ( Biết khối lượng nguyên tử của Iron là 56 amu, oxygen là 16 amu)
Em hãy tạo chương trình Scratch để giải quyết bài toán sau đây:
R là hợp chất S (sulfur) và O (oxygen), khối lượng phân tử của R là 64 amu. Biết khối lượng nguyên tử của S là 32 amu, khối lượng nguyên tử của O là 16 amu, phần trăm khối lượng của O trong R là 50%. Hãy xác định số lượng nguyên tử trong hợp chất.
Để giải bài toán này, ta cần sử dụng các công thức sau:
- Khối lượng mol của hợp chất R = khối lượng phân tử của R = 64 g/mol
- Khối lượng mol của O trong hợp chất R = (50/100) x 64 = 32 g/mol
- Khối lượng mol của O trong hợp chất R = 64 - 32 = 32 g/mol
- Số lượng nguyên tử của S trong hợp chất R = 32/32 = 1 nguyên tử
- Số lượng nguyên tử của O trong hợp chất R = 32/16 = 2 nguyên tử
Với Scratch, em có thể tạo chương trình như sau:
1. Khởi tạo biến
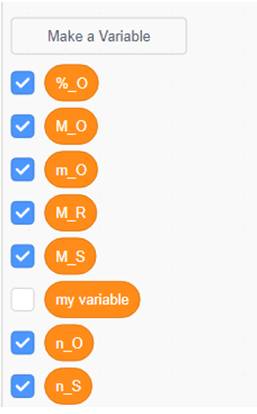
2. Thiết lâp chương trình như sau và hiển thị kết quả như sau:
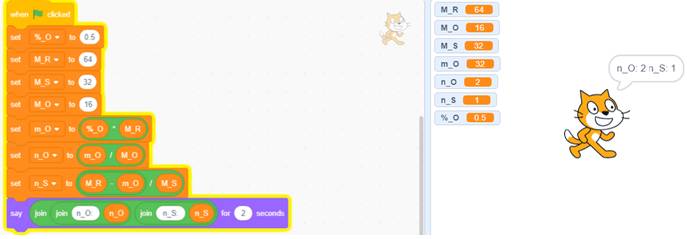
Đúng 1
Bình luận (0)
Khối lượng nguyên tử của oxygen bằng 16 amu. Phân tử khí oxygen gồm 2 nguyên tử oxygen sẽ có khối lượng phân tử bằng bao nhiêu?
Khối lượng phân tử oxygen (O2) bằng: 16 × 2 = 32 amu.
Đúng 0
Bình luận (0)
Biết 4 nguyên tử X nặng bằng 1 nguyên tử Iron a)Tính khối lượng của nguyên tử X theo đơn vị amu và đơn vị gam? b)Xác định tên,kí hiệu hóa học của nguyên tử X?
`#3107.101107`
a)
Khối lượng nguyên tử X là:
`56 \div 4 = 14` (amu)
b)
Tên của X: Nitrogen
KHHH của X: N.
Đúng 1
Bình luận (0)
Nguyên tử X có tổng số hạt là 48 . Số hạt mang điện gấp 2 lần số hạt không mang điện . Khối lượng nguyên tử của X tính theo đơn vị amu là ?
Ta có: P + N + E = 48
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 48 (1)
Theo đề, số hạt mang điện gấp 2 lần số hạt không mang điện.
⇒ 2P = 2N (2)
Từ (1) và (2) ⇒ P = E = N = 16
⇒ MX = 16 + 16 = 32 (amu)
Đúng 2
Bình luận (0)
nguyên tử X có tổng số hạt là 48 . Số hạt mang điện gấp 2 lần số hạt không mang điện . Khối lượng nguyên tử của X tính theo đơn vị amu
-) P+E+N=48 (1)
-) P+E=2N (2)
Từ (1) và (2) ta có:
P+E+N=2N+N=3N=48
⇒ N= 48:3=16
⇒ P+E=48-16=32
⇒ P=E=32:2=16
Vậy P=E=N=16
⇒ Khối lượng của nguyên tử X là:
16+16=32 (amu)
Đúng 0
Bình luận (0)
Hợp chất (X) tạo bởi 2 nguyên tố potassium K và oxygen O có khối lượng phân tử bằng 94 amu, trong đó potassium K chiếm 82,98% về khối lượng. Công thức hóa học của hợp chất (X) là?
Đọc tiếp
Hợp chất (X) tạo bởi 2 nguyên tố potassium K và oxygen O có khối lượng phân tử bằng 94 amu, trong đó potassium K chiếm 82,98% về khối lượng. Công thức hóa học của hợp chất (X) là?
Gọi ct chung: \(\text{K}_{\text{x}}\text{O}_{\text{y}}\)
\(\text{% O = }100\%-82,98\%=17,02\%\)
\(\text{PTK = }39\cdot\text{x}+16\cdot\text{y}=94< \text{amu}>\)
\(\text{%K = }\dfrac{39\cdot x\cdot100}{94}=82,98\%\)
`-> 39*x*100=82,98*94`
`-> 39*x*100=7800,12`
`-> 39x=7800,12 \div 100`
`-> 39x=78,0012`
`-> x=78,0012 \div 39`
`-> x=2,00...` làm tròn lên là `2`
Vậy, có `2` nguyên tử \(\text{K}\) trong phân tử \(\text{K}_{\text{x}}\text{O}_{\text{y}}.\)
\(\text{ %O}=\dfrac{16\cdot y\cdot100}{94}=17,02\%\)
`-> y=0,99...` làm tròn lên là `1`
Vậy, có `1` nguyên tử \(\text{O}\) trong phân tử \(\text{K}_{\text{x}}\text{O}_{\text{y}}.\)
`=>`\(\text{CTHH: K}_2\text{O.}\)
Đúng 0
Bình luận (0)
1. Hợp chất A do 2 nguyên tố Carbon và Hydrogen tạo nên, trong đó Carbon chiếm 85,71% theo khối lượng . Xách định công thức hóa học của A biết khối lượng phân tử của A là 28 amu. 2. Hợp chất X được tạo bởi nguyên tố Sodium , Sulfur và Oxygen trong đó phần trăm về khối lượng . Xác định công thức hóa học của X biết khối lượng phân tử của X là 126 amu.
Đọc tiếp
1. Hợp chất A do 2 nguyên tố Carbon và Hydrogen tạo nên, trong đó Carbon chiếm 85,71% theo khối lượng . Xách định công thức hóa học của A biết khối lượng phân tử của A là 28 amu.
2. Hợp chất X được tạo bởi nguyên tố Sodium , Sulfur và Oxygen trong đó phần trăm về khối lượng . Xác định công thức hóa học của X biết khối lượng phân tử của X là 126 amu.![]()
1. Gọi ct chung: \(C_xH_y.\)
\(K.L.P.T=12.x+1.y=28< amu>.\)
\(\%H=100\%-85,71\%=14,29\%\)
\(\%C=\dfrac{12.x.100}{28}=85,71\%\)
\(C=12.x.100=85,71.28\)
\(C=12.x.100=2399,88\)
\(12.x=2399,88\div100\)
\(12.x=23,9988\)
\(x=23,9988\div12=1,9999\) làm tròn lên là 2.
vậy, có 2 nguyên tử C trong phân tử \(C_xH_y.\)
\(\%H=\dfrac{1.y.100}{28}=14,29\%\)
\(\Rightarrow y=4,0012\) làm tròn lên là 4 (cách làm tương tự nhé).
vậy, cthh của A: \(C_2H_4.\)
2. Mình chưa hiểu đề của bạn cho lắm? Trong đó % khối lượng mình k có thấy số liệu á.
Đúng 2
Bình luận (4)
1,
Gọi công thức cần tìm là CxHy
Khối lượng phân tử là 28(amu)
%Khối lượng nguyên tử H là:
100%-85,71%=14,29%
\(\%C=\dfrac{12.x}{28}.100=85,71\%\)
=>x=2
\(\%H=\dfrac{1.y}{28}.100=14,2\%\)
=>y=4
Vậy công thức hóa học cần tìm là C2H4
2,Chắc là sai đề r ý
Đúng 0
Bình luận (0)
Điện tích của hạt nhân nguyên tử fluorine là +1,4418.10-18 culong. Hãy xác định khối lượng nguyên tử fluorine theo đơn vị amu, biết rằng số neutron có trong nguyên tử này là 10.
Ta biết.
Điện tích của hạt nhân nguyên tử fluorine là +1,4418.10-18 culong.
Vậy Số proton của nguyên tử fluorine là bao nhiêu
Đọc tiếp
Điện tích của hạt nhân nguyên tử fluorine là +1,4418.10-18 culong. Hãy xác định khối lượng nguyên tử fluorine theo đơn vị amu, biết rằng số neutron có trong nguyên tử này là 10.
Ta biết.
Điện tích của hạt nhân nguyên tử fluorine là +1,4418.10-18 culong.
Vậy Số proton của nguyên tử fluorine là bao nhiêu
Nguyên tử oxygen -16 có 8 proton, 8 neutron và 8 electron. Tính khối lượng nguyên tử oxygen theo đơn vị gam và amu.
Khối lượng p = 1,673.10-24 gam = 1 amu
Khối lượng n = 1,675.10-24 gam = 1 amu
Khối lượng e = 9,11.10-28 gam = 0,00055 amu
- Khối lượng nguyên tử oxygen theo đơn vị gam:
8 x 1,673.10-24 + 8 x 1,675.10-24 + 8 x 9,11.10-28 = 2,679.10-23 gam
- Khối lượng nguyên tử oxygen theo đơn vị amu:
8 x 1 + 8 x 1 + 8 x 0,00055 = 16,0044 amu
Đúng 1
Bình luận (0)
mO= mproton + mneutron = 8+8=16 (amu)
Đúng 0
Bình luận (0)




















