cho dung dịch chứa 10 gam CH3COOH tác dụng với dung dịch chứa 10g KOH sau khi phản ứng hoàn toàn dung dịch chứa các chất tan là

Những câu hỏi liên quan
Cho hỗn hợp gồm valin và axit glutamic (có tỉ lệ mol tương ứng là 2:1) tác dụng với 198 ml dung dịch KOH 2M (dùng dư 10% so với lượng phản ứng). Sau khi các phản ứng xảy ra hoàn toàn, thuy được dung dịch X chứa m gam chất tan. Giá trị của m là A. 61,416 B. 49,986 C. 61,024 D. 49,708
Đọc tiếp
Cho hỗn hợp gồm valin và axit glutamic (có tỉ lệ mol tương ứng là 2:1) tác dụng với 198 ml dung dịch KOH 2M (dùng dư 10% so với lượng phản ứng). Sau khi các phản ứng xảy ra hoàn toàn, thuy được dung dịch X chứa m gam chất tan. Giá trị của m là
A. 61,416
B. 49,986
C. 61,024
D. 49,708
Đáp án B
Phương pháp:
- Đặt ẩn số mol valin và axit glutamic. Dựa trên dữ kiện tỉ lệ mol và số mol KOH ta lập được hệ hai phương trình 2 ẩn. Giải hệ thu được số mol mỗi chất.
BTKL: m chất tan = m hỗn hợp + m KOH - m H 2 O
Hướng dẫn giải: Do lấy KOH dư 10% so với lượng phản ứng nên ta có:

Đúng 0
Bình luận (0)
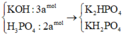
Cho a mol P2O5 vào dung dịch chứa 3a mol KOH. Sau khi phản ứng xảy ra hoàn toàn, dung dịch thu được chứa các chất tan là: A. K3PO4 và KOH. B. H3PO4 và KH2PO4. C. K3PO4 và K2HPO4. D. K2HPO4 và KH2PO4.
Đọc tiếp
Cho a mol P2O5 vào dung dịch chứa 3a mol KOH. Sau khi phản ứng xảy ra hoàn toàn, dung dịch thu được chứa các chất tan là:
A. K3PO4 và KOH.
B. H3PO4 và KH2PO4.
C. K3PO4 và K2HPO4.
D. K2HPO4 và KH2PO4.
Cho m gam axit glutamic vào dung dịch chứa NaOH 0,5M và KOH 0,8M, thu được dung dịchX chứa 14,43 gam chất tan. X phản ứng vừa đủ với dung dịch Y chứa H2SO4 0,6M và HCl 0,8M, thu được dung dịch Z chứa 23,23 gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 10,29. B. 11,76. C. 8,82. D. 7,35.
Đọc tiếp
Cho m gam axit glutamic vào dung dịch chứa NaOH 0,5M và KOH 0,8M, thu được dung dịchX chứa 14,43 gam chất tan. X phản ứng vừa đủ với dung dịch Y chứa H2SO4 0,6M và HCl 0,8M, thu được dung dịch Z chứa 23,23 gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 10,29.
B. 11,76.
C. 8,82.
D. 7,35.
Đáp án A
Gọi x là số mol của NaOH, suy ra số mol KOH là 1,6x. Gọi số mol axit glutamic là y. → 147 y + 40 x + 56 . 1 , 6 x - 2 , 6 x . 18 = 14 , 43
Cho X tác dụng với H2SO4 0,6M và HCl 0,8M thì
n H + = y + 2 , 6 x → V Y = 2 , 6 x + y 0 , 6 . 2 + 0 , 8 = 1 , 3 x + 0 , 5 y → n H 2 S O 4 = 0 , 78 x + 0 , 3 y ; n H C l = 1 , 04 x + 0 , 4 y
Ta có: 147y+40x+56x.1,6+98(0,78x+0,3y)+36,5(1,04x+0,4y)-18.2,6x=23,23
Giải hệ: x = 0,05; y = 0,07
→ m = 10 , 29 g a m
Đúng 0
Bình luận (0)
Đề bài: Cho m gam hỗn hợp X gồm Fe3O4 và Cu tác dụng với lượng dư dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và 1,6 gam kim loại không tan. Dung dịch Y tác dụng vừa đủ với 500ml dung dịch chứa NaOH 1M và KOH 1M thu được 36,8 gam kết tủa. Tính số mol HCl ban đầu và giá trị của m.
Cảm ơn !
Đề bài: Cho m gam hỗn hợp X gồm Fe3O4 và Cu tác dụng với lượng dư dung dịch HCl. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y và 1,6 gam kim loại không tan. Dung dịch Y tác dụng vừa đủ với 500ml dung dịch chứa NaOH 1M và KOH 1M thu được 36,8 gam kết tủa. Tính số mol HCl ban đầu và giá trị của m.
Cảm ơn !
Đặt số mol Fe3O4 là x (mol)
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
x..............8x..........2x............x
Cu + 2FeCl3 ⟶ 2FeCl2 + CuCl2
x.........2x................2x.............x
Kim loại không tan là Cu
Dung dịch Y gồm FeCl2, CuCl2 và HCl dư
=> \(n_{FeCl_2}=x+2x=3x\left(mol\right);n_{CuCl_2}=x\left(mol\right)\)
\(n_{OH^-}=0,5.1+0,5.1=1\left(mol\right)\)
\(H^+_{\left(dư\right)}+OH^-\rightarrow H_2O\)
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
3x..........6x...............3x
\(Cu^{2+}+2OH^-\rightarrow Cu\left(OH\right)_2\)
x.............2x.................x
Kết tủa là Cu(OH)2 và Fe(OH)2
Ta có : \(3x.90+x.98=36,8\)
=> x=0,1 (mol)
=> \(m_{Cu}=x.64+1,6=8\left(g\right)\)
=> \(m=0,1.232+8=31,2\left(g\right)\)
Mặt khác : \(n_{HCl\left(dư\right)}=1-\left(6x+2x\right)=0,2\left(mol\right)\)
=> \(n_{HCl\left(bđ\right)}=8x+0,2=1\left(mol\right)\)
Đúng 1
Bình luận (0)
Cho m gam axit glutamic vào dung dịch chứa NaOH 0,5M và KOH 0,8M, thu được dung dịch X chứa 14,43 gam chất tan. X phản ứng vừa đủ với dung dịch Y chứa H2SO4 0,6M và HCl 0,8M, thu được dung dịch Z chứa 23,23 gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là: A. 7,35 B. 8,82 C. 10,29 D. 11,76
Đọc tiếp
Cho m gam axit glutamic vào dung dịch chứa NaOH 0,5M và KOH 0,8M, thu được dung dịch X chứa 14,43 gam chất tan. X phản ứng vừa đủ với dung dịch Y chứa H2SO4 0,6M và HCl 0,8M, thu được dung dịch Z chứa 23,23 gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 7,35
B. 8,82
C. 10,29
D. 11,76
Cho 11,25 gam C2H5NH2 tác dụng với 200 ml dung dịch HCl a(M). Sau khi phản ứng hoàn toàn thu được dung dịch (X) có chứa 22,2 gam chất tan. Giá trị của a là
A. 1,36M
B. 1,5M
C. 1,25M
D. 1,3M
Đáp án B
Ta có phản ứng: C2H5NH2 + HCl → C2H5NH3Cl
Bảo toàn khối lượng → mHCl = 22,2 - 11,25 = 10,95 gam
⇒ nHCl =0,3 mol ⇒ a = 0,3/0,2 = 1,5M
Đúng 0
Bình luận (0)
Cho 11,25 gam C2H5NH2 tác dụng với 200 ml dung dịch HCl a(M). Sau khi phản ứng hoàn toàn thu được dung dịch (X) có chứa 22,2 gam chất tan. Giá trị của a là:
A. 1,36M.
B. 1,5M.
C. 1,25M.
D. 1,3M.
Cho m gam P2O5 tác dụng với 500ml dung dịch KOH 1M, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X (không chứa H3PO4). Cô cạn dung dịch X thu được dfrac{193m}{71}gam chất rắn khan.a) Tính giá trị mb)Cho X tác dụng với lượng dư dung dịch BaCl2. Tinh khối lượng kết tủa thu được sau khi kết thúc các phản ứng.
Đọc tiếp
Cho m gam P2O5 tác dụng với 500ml dung dịch KOH 1M, sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X (không chứa H3PO4). Cô cạn dung dịch X thu được \(\dfrac{193m}{71}\)gam chất rắn khan.
a) Tính giá trị m
b)Cho X tác dụng với lượng dư dung dịch BaCl2. Tinh khối lượng kết tủa thu được sau khi kết thúc các phản ứng.
a)
X gồm :
$PO_4^{3-} : a(mol)$
$HPO_4^{2-} : b(mol)$
$K^+ : 0,5(mol)$
Bảo toàn điện tích : $3a + 2b = 0,5$
Khối lượng rắn khan : $95a + 96b + 0,5.39 = \dfrac{193}{71}m$
Bảo toàn P : $142.0,5(a + b) = m$
Suy ra : a = 0,1 ; b = 0,1 ; m = 14,2
b)
$n_{BaHPO_4} = b = 0,1(mol)$
$n_{Ba_3(PO_4)_2} = 0,5a = 0,05(mol)$
$m_{Kết\ tủa} = 0,1.233 + 0,05.601 = 53,35(gam)$
Đúng 3
Bình luận (0)