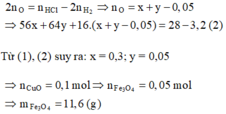Cho kim loại R hoá trị không đổi vào 100ml dung dịch HCl 1,5M thu được 2,24 lít H2 (đktc) và dung dịch X. Tính khối lượng kết tủa thu được khi cho dung dịch AgNO3 dư vào dung dịch X. (Đ/S: 27,325g)
Cho a gam kim loại R tan hoàn toàn trong 200 ml dung dịch HCl 0,5M, thu được dung dịch X và 2,24 lít H2 (đktc). Cho dung dịch AgNO3 dư vào X, thu được m gam kết tủa. Giá trị của m là
A. 25,95.
B. 14,35.
C. 32,84.
D. 28,70.
Giải thích:
nHCl = 0,2.0,5 = 0,1 (mol); nH2 = 2,24 :22,4 = 0,1 (mol)
=> nHCl < 2nH2
=> R là kim loại kiềm hoặc kiềm thổ, phản ứng hết với HCl sau đó phản ứng được với H2O
2R + 2nHCl → RCln + nH2↑
0,1 → 0,05
2R + 2nH2O → 2R(OH)n + nH2↑
0,1/n ←0,05
RCln + nAgNO3 → nAgCl↓ + R(NO3)n
2R(OH)n + 2nAgNO3 → nAg2O↓ + R(NO3)n + nH2O
0,1/n → 0,05
=> m↓ = mAgCl + mAg2O = 0,1.143,5 + 0,05. 232 = 25,95(g)
Chú ý:
Tránh sai lầm khi chỉ tính khối lượng kết tủa là AgCl khi đó sẽ ra 14,35 g => chọn ngay đáp án B sẽ dẫn đến sai lầm
Đáp án A
Kim loại R hóa trị không đổi vào 100 ml dd HCl 1,5M được 2,24 lít H2 (đktc) và dd X. Tính khối lượng kết tủa thu được khi cho dd AgNO3 dư vào dd X.
A. 21,525 g
B. 26,925 g
C. 24,225 g
D. 27,325g
Lấy 4 g kim loại R hoá trị II đem hoà tan trong dung dịch HCl vừa đủ thì nhận được 2,24 lít H2 (đktc) và dung dịch X. Cho dung dịch Na2CO3 dư vào dung dịch X thì nhận được m (g) kết tủa. Vậy m có giá trị là
A. 8,12.
B. 10,0.
C. 11,12.
D. 12,0.
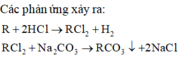
Như vậy từ kim loại ban đầu là R ta có sản phẩm muối cuối cùng là kết tủa RCO3.
Cứ 1 mol R sau các phản ứng tạo 1 mol RCO3 thì khối lượng tăng lên 60 gam.
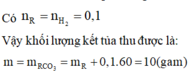
Đáp án B
Cho 15,25 g hỗn hợp 1 kim loại hóa trị II và Fe tan hết trong dung dịch HCl dư, thoát ra 4,48 dm3 khí H2 ở đktc và thu được dung dịch X. Thêm dung dịch NaOH dư vào X thu được kết tủa, lọc kết tủa rồi nung đến khối lượng không đổi cân nặng 12g
a) Viết các PTHH xảy ra
b) Tìm kim loại hóa trị II biết nó không tạo kết tủa với Hiđroxit
gọi kim loại hóa trị II là Mpt pứ:M+2HCl−−−>MgCl2+H2Fe+2HCl−−−>FeCl2+H2dd X: MgCl2,FeCl2,HCldưThêm NaOH dư vào X và biết nó không tạo kết tủa với hidroxit nên ta có pt pứFeCL2+2NaOH−−−>Fe(0H)2+2NaCl4Fe(OH)2+02−−−>2Fe203+4H20n Fe203 = 0, 075 moltừ các pt pu --->n H2= n Fe= n FeCl
Hòa tan hoàn toàn m gam kim loại R trong dung dịch HCl dư thu được dd X và 2,24 lít H2(đktc). Cô cạn dd X thu được 19,9 gam muối B duy nhất. Nếu cho dd X tác dụng với dung dịch KOH dư lọc kết tủa nung ngoài không khí đến khối lượng không đổi thu được (m+2,4) gam chất rắn D. Hòa tan D trong dd H2SO4 loãng, vừa đủ thu được dung dịch E. Cô cạn E thu được 28,2 gam muối G duy nhất. Xác định công thức R,B, G
Giúp mình với, cảm ơn các bạn
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
- Nếu B là muối khan
PTHH: 2R + 2nHCl --> 2RCln + nH2
\(\dfrac{0,2}{n}\) <----- \(\dfrac{0,2}{n}\)<--0,1
- Nếu B là muối khan
=> \(M_{RCl_n}=\dfrac{19,9}{\dfrac{0,2}{n}}=99,5n\left(g/mol\right)\)
=> MR = 64n (g/mol)
Với mọi n --> Không có TH thỏa mãn => Loại
=> B là muối ngậm nước
\(n_{RCl_n.xH_2O}=\dfrac{0,2}{n}\left(mol\right)\)
=> \(M_R+35,5n+18x=99,5n\)
=> MR = 64n - 18x (1)
Chất rắn D là oxit của R
Giả sử D có CTHH: R2Oy
Bảo toàn R: \(n_{R_2O_y}=\dfrac{0,1}{n}\left(mol\right)\)
=> \(m_{R_2O_y}=\dfrac{0,1}{n}\left(2.M_R+16y\right)\)
=> \(\dfrac{0,1}{n}\left(2.M_R+16y\right)=m+2,4=\dfrac{0,2}{n}.M_R+2,4\)
=> \(\dfrac{1,6y}{n}=2,4\)
=> \(\dfrac{y}{n}=\dfrac{3}{2}\) => Chọn y = 3; n = 2
(1) => MR = 128 - 18x (g/mol)
Chỉ có x = 4 thỏa mãn => MR = 56 (g/mol)
=> R là Fe
B là FeCl2.4H2O
\(n_{Fe_2O_3}=\dfrac{m+2,4}{160}=\dfrac{5,6+2,4}{160}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0,05----------------->0,05
G có dạng Fe2(SO4)3.qH2O
=> \(n_{Fe_2\left(SO_4\right)_3.qH_2O}=0,05\left(mol\right)\)
=> \(M_{Fe_2\left(SO_4\right)_3.qH_2O}=\dfrac{28,2}{0,05}=564\left(g/mol\right)\)
=> q = 9,11 (L)
=> Không tìm đc G, bn check đề nhé :)
à mình bị sai 1 chỗ là khối lượng của G là 28,1 gam, cảm ơn bạn
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2R + 2xHCl ---> 2RClx + xH2
\(\dfrac{0,2}{x}\) 0,2 \(\dfrac{0,2}{x}\) 0,1
Áp dụng ĐLBTKL:
\(m_R+m_{HCl}=m_{RCl_x}+m_{H_2}\\ \rightarrow m_R=19,9+0,1.2-0,2.36,5=12,8\left(g\right)\)
\(\rightarrow M_R=\dfrac{12,8}{\dfrac{0,2}{x}}=64x\left(\dfrac{g}{mol}\right)\)
Xét x = 1 thoả mãn => R là Cu
Bạn ơi sai đề à Cu ko pư vs HCl :)?
Cho 28 gam hỗn hợp X gồm Fe, Fe3O4, CuO vào dung dịch HCl, thu được 3,2 gam một
kim loại không tan, dung dịch Y chỉ chứa muối và 1,12 lít khí H2 (đktc). Cho Y vào dung
dịch AgNO3 dư, thu được 132,85 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Khối lượng
Fe3O4 trong X là
A. 5,8 gam.
B. 14,5 gam.
C. 17,4 gam.
D. 11,6 gam.
Đáp án D
Kim loại không tan là Cu (0,05 mol) nên Y chứa FeCl2 (u) và CuCl2 (v)

Cho 28 gam hỗn hợp X gồm Fe; Fe3O4; CuO vào dung dịch HCl, thu được 3,2 gam một kim loại không tan, dung dịch Y chỉ chứa muối và 1,12 lít H2 (đktc). Cho Y vào dung dịch AgNO3 dư, thu được 132,85 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Fe3O4 trong X là:
A. 5,8 gam.
B. 14,5 gam.
C. 17,4 gam.
D. 11,6 gam.
Cho 28 gam hỗn hợp X gồm Fe, Fe3O4, CuO vào dung dịch HCl, thu được 3,2 gam một kim loại không tan, dung dịch Y chỉ chứa muối và 1,12 lít khí H2 (đktc). Cho Y vào dung dịch AgNO3 dư, thu được 132,85 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Fe3O4 trong X là
A. 5,8 gam.
B. 14,5 gam.
C. 17,4 gam.
D. 11,6 gam.
Đáp án D
Kim loại không tan là Cu (0,05 mol) nên Y chứa FeCl2 (u) và CuCl2 (v)
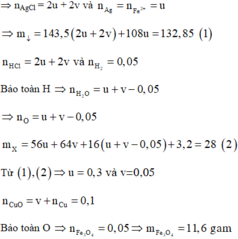
Cho 28 gam hỗn hợp X gồm Fe, Fe3O4, CuO vào dung dịch HCl, thu được 3,2 gam một kim loại không tan, dung dịch Y chỉ chứa muối và 1,12 lít khí H2 (đktc). Cho Y vào dung dịch AgNO3 dư, thu được 132,85 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Khối lượng Fe3O4 trong X là
A. 17,4 gam
B. 5,8 gam
C. 11,6 gam
D. 14,5 gam
Đáp án C
Dung dịch Y chứa Fe2+ (x mol), Cu2+ (y mol), Cl- (2x + 2y mol).
Kết tủa gồm Ag (x mol) và AgCl (2x + 2y mol) => 395x + 287y = 132,85 (1)
Ta có: