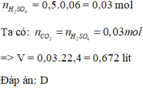Cho 200 gam dung dịch CH3COOH 9% tác dụng vừa đủ với Na2CO3. Thể tích khí CO2 sinh ra ở đktc là bao nhiêu? (ĐS: 3,36l)

Những câu hỏi liên quan
Cho 3,28 gam hỗn hợp 3 muối
K
2
CO
3
,
Na
2
CO
3
và
MgCO
3
tác dụng vừa đủ với 60 ml dung dịch
H
2
SO
4
0,5M. Thể tích...
Đọc tiếp
Cho 3,28 gam hỗn hợp 3 muối K 2 CO 3 , Na 2 CO 3 và MgCO 3 tác dụng vừa đủ với 60 ml dung dịch H 2 SO 4 0,5M. Thể tích khí CO 2 sinh ra ở đktc là
A. 0,224 lít
B. 0,448 lít
C. 0,336 lít
D. 0,672 lít
cho 200 gam dung dịch CH3COOH 12% tác dụng với dung dịch Na2CO3 50% a viết phương trình phản ứng xảy ra b tính khối lượng dung dịch Na2CO3 phản ứng c tính thể tích khí thoát ra ở đktc
a) 2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
b) \(n_{CH_3COOH}=\dfrac{200.12\%}{60}=0,4\left(mol\right)\)
PTHH: 2CH3COOH + Na2CO3 --> 2CH3COONa + CO2 + H2O
0,4------->0,2------------------------->0,2
=> \(m_{Na_2CO_3}=0,2.106=21,2\left(g\right)\)
=> \(m_{dd.Na_2CO_3}=\dfrac{21,2.100}{50}=42,4\left(g\right)\)
c) \(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 3
Bình luận (0)
Bài 4: Cho 500 ml dung dịch CH3COOH tác dụng vừa đủ với một dung dịch có hòa tan 8,4g KOH.a/ Tính nồng độ mol của dung dịch CH3COOH ?b/ Nếu cho toàn bộ dung dịch CH3COOH ở trên vào 200 ml dung dịch Na2CO3 0,5 M thì thu được bao nhiêu lít khí CO2 thoát ra ở đktc ?
Đọc tiếp
Bài 4: Cho 500 ml dung dịch CH3COOH tác dụng vừa đủ với một dung dịch có hòa tan 8,4g KOH.
a/ Tính nồng độ mol của dung dịch CH3COOH ?
b/ Nếu cho toàn bộ dung dịch CH3COOH ở trên vào 200 ml dung dịch Na2CO3 0,5 M thì thu được bao nhiêu lít khí CO2 thoát ra ở đktc ?
a, \(n_{KOH}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PT: \(CH_3COOH+KOH\rightarrow CH_3COOK+H_2O\)
Theo PT: \(n_{CH_3COOH}=n_{KOH}=0,15\left(mol\right)\Rightarrow C_{M_{CH_3COOH}}=\dfrac{0,15}{0,5}=0,3\left(M\right)\)
b, \(n_{Na_2CO_3}=0,2.0,5=0,1\left(mol\right)\)
PT: \(2CH_3COOH+Na_2CO_3\rightarrow2CH_3COONa+CO_2+H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{2}< \dfrac{0,1}{1}\), ta được Na2CO3 dư.
Theo PT: \(n_{CO_2}=\dfrac{1}{2}n_{CH_3COOH}=0,075\left(mol\right)\Rightarrow V_{CO_2}=0,075.22,4=1,68\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 4,41 gam hỗn hợp 3 muối:
K
2
CO
3
,
Na
2
CO
3
và
BaCO
3
tác dụng vừa đủ với dung dịch HCl. Cô cạn dung dịch sau phản ứng thu được 4,74 gam muối khan. Thể tích khí
CO
2...
Đọc tiếp
Cho 4,41 gam hỗn hợp 3 muối: K 2 CO 3 , Na 2 CO 3 và BaCO 3 tác dụng vừa đủ với dung dịch HCl. Cô cạn dung dịch sau phản ứng thu được 4,74 gam muối khan. Thể tích khí CO 2 sinh ra là:
A. 0,224 lít
B. 0,448 lít
C. 0,672 lít
D. 0,448 lít
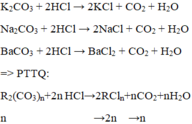
Ta thấy chênh lệch khối lượng hai muối là
n R C l n − n R 2 ( C O 3 ) n = 2. n .35,5 − 60 n = 11 n
Với n là số mol của muối ban đầu
Áp dụng công thức tính nhanh:
n C O 2 = m R C l n − m R 2 ( C O 3 ) n 11 = 4 , 74 − 4 , 41 11 = 0 , 03 m o l
=> V = 0,03.22,4 = 0,672 lít
Đáp án: C
Đúng 0
Bình luận (0)
Câu 18: Cho 146 gam dung dịch HCl 50 % tác dụng vừa đủ với dung dịch Na2CO3 . Tìm thể tích khí sinh ra ở ĐKC (H1, S32 ,O16 ,Na23, C 12) A. 44,8 lB. 4,48 lC. 22,4 lD. 2,24 l Câu 19: Cho 500 ml dung dịch NaOH 9 M tác dụng vừa đủ với dung dịch FeCl3. Tìm khối lượng kết tủa thu được sau phản ứng (Fe56 ,O16 ,H1, Cl35,5. Na23) A. 1,605 gB. 16,05 gC. 160,50 gD. 96,3 g Câu 20: Nhiệt phân hoàn toàn 174g Mg(OH)2. Tìm khối lượng chất rắn thu được sau phản ứng (Mg24 ,O16, H1): A. 120 gB. 12 gC. 6 gD. 7...
Đọc tiếp
Câu 18: Cho 146 gam dung dịch HCl 50 % tác dụng vừa đủ với dung dịch Na2CO3 . Tìm thể tích khí sinh ra ở ĐKC (H=1, S=32 ,O=16 ,Na=23, C =12)
A. 44,8 l
B. 4,48 l
C. 22,4 l
D. 2,24 l
Câu 19: Cho 500 ml dung dịch NaOH 9 M tác dụng vừa đủ với dung dịch FeCl3. Tìm khối lượng kết tủa thu được sau phản ứng (Fe=56 ,O=16 ,H=1, Cl=35,5. Na=23)
A. 1,605 g
B. 16,05 g
C. 160,50 g
D. 96,3 g
Câu 20: Nhiệt phân hoàn toàn 174g Mg(OH)2. Tìm khối lượng chất rắn thu được sau phản ứng (Mg=24 ,O=16, H=1):
A. 120 g
B. 12 g
C. 6 g
D. 72 g
\(n_{HCl}=\dfrac{146.50}{100.36,5}=2\left(mol\right)\)
PTHH: Na2CO3 + 2HCl --> 2NaCl + CO2 + H2O
_______________2----------------->1
=> VCO2 = 1.22,4 = 22,4 (l)
=> C
Đúng 1
Bình luận (0)
Cho 25ml dung dịch CH3COOH tác dụng vừa đủ với kim loại Mg, sau phản ứng thu được 7,1 gam muối khan.
a) Tính thể tích khí H2 sinh ra ở đktc.
b) Tính nồng độ mol của dung dịch CH3COOH đã dùng
a) \(n_{\left(CH_3COO\right)_2Mg}=\dfrac{7,1}{142}=0,05\left(mol\right)\)
PTHH: 2CH3COOH + Mg --> (CH3COO)2Mg + H2
0,1<----------------------0,05------->0,05
=> VH2 = 0,05.22,4 = 1,12 (l)
b) \(C_{M\left(dd.CH_3COOH\right)}=\dfrac{0,1}{0,025}=4M\)
Đúng 2
Bình luận (0)
cho 100 gam dung dịch axit axetic tác dụng vừa đủ với kim loại magie. cô cạn dung dịch sau phản ứng người ta thu được 7,1 gam muối khan a. tính thể tích khí được sinh ra ở đktc ?b. tính C% của dung dịch axit CH3COOH đã dùngc. cho toàn bộ lượng axit trên tác dụng với 6,9 gam rượu etylic có H2SO4 đặc làm xúc tác và đun nóng .tính khối lượng este thu được ? biết hiệu suất của phản ứng este hóa là 80%
Đọc tiếp
cho 100 gam dung dịch axit axetic tác dụng vừa đủ với kim loại magie. cô cạn dung dịch sau phản ứng người ta thu được 7,1 gam muối khan
a. tính thể tích khí được sinh ra ở đktc ?
b. tính C% của dung dịch axit CH3COOH đã dùng
c. cho toàn bộ lượng axit trên tác dụng với 6,9 gam rượu etylic có H2SO4 đặc làm xúc tác và đun nóng .tính khối lượng este thu được ? biết hiệu suất của phản ứng este hóa là 80%
\(a,n_{\left(CH_3COO\right)_2Mg}=\dfrac{7,1}{142}=0,05\left(mol\right)\)
PTHH: \(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\uparrow\)
0,1<----------------0,05-------------->0,05
\(\rightarrow V_{H_2}=0,05.22,4=1,12\left(l\right)\\ b,C\%_{CH_3COOH}=\dfrac{0,1.60}{100}.100\%=6\%\)
\(c,n_{C_2H_5OH}=\dfrac{6,9}{46}=0,15\left(mol\right)\)
PTHH: \(CH_3COOH+C_2H_5OH\xrightarrow[H_2SO_{4\left(đặc\right)}]{t^o}CH_3COOC_2H_5+H_2O\)
bđ 0,1 0,15
pư 0,1 0,1
spư 0 0,05 0,1
\(\rightarrow m_{este}=0,1.80\%.88=7,04\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 2,44 gam hỗn hợp muối
Na
2
CO
3
và
K
2
CO
3
tác dụng vừa đủ với dung dịch
H
2
SO
4
0,5M, sau phản ứng thu được 0,448 lít
CO
2...
Đọc tiếp
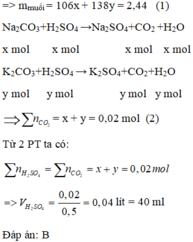
Cho 2,44 gam hỗn hợp muối Na 2 CO 3 và K 2 CO 3 tác dụng vừa đủ với dung dịch H 2 SO 4 0,5M, sau phản ứng thu được 0,448 lít CO 2 ở đktc. Thể tích dung dịch H 2 SO 4 0,5M cần dùng là:
A. 100 ml
B. 40 ml
C. 30 ml
D. 25 ml
![]()
Đặt x, y lần lượt là số mol của Na 2 CO 3 và K 2 CO 3 (x, y > 0)
Đúng 0
Bình luận (0)
Cho 5,6 g kim loại sắt tác dụng vừa đủ với dung dịch CH3COOH 10% A) tính khối lượng dung dịch CH3COOH đã dùng và thể tích khí thoát ra ở đktc B) tính c% của dung dịch sau phản ứng
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Fe+H_2\)
a, Theo PT: \(n_{CH_3COOH}=2n_{Fe}=0,2\left(mol\right)\Rightarrow m_{CH_3COOH}=0,2.60=12\left(g\right)\)
\(\Rightarrow m_{ddCH_3COOH}=\dfrac{12}{10\%}=120\left(g\right)\)
\(n_{H_2}=n_{Fe}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, Theo PT: \(n_{\left(CH_3COO\right)_2Fe}=n_{Fe}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 5,6 + 120 - 0,1.2 = 125,4 (g)
\(\Rightarrow C\%_{\left(CH_3COO\right)_2Fe}=\dfrac{0,1.174}{125,4}.100\%\approx13,88\%\)
Đúng 3
Bình luận (0)