Cho a gam kim loại phản ứng với HCl dư. Thể tính khí hiđrô lớn nhất khi dùng kim loại:
a. Fe b. Pb c. Mg d. Al
Cho a gam kim loại phản ứng với axit HCl lấy dư,thể tích khí H2 thu được lớn nhất khi kim loại là zn ca mg fe
Kim loại R có hóa trị 2
$R + 2HCl \to RCl_2 + H_2$
Theo PTHH :
$n_{H_2} = n_R = \dfrac{a}{R}(mol)$
Ta thấy $R$ càng nhỏ thì $\dfrac{a}{R}$ càng lớn
mà : $M_{Mg} = 24< M_{Ca} = 40 < M_{Fe} = 56 < M_{Zn} = 65$
Do đó : dùng kim loại $Mg$ thu được thể tích $H_2$ lớn nhất
cho a(g) kim loại phản ứng với dung dịch HCl lấy dư thể tích H2 thu được lớn nhất khi kim loại là
A. Zn B. Al C. Mg D. Fe
PTHH: Zn + 2HCl -> ZnCl2 + H2 (1)
2Al + 6HCl -> 2AlCl3 + 3H2 (2)
Mg + 2HCl -> MgCl2 + H2 (3)
Fe + 2HCl -> FeCl2 + H2
Gọi a(g) là khối lượng kim loại tham gia phản ứng trong mỗi phương trình.
Theo các PTHH và đề bài, ta có:
\(n_{Zn\left(1\right)}=\frac{a}{65}\left(mol\right)\\ =>n_{H_2\left(1\right)}=n_{Zn\left(1\right)}=\frac{a}{65}\left(mol\right)->\left(a\right)\)
\(n_{Al\left(2\right)}=\frac{a}{27}\left(mol\right)\\=> n_{H_2\left(2\right)}=\frac{3.\frac{a}{27}}{2}=\frac{a}{18}\left(mol\right)->\left(b\right)\)
\(n_{Mg\left(3\right)}=\frac{a}{24}\left(mol\right)\\ =>n_{H_2\left(3\right)}=n_{Mg\left(3\right)}=\frac{a}{24}\left(mol\right)->\left(c\right)\)
\(n_{Fe\left(4\right)}=\frac{a}{56}\left(mol\right)\\ =>n_{H_2\left(4\right)}=n_{Fe\left(4\right)}=\frac{a}{56}\left(mol\right)->\left(d\right)\)
Từ (a), (b), (c), (d) => \(n_{H_2\left(2\right)}\) là lớn nhất
=> \(V_{H_2\left(đktc\right)\left(2\right)}\) lớn nhất.
Vậy: Ta chọn kim loại Al.
=> Đáp án đúng: B.Al.
Cho a gam kim loại phản ứng với axit hcl lấy dư thể tích H2 thu được lớn nhất khi kim loại là Zn ca mg fe
Ta có: \(n_{Zn}=\dfrac{a}{65}\left(mol\right)\)
\(n_{Ca}=\dfrac{a}{40}\left(mol\right)\)
\(n_{Mg}=\dfrac{a}{24}\left(mol\right)\)
\(n_{Fe}=\dfrac{a}{56}\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(Ca+2HCl\rightarrow CaCl_2+H_2\) (2)
\(Mg+2HCl\rightarrow MgCl_2+H_2\) (3)
\(Fe+2HCl\rightarrow FeCl_2+H_2\) (4)
Theo PT: \(n_{H_2\left(1\right)}=n_{Zn}=\dfrac{a}{65}\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Ca}=\dfrac{a}{40}\left(mol\right)\)
\(n_{H_2\left(3\right)}=n_{Mg}=\dfrac{a}{24}\left(mol\right)\)
\(n_{H_2\left(4\right)}=n_{Fe}=\dfrac{a}{56}\left(mol\right)\)
⇒ nH2 (3) lớn nhất → KL pư với HCl dư thu VH2 lớn nhất là Mg.
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít khí H2 đktc. Kim loại M là kim loại nào sau đây?
A. Fe.
B. Al.
C. Ca.
D. Mg.
Đáp án B.
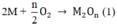
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
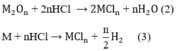
Số mol H2: 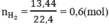
Theo phương trình (1)
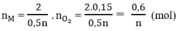
Theo phương trình (3)
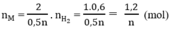
Tổng số mol M là 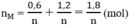
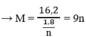
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Câu 1: Hòa tan hết 16,8 gam kim loại A hóa trị II trong dung dịch hydrochloric acid HCl, sau phản ứng thu được 7,437 lít khí H2 ở đktc. Kim loại A là
A. Fe B. Mg C. Cu D. Zn
Câu 2: Cho 5,6 g sắt tác dụng với hydrochloric acid dư, sau phản ứng thể tích khí H2 thu được (ở đktc):
A. 1,24 lít. B. 2,479 lít. C. 12,4 lít. D. 24,79 lít.
Câu 3: Cho các chất sau: H2SO4, HCl, NaCl, CuSO4, NaOH, Mg(OH)2. Số chất thuộc loại axit là:
A. 1 B. 2 C. 3 D. 4
Câu 4: Hoà tan hết 3,6 g một kim loại hoá trị II bằng dung dịch H2SO4 loãng được 3,719 lít H2 (đktc). Kim loại là:
A. Zn. B. Mg. C. Fe. D. Ca.
( Lưu ý : giải ra rồi mới chọn đáp án )
\(1.\\ n_A=\dfrac{16,8}{A}mol\\ n_{H_2}=\dfrac{7,437}{24,79}=0,3mol\\ A+2HCl\rightarrow ACl_2+H_2\\ \Rightarrow\dfrac{16,8}{A}=0,3\\ \Rightarrow A=56g/mol\\ \Rightarrow A.là.Fe\\ \Rightarrow Chọn.A\\ 2.\\ n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{Fe}=n_{H_2}=0,1mol\\ V_{H_2}=0,1.24,79=2,479l\\ \Rightarrow Chọn.B\\ 3.\\ Axit:H_2SO_4;HCl\\ \Rightarrow Chọn.B\\ 4.\\ 3,719l\Rightarrow3,7185\\ CTHH:R\\ n_R=\dfrac{3,6}{R}mol\\ n_{H_2}=\dfrac{3,7185}{24,79}=0,15mol\\ R+2HCl\rightarrow RCl_2+H_2\\ \Rightarrow\dfrac{3,6}{R}=0,15\\ \Rightarrow R=24g/mol,Mg\\ \Rightarrow Chọn.B\)
Dãy kim loại tác dụng được với HCl : ... . A. Mg, Al, Pb, Cu .... B. Fe, Pb, Na , Ag ... C. Mg, Al, Fe, Zn ... D. Al, Mg, Cu, Zn
cho 1,66 gam hỗn hợp gồm 2 kim loại Fe và Al tác dụng với dd HCL dư, sau phản ứng thu được 11,2 lít khí (dktc)
a, viết PTHH
b,tính khối lượng của kim loại trong hỗn hợp ban đầu
a) Fe +2 HCl -> FeCl2 + H2
x____2x______x____x(mol)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
y____3y______y________1,5y(mol)
b) nH2= 0,05(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}56x+27y=1,66\\x+1,5y=0,05\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
=> mFe=0,02.56= 1,12(g)
mAl=0,02.27=0,54(g)
cho 6 g hỗn hợp 2 kim loại Fe, Cu phản ứng với dung dịch HCL dư khi phản ứng kết thúc thu được 3,2g 1 kim loại
a, Kim loại nào tham gia phản ứng và phản ứng bao nhiêu gam
b, viết phương trình hóa học và tính thể tích khí H2, thu được đkC
Giúp mình với ạ!
a) Fe tham gia phản ứng, $m_{Fe} = 6 - 3,2 =2,8(gam)$
b) $Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = n_{Fe} = \dfrac{2,8}{56} = 0,05(mol)$
$V_{H_2} = 0,05.24,79 = 1,2395(lít)$
PTHH: \(Al+NaOH+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\uparrow\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\) (2)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (3)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\) (4)
a) Ta có: \(n_{H_2\left(1\right)}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\) \(\Rightarrow n_{Al}=0,2mol\)
\(\Rightarrow n_{H_2\left(2\right)}=0,3mol\) \(\Rightarrow n_{H_2\left(3\right)}+n_{H_2\left(4\right)}=\dfrac{12,32}{22,4}-0,3=0,25\left(mol\right)\)
Mặt khác: \(m_{Al}=0,2\cdot27=5,4\left(g\right)\) \(\Rightarrow m_{Fe}+m_{Mg}=6,6\left(g\right)\)
Gọi số mol của Fe là \(a\) \(\Rightarrow n_{H_2\left(3\right)}=a\)
Gọi số mo của Mg là b \(\Rightarrow n_{H_2\left(4\right)}=b\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}56a+24b=6,6\\a+b=0,25\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=\dfrac{3}{160}\\b=\dfrac{37}{160}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=\dfrac{3}{160}\cdot56=1,05\left(g\right)\\m_{Mg}=\dfrac{37}{160}\cdot24=5,55\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{1,05}{12}\cdot100\%=8,75\%\\\%m_{Mg}=\dfrac{5,55}{12}\cdot100\%=46,25\%\\\%m_{Al}=45\%\end{matrix}\right.\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl\left(2\right)}=3n_{Al}=0,6mol\\n_{HCl\left(3\right)}=2n_{Fe}=\dfrac{3}{80}\left(mol\right)\\n_{HCl\left(4\right)}=2n_{Mg}=\dfrac{37}{80}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\Sigma n_{HCl}=1,1mol\) \(\Rightarrow V_{HCl}=\dfrac{1,1}{2}=0,55\left(M\right)\)