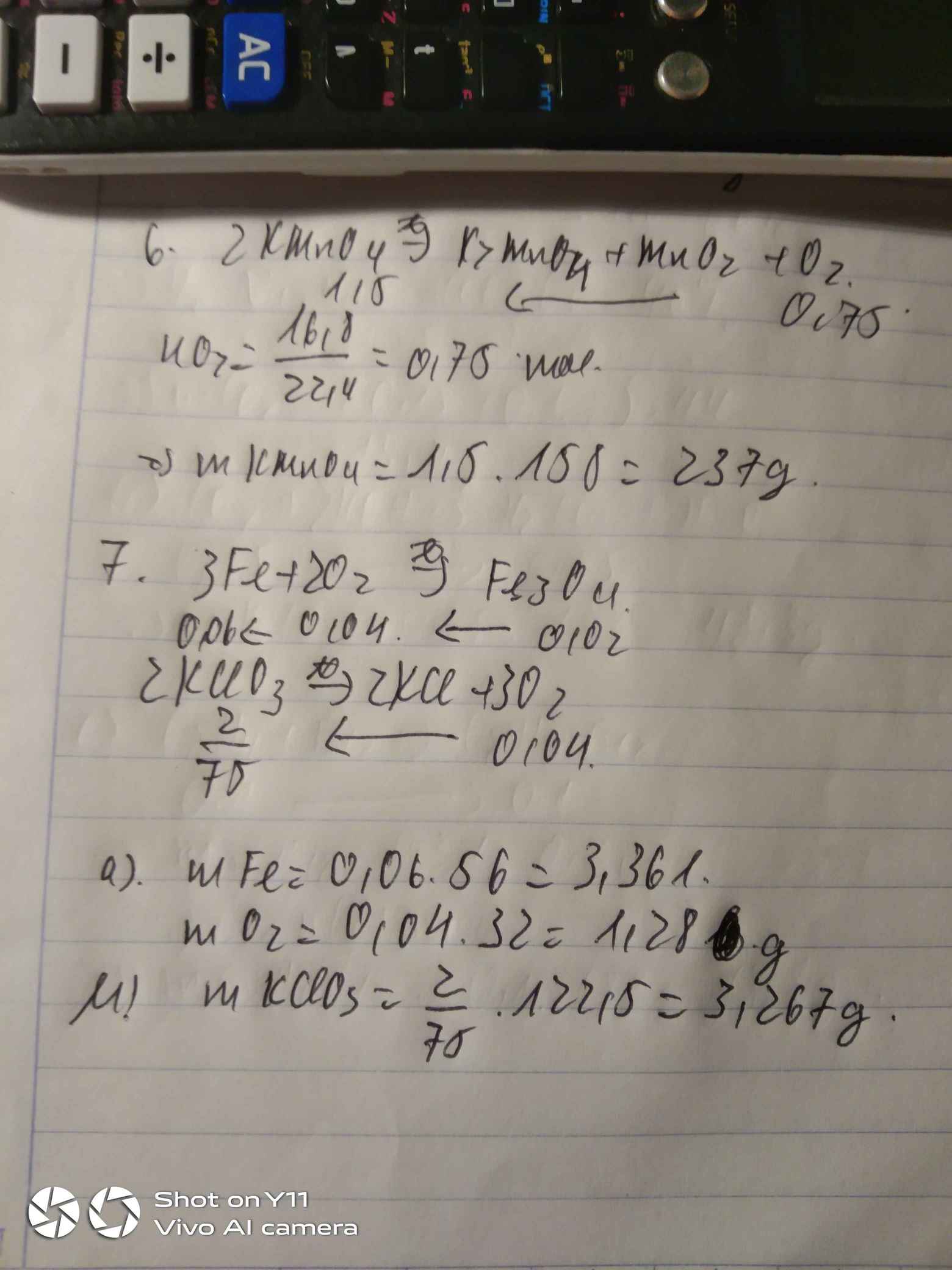Để điều chế được 3,36 lít khí oxi (ở đktc), thì cần nung nóng bao nhiêu gam kali clorat (KClO3)?

Những câu hỏi liên quan
Nung nóng kali clorat KClO3 thu được 3,36 lít khí oxi (đktc) và muối kali clorua KCL
a) Viết phương trình phản ứng
b) Tính khối lượng KClO3 cần dùng.
c) Tính khối lượng muối Kali clorua thu được
a) 2KClO3 --to--> 2KCl + 3O2
b) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
0,1<----------0,1<---0,15
=> \(m_{KClO_3}=0,1.122,5=12,25\left(g\right)\)
c) \(m_{KCl}=0,1.74,5=7,45\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 3: K = 39; Cl = 35,5; O = 16. Trong phòng thí nghiệm để điều chế được 6,72 lít oxi (đktc) thì cần bao nhiêu gam Kali clorat (KClO3): *
nO2=6,72/22,4=0,3(mol)
PTHH: 2 KClO3 -to->2 KCl +3 O2
Ta có: nKClO3=2/3. 0,3=0,2(mol)
=>mKClO3=0,2.122,5=24,5(g)
Đúng 4
Bình luận (0)
Để điều chế oxi trong phòng thí nghiệm người ta nung nóng kali clorat
a) Viết phương trình hoá học
b) Tính khối lượng kali clorua và thể tích khí oxi thu được ( ở đktc) khi nung nóng 12,25g KCLO3. Biết hiệu suất là 85%
c) Tính kali clorat cần dùng để thu được 4,032 lít khí oxi ( ở đktc) khi nung nóng. Biết hiệu suất phản ứng là 80%.
Để điều chế khí oxi trong phòng thí nghiệm, người ta nung nóng 55,125 gam kali clorat KClO3 ở nhiệt độ cao với chất
xúc tác MnO2. Tính thể tích khí oxi thu được ở đktc, biết hiệu suất của phản ứng đạt 85%.
\(n_{KClO_3\left(bd\right)}=\dfrac{55,125}{122,5}=0,45\left(mol\right)\)
=> \(n_{KClO_3\left(pư\right)}=\dfrac{0,45.85}{100}=0,3825\left(mol\right)\)
PTHH: 2KClO3 --to,MnO2--> 2KCl + 3O2
0,3825------------------->0,57375
=> \(V_{O_2}=0,57375.22,4=12,852\left(l\right)\)
Đúng 4
Bình luận (0)
2KClO3-to>2KCl+3O2
0,45---------------------0,675 mol
n KClO3=\(\dfrac{55,125}{122,5}\)=0,45 mol
=>H=85%
=>VO2=0,675.22,4.\(\dfrac{85}{100}\)=12,852l
Đúng 3
Bình luận (1)
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi. a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này. b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
Đọc tiếp
Nung nóng kali clorat có xúc tác là MnO2 thu được kali clorua và khí oxi.
a. Nung nóng 12,25 gam kali clorat thu được 6,8 gam kali clorua. Tính hiệu suất của phản ứng này.
b. Tính khối lượng kali clorat cần dùng để điều chế được 6,72 lít khí oxi (đktc). Biết hiệu suất phản ứng là 85%.
c. Tính khối lượng oxi điều chế được khi phân hủy 24,5 g kali clorat. Biết hiệu suất phản ứng là 80%.
2KClO3-to\xt->2KCl+3O2
0,1------------------0,1
n KClO3=\(\dfrac{12,25}{122,5}\)=0,1 mol
=>m KCl=0,1.74,5=7,45g
H=\(\dfrac{6,8}{7,45}.100\)=91,275%
b)
2KClO3-to\xt->2KCl+3O2
0,2-------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
H=85%
=>m KClO3=0,2.122,5.\(\dfrac{100}{85}\)=28,82g
c)
2KClO3-to\xt->2KCl+3O2
0,2------------------------0,3
n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
H=80%
=>m O2=0,3.32.\(\dfrac{80}{100}\)=10,4g
Đúng 3
Bình luận (0)
Bài 6: Nung nóng Kali pemanganat KMnO4 thu được K2MnO4, MnO2 và khí O2. Hãy tính khối lượng KMnO4 cần thiết để điều chế 16,8 lít khí oxi (đktc).Bài 7: a, Tính số gam sắt và oxi cần dung để điều chế 4,64g oxit sắt từ Fe3O4. b, Tính số gam Kali clorat KClO3 cần dùng để có lượng oxi dùng cho phản ứng trên.
Đọc tiếp
Bài 6: Nung nóng Kali pemanganat KMnO4 thu được K2MnO4, MnO2 và khí O2. Hãy tính khối lượng KMnO4 cần thiết để điều chế 16,8 lít khí oxi (đktc).
Bài 7: a, Tính số gam sắt và oxi cần dung để điều chế 4,64g oxit sắt từ Fe3O4. b, Tính số gam Kali clorat KClO3 cần dùng để có lượng oxi dùng cho phản ứng trên.
Câu 6.
\(n_{O_2}=\dfrac{16,8}{22,4}=0,75mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
1,5 0,75
\(m_{KMnO_4}=1,5\cdot158=237g\)
Câu 7.
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,04 0,02
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{75}\) 0,04
\(m_{KClO_3}=\dfrac{2}{75}\cdot122,5=\dfrac{49}{15}\approx3,27g\)
Đúng 3
Bình luận (1)
Bài 6 :
\(n_{O_2}=\dfrac{16.8}{22,4}=0,75\left(mol\right)\)
PTHH : 2KMnO4 ----t0-----> K2MnO4 + MnO2 + O2
1,5 0,75
\(m_{KMnO_4}=1,5.158=237\left(g\right)\)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Đốt cháy hoàn toàn 3,6 gam magie trong khí oxi trên thì khối lượng kali clorat cần dùng.
A. Tính thể tích khí oxi (đktc) cần dùng?
B. Nếu dùng dịch KCLO3(có xúc tác MnO2) để điều chế lượng khí oxi trên thì khối lượng kali clorat cần dùng là bao nhiêu?
(O=16,CL=35,5,K=39,Mn=55)
2Mg+O2-to>2MgO
0,15---0,075 mol
2KClO3-to->2KCl+3O2
0,05-----------------------0,075
n Mg=\(\dfrac{3,6}{24}\)=0,15 mol
=>VO2=0,075.22,4=1,68l
=>m KClO3=0,05.122,5=6,125g
Đúng 3
Bình luận (0)
a. \(n_{Mg}=\dfrac{3.6}{24}=0,15\left(mol\right)\)
PTHH : 2Mg + O2 ----to----> 2MgO
0,15 0,075
\(V_{O_2}=0,075.22,4=1,68\left(l\right)\)
b. PTHH : 2KClO3 \(\xrightarrow[MnO_2]{t^o}\) 2KCl + 3O2
0,05 0,075
\(m_{KClO_3}=0,05.122,5=6,125\left(g\right)\)
Đúng 1
Bình luận (0)
Để điều chế khí oxi trong phòng thí nghiệm, đem nhiết phân KClO3
a, Nếu nung 3,675g KClO3 thì thể tích khí oxi thu được bao nhiêu lít ở đktc?
b, Nếu thu được 11,2 lít khí oxi ở đktc thì khối lượng KClO3 cần dùng là bao nhiêu g?
\(a.\)
\(n_{KClO_3}=\dfrac{3.675}{122.5}=0.03\left(mol\right)\)
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(0.03........................0.045\)
\(V_{O_2}=0.045\cdot22.4=1.008\left(l\right)\)
\(n_{O_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(\Rightarrow n_{KClO_3}=\dfrac{0.5\cdot2}{3}=\dfrac{1}{3}mol\)
\(\Rightarrow m_{KClO_3}=\dfrac{1}{3}\cdot122.5=40.83\left(g\right)\)
Đúng 2
Bình luận (0)
Thể tích khí SO2 thu được ở đktc khi đốt cháy hoàn toàn 3,2 gam lưu huỳnh là bao nhiêu?A. 1,12 lít B. 2,24 lít C. 3,36 lít D. 4,48 lítCâu 30. Khối lượng KClO3 cần dùng để điều chế được 3,36 lít khí oxi ở đktc là bao nhiêu?A. 6,125 gam B. 12,25 gam C. 18,375 gam D. 24,5 gamCâu 31. Khối lượng KMnO4 cần dùng để điều chế được 2,24 lít khí oxi ở đktc là bao nhiêu?A. 15,8 gam B. 23,7 gam C. 31,6 gam D. 47,4 gam.Câu 32. Thể tích khí H2 cần dùng ở đktc để khử hoàn toàn 8 gam đồng oxit (CuO) là bao nhiêu...
Đọc tiếp
Thể tích khí SO2 thu được ở đktc khi đốt cháy hoàn toàn 3,2 gam lưu huỳnh là bao nhiêu?
A. 1,12 lít B. 2,24 lít C. 3,36 lít D. 4,48 lít
Câu 30. Khối lượng KClO3 cần dùng để điều chế được 3,36 lít khí oxi ở đktc là bao nhiêu?
A. 6,125 gam B. 12,25 gam C. 18,375 gam D. 24,5 gam
Câu 31. Khối lượng KMnO4 cần dùng để điều chế được 2,24 lít khí oxi ở đktc là bao nhiêu?
A. 15,8 gam B. 23,7 gam C. 31,6 gam D. 47,4 gam.
Câu 32. Thể tích khí H2 cần dùng ở đktc để khử hoàn toàn 8 gam đồng oxit (CuO) là bao nhiêu?
A. 1,12 lít B. 2,24 lít C. 3,36 lít D. 4,48 lít
Câu 33. Khối lượng kim loại thu được khi cho 23,2 gam Ag2O phản ứng hoàn toàn với H2 dư, nung nóng là bao nhiêu?
A. 10,8 gam B. 16, 2 gam C. 21,6 gam D. 43,2 gam
Câu 34. Khối lượng chất rắn thu được khi đốt cháy 15,5 gam photpho trong bình chứa 11,2 lít khí oxi (ở đktc) là bao nhiêu?
A. 28,4 gam B. 35,5 gam C. 31,5 gam D. 56,8 gam
Câu 35. Khử hoàn toàn 46,4 gam hỗn hợp oxit CuO, FeO, Ag2O bằng V lít khí H2 vừa đủ, sau phản ứng thu được 40 gam kim loại. Giá trị của V là bao nhiêu?
A. 2,24 lít B. 4,48 lít C. 8,96 lít D. 13,44 lít