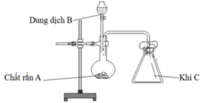
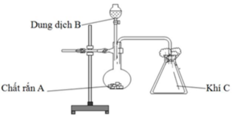
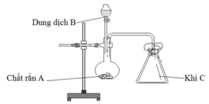
Bài 6. Trong phòng thí nghiệm cần điều chế 5,6 lít khí oxi (ở đktc). Hỏi phải dùng bao nhiêu gam kali clorat KCLO3? (Biết rằng khí oxi thu đc sau phản ứng bị hao hút 10%)
Bài 7. Oxi hoá hoàn toàn m gam hỗn hợp lưu huỳnh và photpho trong bình chứa khí oxi dư thu đc một chất khí có mùi hắc khó thở và 28,4gam một chất bột màu trắng bám trên thành bình.
a, Hãy cho biết công thức hoá học của chất bột, chất khí nói trên
b, Tính phần trăm về khối lượng của từng chất trong hỗn hợp ban đầu biết trong hỗn hợp ban đầu có 20% tạp chất trơ ko tham gia phản ứng và số phân tử chất dạng bột tạo thành gấp 2 lần số phân tử chất dạng khí.
c, Tính số phân tử khí oxi đã tham gia phản ứng.