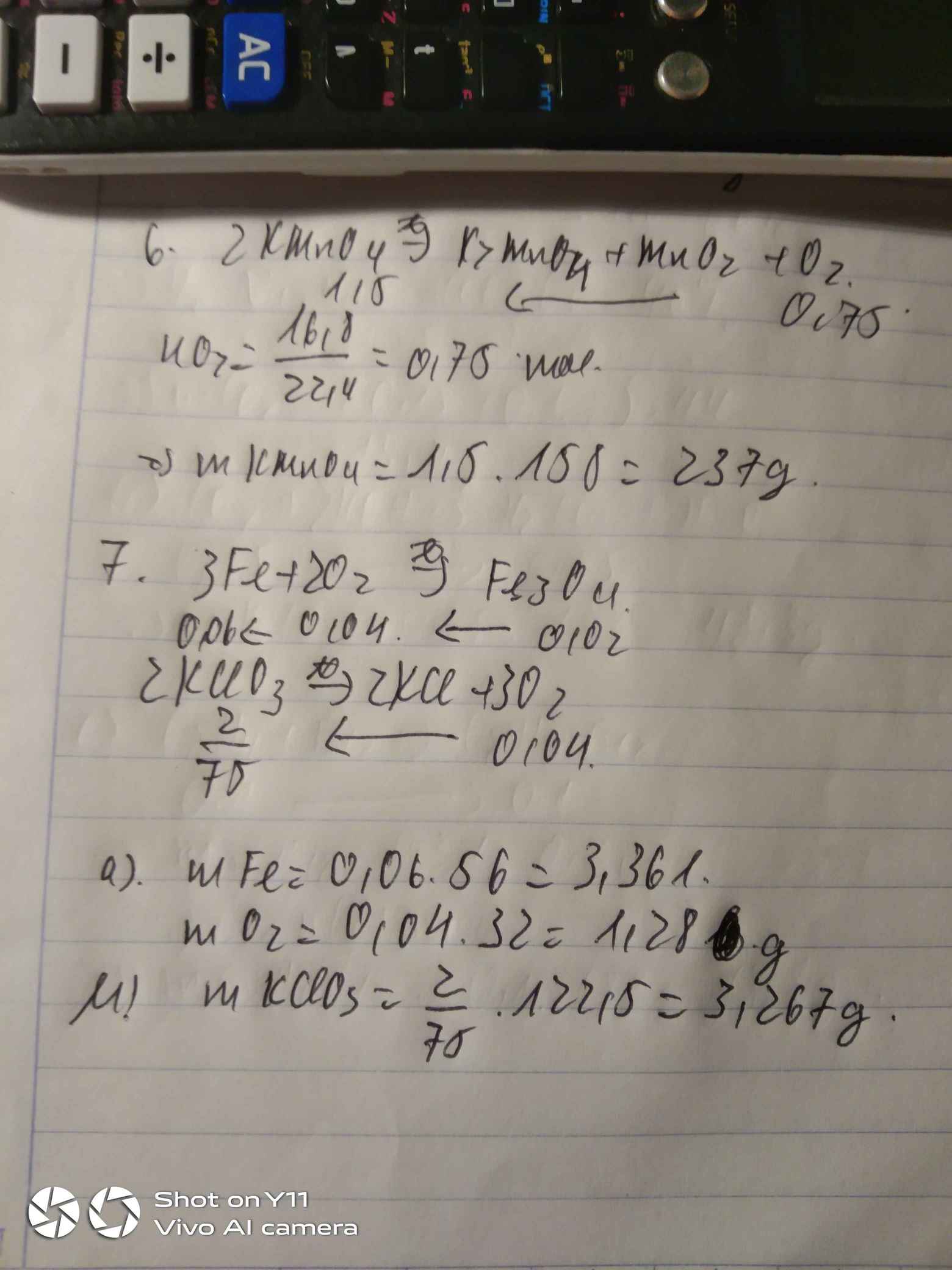Để điều chế t = 6,72 lít (đktc) khí oxi trong phòng thí nghiệm, người ta đã đun
nóng hết một lượng kali pemanganat.
a. Tính khối lượng kali pemanganat đã dùng.
b. Tính khối lượng chất rắn thu được ( 2 cách)?
c. Để điều chế nhôm oxit, người ta oxi hóa hoàn toàn bột nhôm bởi khí oxi
trong không khí và đã dùng 2,5t lít không khí (đktc). Tính thể tích khí oxi
đã dùng, biết oxi chiếm 20% thể tích không khí. Tính khối lượng nhôm
oxit thu được.