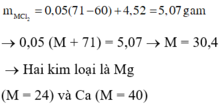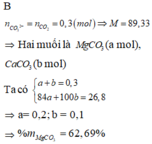Hòa tan hoàn toàn 9,36 gam hỗn hợp hai muối cacbonat của hai kim loại (nhóm IIA, hai chu kì liên
tiếp) vào dung dịch HCl dư, thu được 2,24 lít CO 2 (đktc). Hai kim loại và khối lượng muối trong dung dịch
thu được

Những câu hỏi liên quan
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200 ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là A. 5,07 gam và Mg, Ca B. 5,70 gam và Be, Mg C. 5,70 gam và Mg, Ca D. 5,07 gam và Sr, Ba
Đọc tiếp
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200 ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là
A. 5,07 gam và Mg, Ca
B. 5,70 gam và Be, Mg
C. 5,70 gam và Mg, Ca
D. 5,07 gam và Sr, Ba
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là A. 5,07 gam và Mg, Ca. B. 5,70 gam và Be, Mg. C. 5,07 gam và Mg, Ca. D. 5,70 gam và Sr, Ba.
Đọc tiếp
Hòa tan hết 4,52 gam hỗn hợp gồm hai muối cacbonat của hai kim loại nhóm IIA thuộc hai chu kì kế tiếp nhau bằng 200ml dung dịch HCl 0,5M. Sau phản ứng thu được dung dịch C và 1,12 lít khí D (đktc). Khối lượng chất tan trong dung dịch C và hai kim loại là
A. 5,07 gam và Mg, Ca.
B. 5,70 gam và Be, Mg.
C. 5,07 gam và Mg, Ca.
D. 5,70 gam và Sr, Ba.
Hòa tan 26,8 gam hỗn hợp hai muối cacbonat của hai kim loại (cùng thuộc nhóm IIA và ở hai chu kì liên tiếp của bảng tuần hoàn) tan trong dung dịch HCl vừa đủ. Sau phản ứng thu được 6,72 lít khí (đktc). Thành phần phần trăm khối lượng của muối cacbonat có phân tử khối nhỏ hơn là
A. 56,2%
B. 62,69%
C. 29,6%
D. 25,3 %
hòa tan hoàn toàn 18,4 gam hỗn hợp 2 muối cacbonat của 2 kim loại X,Y thuộc rnhóm IIA và thuộc hai chu kì liên tiếp bằng dung dịch HCl thu được 4,48 lít CO2 (đktc). Hai kim loại X,Y là ?
n muối = n CO2 = 0,2 mol
--> PTK muối = 18,4/0,2 = 92
--> NTK kim loại = 92 - 60 = 32
Vì 24 < 32 < 40 --> hai kim loại là Mg và Ca
Đúng 0
Bình luận (1)
5.Cho 9,1 gam hỗn hợp hai muối cacbonat trung hòa của 2 kim loại kiềm (1A) ở 2 chu kỳ liên tiếp tan hoàn toàn trong dung dịch HCl dư thu được 2,24 lít khí CO2 (đktc). Hai kim loại đó là?
Gọi công thức muối cacbonat trung hòa của 2 kim loại kiềm cần tìm là R2CO3
\(R_2CO_3+2HCl\rightarrow2RCl+H_2O+CO_2\)
\(n_{CO_2}=n_{R_2CO_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \Rightarrow M_{R_2CO_3}=2M_R+60=\dfrac{9,1}{0,1}=91\\ \Rightarrow M_R=15,5\)
Do 2 kim loại kiềm ở chu kì liên tiếp nhau
=> 2 kim loại đó là Li, Na
Đúng 0
Bình luận (0)
X, Y là 2 muối cacbonat của kim loại nhóm IIA thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Hoà tan 28,4 gam hỗn hợp X, Y bằng dung dịch HCl thu được 6,72 lít khí
CO
2
(đktc). Các kim loại nhóm IIA là: A. Be và Mg B. Mg và Ca C. Ca và Sr. D. Sr và Ba
Đọc tiếp
X, Y là 2 muối cacbonat của kim loại nhóm IIA thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Hoà tan 28,4 gam hỗn hợp X, Y bằng dung dịch HCl thu được 6,72 lít khí CO 2 (đktc). Các kim loại nhóm IIA là:
A. Be và Mg
B. Mg và Ca
C. Ca và Sr.
D. Sr và Ba
Hoà tan hoàn toàn 18,4 gam hỗn hợp hai muối cacbonat của hai kim loại X, Y thuộc hai chu kì liên tiếp trong nhóm II A bằng dung dịch HCl thu được 4,48 lít C O 2 (đktc). Xác định tên hai kim loại X và Y.
Hòa tan hoàn toàn 3,68 gam hỗn hợp hai kim loại liên tiếp nhau trong nhóm IIA trong dung dịch
HCl dư thu được 10,78 gam muối clorua và V lít khí H2 (đktc).
a) Xác định hai kim loại trong hỗn hợp và khối lượng mỗi kim loại đó.
b) Tính giá trị của V?
a) Gọi công thức chung của 2 kim loại là M
\(n_M=\dfrac{3,68}{M_M}\left(mol\right)\)
PTHH: M + 2HCl --> MCl2 + H2
\(\dfrac{3,68}{M_M}\)----------->\(\dfrac{3,68}{M_M}\)
=> \(\dfrac{3,68}{M_M}\left(M_M+71\right)=10,78\)
=> MM = 36,8(g)
Mà 2 kim loại liên tiếp nhau
=> 2 kim loại là Mg, Ca
Gọi số mol của Mg, Ca là a, b
=> 24a + 40b = 3,68
PTHH: Mg + 2HCl --> MgCl2 + H2
a----------------->a------>a
Ca + 2HCl --> CaCl2 + H2
b---------------->b------->b
=> 95a + 111b = 10,78
=> a = 0,02 ; b = 0,08
=> \(\left\{{}\begin{matrix}m_{Mg}=0,02.24=0,48\left(g\right)\\m_{Ca}=0,08.40=3,2\left(g\right)\end{matrix}\right.\)
b) VH2 = (a+b).22,4 = 2,24(l)
Đúng 1
Bình luận (0)
Cho hỗn hợp X gồm 2 kim loại thuộc nhóm IIA, ở hai chu kì liên tiếp nhau. Cho 8,4 gam X tan hòan toàn trong dung dịch HCl dư thu được 5,6 lít khí H2( đktc). Cô cạn dung dịch sau phản ứng thu được khối lượng muối khan là: A. 26,15 gam B. 17,275 gam C. 8,9 gam D. 43,9 gam
Đọc tiếp
Cho hỗn hợp X gồm 2 kim loại thuộc nhóm IIA, ở hai chu kì liên tiếp nhau. Cho 8,4 gam X tan hòan toàn trong dung dịch HCl dư thu được 5,6 lít khí H2( đktc). Cô cạn dung dịch sau phản ứng thu được khối lượng muối khan là:
A. 26,15 gam
B. 17,275 gam
C. 8,9 gam
D. 43,9 gam
Đáp án: A
Ta có: nHCl= 2nH2 = 0,5 mol
m muối = m kim loại + mCl-
= 8,4 + 0,5. 35,5 = 26,15 gam
Đúng 0
Bình luận (0)