Cho V lít (dktc) hỗn hợp khí X gồm C2H2 và H2 đi qua ống chứa xúc tác Ni, đun nóng thu được hỗn hợp gồm 3 hidrocacbon có tỉ khối so với H2 bằng 13,5. Phần trăm thể tích khí C2H2 trong X ?
Cho 10,08 lít (đktc) hỗn hợp khí X gồm C2H2 và H2 đi qua ống chứa xúc tác Ni, nung nóng thu được hỗn hợp Y chỉ chứa 3 hiđrocacbon. Tỉ khối của Y so với He là 7,125. Tính phần trăm thể tích của C2H2 trong hỗn hợp X:
A. 62,25%
B. 45,55%
C. 36,73%
D. 44,44%
Cho 10,08 lít (đktc) hỗn hợp khí X gồm C2H2 và H2 đi qua ống chứa xúc tác Ni, nung nóng thu được hỗn hợp Y chỉ chứa 3 hiđrocacbon. Tỉ khối của Y so với He là 7,125. Phần trăm thể tích của C2H2 trong hỗn hợp X là
A. 36,73%.
B. 44,44%.
C. 62,25%.
D. 45,55%.
Gọi : \(n_{C_2H_2} = a(mol); n_{H_2} = b(mol)\)
⇒ a + b = \(\dfrac{10,08}{22,4} = 0,45(1)\)
Vì sau phản ứng ,H2 hết
Suy ra: \(n_Y = n_X - n_{H_2} = 0,45 - b(mol)\)
Bảo toàn khối lượng :
\(m_X = m_Y\\ \Leftrightarrow 26a + 2b = (0,45-b).7,125.4\\ \Leftrightarrow 26a + 30,5b = 12,825(2)\)
Từ (1)(2) suy ra a = 0,2 ; b = 0,25
Vậy :
\(\%V_{C_2H_2} = \dfrac{0,2}{0,45}.100\% = 44,44\%\\ \%V_{H_2} = 100\%- 44,44\% = 55,56\%\)
Dẫn 2,24 lít hỗn hợp khí X gồm C2H2 và H2 (có tỉ lệ thể tích V(C2H2) : V(H2) = 2 : 3) đi qua Ni nung nóng thu được hỗn hợp Y, cho Y đi qua dung dịch Br2 dư thu được 896ml hỗn hợp khí Z bay ra khỏi bình dung dịch Br2. Tỉ khối của Z đối với H2 bằng 4,5. Biết các khí đều đo ở đktc. Khối lượng bình Br2 tăng thêm là
A. 0,4 gam
B. 0,8 gam
C. 1,6 gam
D. 0,6 gam
Đáp án B
Ta có nC2H2 = 0,04 mol, nH2 = 0,06 mol
Bảo toàn khối lượng → mX = m bình tăng + mZ
→ mbình tăng = 0,04.26 + 0,06.2-4,5.2.0,04 = 0,8 gam
Cho hỗn hợp X gồm C2H2 và H2 qua xúc tác Ni nung nóng, phản ứng hoàn toàn thu được hỗn hợp Y gồm 3 hidrocacbon có tỉ khối của Y so với H2 là 14,5. Hỏi tỉ khối của X vói H2 là bao nhiêu.
A. 7,8.
B. 6,7.
C. 6,2.
D. 5,8.
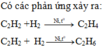
Y chỉ gồm 3 hidrocacbon => H2 phản ứng hết.
Vậy Y gồm 3 hidrocacbon là C2H2 dư, C2H4 và C2H6.
Ta để ý thấy cả 3 hidrocacbon của Y đều có 2 nguyên tử C.
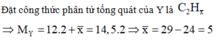
Do đó các hidrocacbon trong Y có công thức chung là C2H5.
Do tỉ khối không tùy thuộc vào lượng chất ban đầu nên ta tự chọn lượng chất ban đầu.
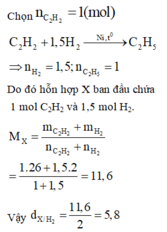
Đáp án D.
Cho 6,72 lít (đktc) hỗn hợp khí X gồm C2H2 và H2 qua bình đựng Ni nung nóng), thu được hỗn hợp khí Y (chỉ chứa 3 hiđrocacbon) có tỉ khối so với H2 là 13,5. Biết Y phản ứng tối đa với t mol Br2 trong dung dịch a) Tính t b) Trình bày phương pháp hóa học để tách riêng từng khí trong Y.
Hỗn hợp khí X gồm 0,3 mol C2H4; 0,15 mol C2H2 và 0,5 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 13,3. Hỗn hợp Y phản ứng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
A. 0,1
B. 0,15
C. 0,25
D. 0,3
Hỗn hợp khí X gồm 0,3 mol C2H4; 0,15 mol C2H2 và 0,5 mol H2. Đun nóng X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 13,3. Hỗn hợp Y phản ứng tối đa với x mol Br2 trong dung dịch. Giá trị của x là
A. 0,1
B. 0,15
C. 0,25
D. 0,3
Đáp án B
hhX gồm 0,3 mol C2H4; 0,15 mol C2H2 và 0,5 mol H2.
Đun nóng X với Ni → hhY có dY/H2 = 13,3.
• Theo BTKL; mX = mhh ban đầu = 0,3 x 28 + 0,15 x 26 + 0,5 x 2 = 13,3 gam
→ nX = 13,3 : (13,3 x 2) = 0,5 mol.
Ta có:
nH2phản ứng = nhh ban đầu - nX = (0,3 + 0,15 + 0,5) - 0,5 = 0,45 mol.
nπ trước phản ứng = 1 x nC2H4 + 2 x nCH≡CH
= 0,3 + 2 x 0,15 = 0,6 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,6 - 0,45 = 0,15 mol
→ nBr2 = 0,15 mol
Hỗn hợp X gồm C2H2 và H2 (có tỉ lệ mol tương ứng là 1 : 2). Đun nóng 10,08 lít (đktc) hỗn hợp X với xúc tác Ni, sau một thời gian thu được hỗn hợp khí Y. Dẫn hỗn hợp Y qua dung dịch nước brom dư, thấy bình brom tăng 3 gam và còn lại V lít (đktc) hỗn hợp khí Z không bị hấp thụ. Tỉ khối của Z so với heli bằng 5/3. Giá trị của V là
A. 13,44 lít
B. 4,48 lít
C. 10,08 lít
D. 5,04 lít
Đáp án D
Ta có nC2H2 = 0,15 mol, nH2 = 0,3 mol
Ta có mX = mY = mbình tăng + mZ
→ 0,15. 26 + 0,3. 2 = 3 + mZ → mZ = 1,5 gam
→ nZ =
1
,
5
5
3
.
4
= 0,225 mol → V= 5,04 lít.