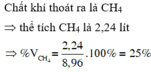Cho 8,288 l hh khí gồm Metan, Etilen đi qua dd Brom dư thấy dd nhạt màu và còn lại 7,84 lít khíthóat ra (đktc). %V của 2 chất trên lần lượt là:
A. 94% và 6% B. 5,4% và 94,6% C. 94,6% và 5,4% D. 60% và 40%
Những câu hỏi liên quan
Cho 0,448 lít hỗn hợp khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 0,112 lít khí thoát ra. Biết các thể tích khí đo ở đktc, thành phần % thể tích khí metan có trong hỗn hợp là
A. 25%
B. 50%.
C. 60%.
D. 37,5%.
- Do dung dịch brom dư, nên khí thoát ra là metan.
![]()
- Chọn đáp án A.
Đúng 0
Bình luận (0)
Cho hh khí X gồm 0.15mol metan, 0.2mol axetilen, 0.1mol etilen, và 0.42mol H2 đi qua ống sứ đựng Ni làm xúc tác, đun nóng thu hh khí Y. Dẫn Y qua bình dd Brom dư thấy bình Brom nhạt màu, khối lượng bình tăng 3.54g và có m(g) khí Z thoát ra khỏi bình. Giá trị của m =?
Dẫn 1,12 lít hh A(metan và etilen) đo ở đktc qua dd brom thì sau pứ làm mất màu tối đa 40g dd brom 4%.Thành phần % thể tích metan và etilen lần lượt là bao nhiêu?
\(n_A=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ n_{Br_2}=\dfrac{40.4\%}{160}=0,01\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,01<---0,01
\(\rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,01}{0,05}.100\%=20\%\\\%V_{CH_4}=100\%-20\%=80\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 1,4g anken A làm mất màu 8g ddb ra) Xét CTPT A, gọi tênb) Cho 4,48 lít hh khí gồm anken A và khí metan đi qua dd br dư thấy nhạt màu và còn 1,12 lít khí thoát ra các thể tích khí thoát ra ở điều kiện tiêu chuẩn tính % mỗi khí trong hh ban đ...
Xem chi tiết
\(n_{Br_2}=\dfrac{8}{160}=0.05\left(mol\right)\)
\(C_nH_{2n}+Br_2\rightarrow C_nH_{2n}Br_2\)
\(0.05.........0.05\)
\(M_A=\dfrac{1.4}{0.05}=28\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow14n=28\)
\(\Rightarrow n=2\)
\(CTPT:C_2H_4\)
\(\Rightarrow etilen\)
\(b.\)
\(V_{CH_4}=1.12\left(l\right)\)
\(\Rightarrow V_{C_2H_4}=4.48-1.12=3.36\left(l\right)\)
\(\%V_{CH_4}=\dfrac{1.12}{4.48}\cdot100\%=25\%\)
\(\%V_{C_2H_4}=75\%\)
Đúng 1
Bình luận (0)
Cho 4,48 lít khí gồm metan và etilen đi qua dung dịch brom dư, thấy dung dịch nhạt màu và còn 1,12 lít khí thoát ra. Các thể tích khí đo ở điều kiện tiêu chuẩn. Thành phần phần trăm thể tích của khí metan trong hỗn hợp là:
A. 25% ; B. 50% ; C. 60% ; D. 37,5%
Hãy chọn đáp án đúng
- Đáp án A
- Khi cho hỗn hợp khí (gồm CH4 và C2H4 ) đi qua dung dịch brom thì C2H4 sẽ phản ứng hết với dung dịch brom, CH4 không tác dụng sẽ đi ra khỏi bình.
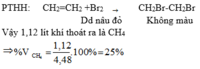
Đúng 0
Bình luận (0)
Dẫn 8,96 lít hỗn hợp khí X gồm metan và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều do(đktc)). Thành phần phần trăm thể tích của metan trong X là
A. 25,0%
B. 50,0%
C. 60,0%
D. 37,5%
Đáp án A
Hướng dẫn
Chất khí thoát ra là CH4 => thể tích CH4 là 2,24 lít
=> % V C H 4 = 2 , 24 8 , 96 .100% = 25%
Đúng 0
Bình luận (0)
Cho 6(g) hỗn hợp khí X(metan,etilen) đi qua dd brom dư, thấy dd bị nhạt màu và có 4.48(l) khí thoát ra. Các V đo ở dktc
a, Tính % theo V mỗi khí trong hh X
b, Đốt cháy ht hh X. Cho toàn bộ sản phẩm cháy vào 300 ml dd Ca(OH)_2 1M thu được m(g) kết tủa. Tính m
a) C2H4 + Br2 ---> C2H4Br2
Khí thoát ra là CH4 (metan) ---> mCH4 = 0,2.16 = 3,2g ---> mC2H4 = 6 - 3,2 = 2,8g. (0,1 mol).
---> %CH4 = 0,2/0,3 = 66,7%; %C2H4 = 33,3%.
b) nCO2 = nCH4 + 2nC2H4 = 0,4 mol.
CO2 + Ca(OH)2 ---> CaCO3 + H2O
CO2 + CaCO3 + H2O ---> Ca(HCO3)2
---> nCaCO3 = 0,2 mol ---> m = 0,2.100 = 20g.
Đúng 0
Bình luận (0)
Dẫn 8,96 lít hỗn hợp khí X gồm metan và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều đo ở đktc). Thành phần phần trăm thể tích của metan trong X là A. 25,0% B. 50,0% C. 60,0% D. 37,5%
Đọc tiếp
Dẫn 8,96 lít hỗn hợp khí X gồm metan và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều đo ở đktc). Thành phần phần trăm thể tích của metan trong X là
A. 25,0%
B. 50,0%
C. 60,0%
D. 37,5%
Dẫn 7,84 lít hỗn hợp khí etilen và metan(đktc) qua dd Brom dư ,thấy khối lượng tăng lên 4,2 gam . Tính thành phần % thể tích mỗi khí trong hỗn hợp đầu.
\(n_{hhkhí\left(C_2H_4,CH_4\right)}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(m_{tăng}=m_{C_2H_4}=4,2\left(g\right)\\ n_{C_2H_4}=\dfrac{4,2}{28}=0,15\left(mol\right)\\ \%V_{C_2H_4}=\dfrac{0,15}{0,35}=42,85\%\\ \%V_{CH_4}=100\%-42,85\%=57,15\%\)
Đúng 3
Bình luận (0)