Cho 28 g một oxit kim loại R hóa trị 2 tác dụng vừa đủ với 250 ml dd h2so4 2M xác dịnh công thức . Help me

Những câu hỏi liên quan
Hòa tan hoàn toàn 8 gam một oxit kim loại A( A có hóa trị 2 trong hợp chất) cần dùng vừa đủ 400 ml dd HCl 1M
1. Xác định kim loại A và công thức hóa học của oxit
2. cho 8,4 gam ACO3 tác dụng với 500 ml dd H2SO4 1M đến khi phản ứng xảy ra hoàn toàn. Tính nồng độ mol của các chất trong dd sau phản ứng ( coi thể tích dd sau phản ứng là 500 ml )
Cho 20g oxit của kim loại hóa trị II tác dụng vừa hết với 500 ml dd H 2 S O 4 1M. Công thức phân tử của oxit là
A. MgO.
B. FeO.
C. CuO.
D. CaO.
cho 8g một oxit kim loại hóa trị 2 tác dụng vừa đủ với 100g dd h2so4 9,8%. Tìm CTHH của oxit
Gọi A là kim loại có mặt trong oxit cần tìm
\(PTHH:AO+H_2SO_4\rightarrow ASO_4+H_2O\\ n_{H_2SO_4}=\dfrac{100.9,8\%}{98}=0,1\left(mol\right)\\ n_{AO}=n_{H_2SO_4}=0,1\left(mol\right)\\ M_{AO}=\dfrac{8}{0,1}=80\left(\dfrac{g}{mol}\right)=M_A+16\\ \Rightarrow M_A=64\left(\dfrac{g}{mol}\right)\\ \Rightarrow Oxit.AO:CuO\)
Đúng 2
Bình luận (0)
Gọi cthh của oxit kim loại hóa trị II là RO.
RO + H2SO4 --> RSO4 + H2O (1)
mH2SO4 = 9,8%.100 = 9,8 (g)
-> nH2SO4 = 9,8/98 = 0,1 (mol)
nRO = 8/R+16 (mol)
Từ (1) -> nRO = nH2SO4 = 0,1mol
-> 8/R+16 = 0,1 -> R = 64 -> R là Cu
Đúng 0
Bình luận (0)
Cho 8g oxit của một kim loại hóa trị III tác dụng vừa đủ với 150ml dung dịch H2SO4 1M. Tìm công thức của oxit.
\(A_2O_3+3H_2SO_4\rightarrow3H_2O+A_2\left(SO_4\right)_3\)
mol 0,05 0,15
\(N_{H_2SO_4}=1.0,15=0,15\left(mol\right)\)
\(N_{A_2O_3}=\frac{0,15}{3}=0,05\left(mol\right)\)
\(M_{A_2O_3}=\frac{8}{0,05}=160\left(g\right)\)
=>\(2A+16.3=160\)
<=>\(2A=112\)
<=>\(A=56\)=> A là Fe
Vậy CT là \(Fe_2O_3\)
Đúng 0
Bình luận (0)
Cho 8,4 gam một oxit kim loại có hóa trị II tác dụng vừa đủ với 100 ml dung dịch H2SO41,5M. Công thức hóa học của oxit là
A. BaO.B. MgO. C. CaO. D. ZnO.
\(n_{H_2SO_4}=0,1.1,5=0,15\left(mol\right)\)
PTHH: RO + H2SO4 → RSO4 + H2O
Mol: 0,15 0,15
\(M_{RO}=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
\(\Rightarrow M_R=56-16=40\left(g/mol\right)\)
⇒ R là canxi (Ca)
Vậy CTHH là CaO
⇒ Chọn C
Đúng 1
Bình luận (0)
cho 5,4 g một kim loại R( có hóa trị từ 1 đến 3) tác dụng vừa đủ với dung dịch h2so4 loãng dư thu được 34,2 (g) muối. xác định kim loại R
Gọi hóa trị của R là n
PTHH : \(2R+nH_2SO_4-->R_2\left(SO_4\right)n+nH_2\)
Theo pthh : \(n_{R2\left(SO4\right)n}=\dfrac{1}{2}n_R\)
\(\Rightarrow\dfrac{34,2}{2M_R+96n}=\dfrac{1}{2}.\dfrac{5,4}{M_R}\)
\(\Rightarrow M_R=9n\)
Ta có bảng sau :
| n | I | II | III |
| MR | 9 | 18 | 27 |
| KL | Loại | Loại | Al |
Vậy R là kim loại Al
Đúng 1
Bình luận (0)
Cho 6gam một oxit kim loại có hóa trị II tác dụng vừa đủ với 200 gam dung dịch H2SO4 7,35%. Công thức hóa học của oxit là
A. BaO. B. MgO. C. CaO. D. ZnO.
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{m_{H_2SO_4}}{200}.100\%=7,35\%\)
=> \(m_{H_2SO_4}=14,7\left(g\right)\)
=> \(n_{H_2SO_4}=\dfrac{14,7}{98}=0,15\left(mol\right)\)
Gọi oxit kim loại là: MO
PTHH: MO + H2SO4 ---> MSO4 + H2O
Theo PT: \(n_{MO}=n_{H_2SO_4}=0,15\left(mol\right)\)
=> \(M_{MO}=\dfrac{6}{0,15}=40\left(g\right)\)
Ta có: \(M_{MO}=NTK_M+16=40\left(g\right)\)
=> \(NTK_M=24\left(đvC\right)\)
Dựa vào bảng hóa trị, suy ra:
M là Mg
=> Oxit kim loại có CTHH là: MgO
Chon B. MgO
Đúng 2
Bình luận (0)
Cho kim loại sắt Fe tác dụng vừa đủ với 147gam dung dịch H2SO4 có nồng độ 20℅ thu được muối và khí hidro. Dân toàn bộ khí hidro qua 16g oxit kim loại có hóa trị III. Xác định công thức hóa học của oxit cầu cíu các cao nhân
\(n_{H_2SO_4}=\dfrac{147.20\%}{98}=0,3\left(mol\right)\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=n_{axit}=0,3\left(mol\right)\\ Đặt:A_2O_3\\ A_2O_3+3H_2\rightarrow\left(t^o\right)2A+3H_2O\\ n_{oxit}=\dfrac{n_{H_2}}{3}=\dfrac{0,3}{3}=0,1\left(mol\right)\\ M_{oxit}=\dfrac{16}{0,1}=160\left(\dfrac{g}{mol}\right)=2M_A+48\\ \Rightarrow M_A=56\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Sắt\left(Fe=56\right)\\ \Rightarrow Oxit:Fe_2O_3\)
Đúng 1
Bình luận (0)
Cho 20 gam oxit của kim loại hóa trị II tác dụng vừa hết 500 ml dung dịch
H
2
SO
4
1M. Công thức phân tử của oxit là A. MgO. B. FeO. C. CuO. D. CaO.
Đọc tiếp
Cho 20 gam oxit của kim loại hóa trị II tác dụng vừa hết 500 ml dung dịch H 2 SO 4 1M. Công thức phân tử của oxit là
A. MgO.
B. FeO.
C. CuO.
D. CaO.
Đáp án A
Số mol của H 2 SO 4 là: n H 2 SO 4 = 0 , 5 . 1 = 0 , 5 mol
Đặt công thức của oxit kim loại hóa trị II là MO
Phương trình hóa học:
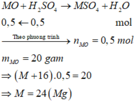
=> Oxit là MgO
Đúng 0
Bình luận (0)



















