Ion R2+ có tổng số các loại hạt là 11. Trong ion R2+ số hạt mang điện bằng 1,2 lần số hạt không mang điện. Viết cấu hình e của nguyên tử R.

Những câu hỏi liên quan
ion x- có tổng số hạt là 29 .Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 9
a)Xác định số hạt e,nowtron va số khối của X
b)Viết cấu hình e của X và ion X-
c)Nguyên tử nguyên tố R có cấu hình e lớp vỏ ngoài cùng 3s2
-Cho biết vị trí(chu kì,nhóm) và tên nguyên tố R
-Cho biết công thức hợp chất T tạo từ R và X
ion x- có tổng số hạt là 29 .Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 9
a)Xác định số hạt e,nowtron va số khối của X
b)Viết cấu hình e của X và ion X-
c)Nguyên tử nguyên tố R có cấu hình e lớp vỏ ngoài cùng 3s2
-Cho biết vị trí(chu kì,nhóm) và tên nguyên tố R
-Cho biết công thức hợp chất T tạo từ R và X
Trong nguyên tử X: số nơtron nhiều hơn số proton là 3 hạt Trong ion X: số hạt mang điện gấp 1,75 lần số hạt không mang điện a) tính số hiệu nguyên tử của X b) viết cấu hình e của nguyên tử X và ion X
Tổng số hạt các loại trong nguyên tử nguyên tố X là 52, trong đó số hạt không mang điện gấp 1,0588 lần số hạt mang điện dương.
a. Tính số khối của X và viết kí hiệu nguyên tử X?
b. Viết cấu hình electron nguyên tử và ion tương ứng của X?
c. Cho biết loại liên kết trong hợp chất oxit cao nhất và hợp chất khí với hidro tạo bởi nguyên tố X?
a) Có \(\left\{{}\begin{matrix}p+e+n=2p+n=52\\n=1,0588p\end{matrix}\right.=>\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)
=> A = 17 + 18 = 35
=> X là Cl
b)
Cấu hình của Cl: 1s22s22p63s23p5
Cấu hình của ion Cl-: 1s22s22p63s23p6
c)
- Hợp chất oxit cao nhất là Cl2O7
Hiệu độ âm điện = 3,44 - 3,16 = 0,28
=> lk cộng hóa trị không phân cực
- Hợp chất khí với hidro là HCl
Hiệu độ âm điện = 3,16 - 2,2 = 0,96
=> lk cộng hóa trị phân cực
Đúng 1
Bình luận (0)
đề bài : một nguyên tử R có tổng số hạt là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện.a) tìm số hạt p,e,n và số khối của nguyên tử Rb)viết cấu hình electron của R theo 4 cách.c) xác định loại nguyên tố R, giải thích?d)nguyên tố R là nguyên tố kim loại, phi kim, hay khí hiếm giải thích?e) để đạt cấu hình e bền của khí hiếm R có khuynh hướng cho hay nhận e, viết cấu hình e của ion mà r có thể tạo thành
Đọc tiếp
đề bài :" một nguyên tử R có tổng số hạt là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện.
a) tìm số hạt p,e,n và số khối của nguyên tử R
b)viết cấu hình electron của R theo 4 cách.
c) xác định loại nguyên tố R, giải thích?
d)nguyên tố R là nguyên tố kim loại, phi kim, hay khí hiếm giải thích?
e) để đạt cấu hình e bền của khí hiếm R có khuynh hướng cho hay nhận e, viết cấu hình e của ion mà r có thể tạo thành
ta co p+n+e =34
ma P=E suy ra 2p +n =34
2p =1,833 +n
p<n<1,5p
suy ra 3p<2p+n<3,5p
3p<34<3,5p
34:3,5<p<34:3
=9,7<p<11,3
thu p=10 va 11 ta thay 11 hop li nen chon p=11=e
r la na va la nguyen to kim loai vi co 1e lop ngoai cung
Đúng 0
Bình luận (0)
Cho các thông tin sau: Ion
X
2
-
có cấu trúc electron:
1
s
2
2
s
2
2
p
6
3
s
2
3
p
6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là...
Đọc tiếp
Cho các thông tin sau:
Ion X 2 - có cấu trúc electron: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z 2 + có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); (Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); (Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
Nguyên tử nguyên tố X có tổng các loại hạt cơ bản là 40, trong đó số hạt mang điện dương ít hơn số hạt không mang điện là 1 hạt.
a. Tìm số khối và điện tích hạt nhân của X.
b. X sẽ tạo thành ion dương hay ion âm ? Viết quá trình hình thành ion tương ứng từ X ?
a) Có p+n+e = 40
=> 2p + n = 40
Mà n - p = 1
=> p=e=13; n = 14
A= 13+14 = 27
Điện tích hạt nhân là 13+
b)
Cấu hình: 1s22s22p63s23p1
=> X nhường 3e để đạt cấu hình electron bền của khí hiếm, tạo ra ion dương
X0 --> X3+ + 3e
Đúng 1
Bình luận (0)
Cho các thông tin sau: Ion X2- có cấu trúc electron: 1s22s22p63s23p6. Nguyến tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29. Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là: A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB). B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhó...
Đọc tiếp
Cho các thông tin sau:
Ion X2- có cấu trúc electron: 1s22s22p63s23p6.
Nguyến tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
Đáp án A
Ion X2- có cấu trúc electron: 1s22s22p63s23p6
X + 2e → X2-
Vậy cấu hình electron của X là 1s22s22p63s23p4
X có 3 lớp electron → X thuộc chu kì 3.
X có số electron = 16 → X thuộc ô 16.
X có 6 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → X thuộc nhóm VIA.
• Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Giả sử số hiệu nguyên tử, số nơtron của Y lần lượt là Z, N
Ta có hpt: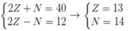
Cấu hình electron của Y là 13Y: 1s22s22p63s23p1
Y có 3 lớp electron → X thuộc chu kì 3.
Y có số electron = 13 → X thuộc ô số 13.
Y có 3 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → Y thuộc nhóm IIIA.
• Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Z có số hạt mang điện tích dương bằng ion Z2+
Cấu hình electron của Z là 29Z: 1s22s22p63s23p63d104s1
Z thuộc ô số 29.
Z có 4 lớp electron → X thuộc chu kì 4.
Z có electron cuối cùng điền vào phân lớp 3d, có 1 electron hóa trị → Z thuộc nhóm IB.
→ Chọn A.
Đúng 0
Bình luận (0)
Ion M2+ có tất cả 58 hạt cơ bản. Số hạt mang điện nhiều hơn số hạt không mang điện 18 hạt. Viết cấu hình e của nguyên tử M và ion M2+.














