Dẫn 4.48 lít khí SO2(đktc) vào 300ml dung dịch KOH 1M thu được dung dịch A. Tính CM của dung dịch A? (biết thể tích dung dịch sau phản ứng không thay đổi)

Những câu hỏi liên quan
Cho 250ml dung dịch H2SO4 1,5M phản ứng với 37,8g Na2SO3 thì thu được V( l ) khí SO2 (đktc)
a Viết PTHH
b Tính thể tích SO2 thu được
c Tính CM các chất dung dịch sau phản ứng ( biết thể tích dung dịch sau pư thay đổi không đáng kể )
250ml = 0,25l
\(n_{H2SO4}=1,5.0,25=0,375\left(mol\right)\)
\(n_{Na2SO3}=\dfrac{37,8}{126}=0,3\left(mol\right)\)
a) Pt : \(H_2SO_4+Na_2SO_3\rightarrow Na_2SO_4+SO_2+H_2O|\)
1 1 1 1 1
0,375 0,3 0,3 0,3
b) Lập tỉ số so sánh : \(\dfrac{0,375}{1}>\dfrac{0,3}{1}\)
⇒ H2SO4 dư , Na2SO3 phản ứng hết
⇒ Tính toán dựa vào số mol của Na2SO3
\(n_{SO2}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,3.22,4=6,72\left(l\right)\)
c) \(n_{Na2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(n_{H2SO4\left(dư\right)}=0,375-0,3=0,075\left(mol\right)\)
\(C_{M_{Na2SO4}}=\dfrac{0,3}{0,25}=1,2\left(M\right)\)
\(C_{M_{H2SO4\left(dư\right)}}=\dfrac{0,075}{0,25}=0,3\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
dẫn 3,36 lít khí clo (đktc) vào 300 ml dung dịch NaOH vừa đủ, ta thu được dung dịch nước Gia-ven. hãy tính nồng độ mol/lít của các chất trong dung dịch sau phản ứng. biết rằng thể tích dung dịch thay đổi không đáng kể.
\(n_{Cl_2}=\dfrac{3,36}{22,4}=0,15mol\\ Cl_2+2NaOH\rightarrow NaCl+NaOH+H_2O\\ n_{NaCl}=n_{NaOH}=n_{Cl_2}=0,15mol\\ C_{M_{NaCl}}=\dfrac{0,15}{0,3}=0,5M\\ C_{M_{NaClO}}=\dfrac{0,15}{0,3}=0,5M\)
Đúng 3
Bình luận (0)
Hoà tan 13gam Zn vào 300ml dung dịch H2SO4 thu được dung dịch A và V lít khí H2 ở đktc , tính V và nồng độ mol/lít của dunh dịch A , biết thể tích thay đổi không đáng kể
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
_____0,2---->0,2------>0,2----->0,2
VH2 = 0,2.22,4 = 4,48(l)
\(C_{M\left(ZnSO_4\right)}=\dfrac{0,2}{0,3}=0,667M\)
Đúng 0
Bình luận (0)
Cho 2,24 lít CO2 (đktc) sục vào bình đựng 250ml dung dịch koh 1M sản phẩm tạo ra là K2CO3 và nước. Biết thể tích dung dịch trước và sau phản ứng không thay đổi. Nồng độ mol của muối K2CO3 thu được sau phản ứng là
A.0,2M
B.0,3M
C.0,4M
D.0,5M
nCO2=0,075 mol
CO2 + 2KOH => K2CO3 + H2O
0,075 mol =>0,075 mol
CM dd K2CO3=0,075/0,25=0,3M
Đúng 0
Bình luận (0)
Dấu 4.48 l khí So2 300ml dung dịch cu(oh)2 1m tính nồng độ mol của các chất trong dung dịch sau phản ứng biết thể tích dung dịch ko thay đổi
Cho 1,68 lít CO2 (đktc) sục vào bình đựng 250 ml dung dịch KOH dư. Biết thể tích dung dịch sau phản ứng không thay đổi. Nồng độ mol/lít của muối thu được là bao nhiêu
$2KOH + CO_2 \to K_2CO_3 + H_2O$
$n_{K_2CO_3} = n_{CO_2} = \dfrac{1,68}{22,4} = 0,075(mol)$
$V_{dd} = V_{dd\ KOH} = 0,25(lít)$
$C_{M_{K_2CO_3}} = \dfrac{0,075}{0,25} = 0,3M$
Đúng 3
Bình luận (0)
nCO2=0,075(mol)
PTHH: CO2 + 2 KOH -> K2CO3 + H2O
Vddmuoi= VddKOH=0,25(l)
=> nK2CO3=nCO2=0,075(mol)
=>CMddK2CO3=0,075/0,25=0,3(M)
Đúng 0
Bình luận (0)
Cho 1,68 lít
C
O
2
(đktc) sục vào bình đựng 250 ml dung dịch KOH dư. Biết thể tích dung dịch trước và sau phản ứng không thay đổi Nồng độ mol/lit của muối thu được sau phản ứng là A. 0,2M B. 0,3M C. 0,4M D. 0,5M
Đọc tiếp
Cho 1,68 lít C O 2 (đktc) sục vào bình đựng 250 ml dung dịch KOH dư. Biết thể tích dung dịch trước và sau phản ứng không thay đổi Nồng độ mol/lit của muối thu được sau phản ứng là
A. 0,2M
B. 0,3M
C. 0,4M
D. 0,5M
Chọn B
n C O 2 = 0,075 mol
Vì KOH dư nên phản ứng tạo ra muối trung hòa
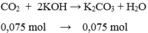
Vì thể tích dung dịch trước và sau không thay đổi

Đúng 1
Bình luận (0)
dẫn từ từ 6,72 lít khí so2 (đktc) vào một dung dịch có hoà tan 44,8g KOH. a) Xác định các chất có trong dung dịch sau phản ứng. b)Hãy tính khối lượng các chất thu được sau phản ứng
a)
$n_{KOH} = \dfrac{44,8}{56} = 0,8(mol)$
$n_{SO_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
Ta thấy : $n_{KOH} : n_{SO_2} = 0,8 : 0,3 = 2,67 > 2$ nên dung dịch sau phản ứng có : $KOH$ dư ; $K_2SO_3$
b)
$n_{K_2SO_3} = n_{SO_2} = 0,3(mol)$
$\Rightarrow m_{K_2SO_3} = 0,3.158 = 47,4(gam)$
$n_{KOH\ dư} = 0,8 - 0,3.2 = 0,2(mol)$
$\Rightarrow m_{KOH\ dư} = 0,2.56 = 11,2(gam)$
Đúng 4
Bình luận (0)
dẫn từ từ 13,44 lít khí so2 (đktc) vào một dung dịch có hoà tan 44,8g KOH. a) Xác định các chất có trong dung dịch sau phản ứng. b)Hãy tính khối lượng các chất thu được sau phản ứng
a, Ta có: \(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{KOH}=\dfrac{44,8}{56}=0,8\left(mol\right)\)
\(\Rightarrow\dfrac{n_{KOH}}{n_{SO_2}}=1,3333\)
⇒ Dd sau pư gồm: K2SO3 và KHSO3.
b, PT: \(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
\(SO_2+KOH\rightarrow KHSO_3\)
Giả sử: \(\left\{{}\begin{matrix}n_{K_2SO_3}=x\left(mol\right)\\n_{KHSO_3}=y\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}x+y=0,6\\2x+y=0,8\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{K_2SO_3}=0,2.158=31,6\left(g\right)\\m_{KHSO_3}=0,4.120=48\left(g\right)\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)






















