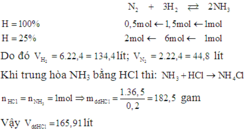Dung dịch chứa NaBr với hàm lượng 40g/l. Cần bao nhiêu lít khí Clo (đktc) và bao nhiêu gam dung dịch đó để điều chế 3 lít Brom lỏng (D=3,,25Kg/l)

Những câu hỏi liên quan
. Cần bao nhiêu gam KMnO4 và bao nhiêu lít dung dịch axit HCl 1M để điều chế được 11,2 lít khí clo (ở đktc)?
cần bao nhiêu gam kmno4 và bao nhiêu ml dung dịch axit HCL 1M để điều chế được 11,2 lít khí Clo ở(đktc)?
\(n_{Cl_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(2KMnO_4+16HCl_{\left(đ\right)}\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.2...................1.6...........................................0.5\)
\(m_{KMnO_4}=0.2\cdot158=31.6\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{1.6}{1}=1.6\left(l\right)=1600\left(ml\right)\)
Đúng 0
Bình luận (0)
\(n_{Cl_2}=\dfrac{11,2}{22,4}=0,5(mol)\\ PTHH:2KMnO_4+16HCl\to 2KCl+2MnCl_2+5Cl_2+8H_2O\\ \Rightarrow n_{KMnO_4}=\dfrac{2}{5}n_{Cl_2}=0,2(mol);n_{HCl}=\dfrac{16}{5}n_{Cl_2}=1,6(mol)\\ \Rightarrow m_{KMnO_4}=0,2.158=31,6(g);V_{dd_{HCl}}=\dfrac{1,6}{1}=1,6(l)=1600(ml)\)
Đúng 0
Bình luận (0)
Một quả bóng bay nhỏ, bơm căng chứa 1,68 lít khí hiđro H2 (ở đktc). Vậy nếu dùng nhôm Al và dung dịch axit clo hiđric HCl 7,3% điều chế khí H2 để bơm vào 10 quả bóng bay như trên thì cần tối thiểu: a. bao nhiêu gam nhôm Al? b. bao nhiêu gam dung dịch axit clo hiđric HCl 7,3%? Biết phản ứng xảy ra hoàn toàn. ( H = 1; Al = 27, Cl = 35,5)
2Al+6HCl->2AlCl3+3H2
0,5----1,5-------------------------0,75
n H2=0,075 mol
cần 10 quả bóng =>0,075.10=0,75 mol
=>mAl=0,5.27=13,5g
m HCl=1,5.36,5=54,75g
=>m dd=75g
Đúng 1
Bình luận (1)
\(n_{H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\\
pthh:2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,1125 0,15 0,075
\(m_{Al}=0,1125.27=3,0375\left(g\right)\\
m_{HCl}=\dfrac{\left(0,15.36,5\right).100}{7,3}=75\left(g\right)\)
Có thể điều chế bao nhiêu gam axit sunfuric khi cho 240g SO4 tác dụng với nước?
Đốt cháy hỗn hợp khí gồm 1,12 lít khí hidro và 1,68 khí oxi (đktc) tính khối lượng nước và thể tích nước ( trạng thái lỏng ) thu được?
Để có một dung dịch chứa 16g NaOH thì cần bao nhiêu gam Na2O cho vào nước?
a)
SO3 + H2O $\to$ H2SO4
n H2SO4 = n SO3 = 240/80 = 3(mol)
m H2SO4 = 3.98 = 294(gam)
b)
2H2 + O2 $\xrightarrow{t^o}$ 2H2O
V H2 / 2 = 0,56 < V O2 = 1,68 nên O2 dư
n H2O = n H2 = 1,12/22,4 = 0,05(mol)
m H2O = 0,05.18 = 0,9(gam)
V H2O = m/D = 0,9/1 = 0,9(ml)
c)
n NaOH = 16/40 = 0,4(mol)
Na2O + H2O $\to$ 2NaOH
n Na2O = 1/2 n NaOH = 0,2(mol)
m Na2O = 0,2.62 = 12,4(gam)
Đúng 3
Bình luận (2)
a)Ta có PT:SO4+H2O=H2SO4
Theo bài ra t có nSO4=240:96=2,5
Mà nSo4=nH2So4=2,5 mol
suy ra:mH2So4=2,5.98=245g
Đúng 1
Bình luận (0)
ta có PT 2H2+O2=2H2O
nH2=1,12:22,4=0,05MOL
nO2=1,68:22.4=0,075mol
theo pt ta có 0,05:2<0,075:1
suy ra H2 hết,O2 dư.
theo PT ta có:nH2O=nH2=0,05mol
suy ra VH2O=.....
mH2O=.....
Đúng 1
Bình luận (0)
Người ta điều chế H2 bằng cách cho Al vào dung dịch NaOH
a) Viết PT phản ứng
b) Tính khối lượng Al để điều chế đc 13,44 lít khí H2 ở đktc
c) Nếu cho 4,86 gam Al vào dung dịch có chứa 8 gam NaOH thì sau phản ứng thu đc bao nhiêu lít khí H2 ở đktc ?
a) PTHH: NaOH + Al + H2O -> NaAlO2 + 3/2 H2
b) nH2= 0,6(mol)
-> nAl=0,4(mol) => mAl=0,4.27=10,8(g)
c) nAl=0,18((mol); nNaOH=0,2(mol)
PTHH: 0,18/1 < 0,2/1
=> Al hết, NaOH dư, tính theo nAl.
-> nH2= 3/2. 0,18=0,27(mol)
=>V(H2,đktc)=0,27.22,4= 6,048(l)
Đúng 1
Bình luận (0)
\(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
\(2NaOH+2Al+2H_2O\rightarrow2NaAlO_2+3H_2\)
\(...........0.4.........................0.6\)
\(m_{Al}=0.4\cdot27=10.8\left(g\right)\)
\(n_{Al}=\dfrac{4.86}{27}=0.18\left(mol\right)\)
\(n_{NaOH}=\dfrac{8}{40}=0.2\left(mol\right)\)
\(2NaOH+2Al+2H_2O\rightarrow2NaAlO_2+3H_2\)
\(2.................2\)
\(0.2...............0.18\)
\(LTL:\dfrac{0.2}{2}>\dfrac{0.18}{2}\)
\(\Rightarrow NaOHdư\)
\(n_{H_2}=0.18\cdot\dfrac{3}{2}=0.27\left(mol\right)\)
\(V_{H_2}=0.27\cdot22.4=6.048\left(l\right)\)
Đúng 1
Bình luận (0)
a, PTHH: 2NaOH + 2Al + 2H2O → 2NaAlO2 + 3H2↑
b, nH2=0,6 mol -mAl=10,8 g
c, nAl=0,16(592) mol
nNaOH=0,2 mol
-NaOH hết, Al dư
-VH2=6,72 l
Đúng 2
Bình luận (0)
Từ 5 lít dung dịch H2SO4 0,3M làm bay hơi chỉ để còn lại 3 lít dung dịch (gọi dung dịch X). Phải lấy bao nhiêu ml dung dịch X cho phản ứng đủ với kẽm để điều chế 1,568 lít khí H2 ở đktc?
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{H_2SO_4}=n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\\ n_{H_2SO_4\left(ban.đầu\right)}=5.0,3=1,5\left(mol\right)\\ V_{ddH_2SO_4\left(lấy\right)}=\dfrac{0,07}{1,5}.3=0,14\left(l\right)=140\left(ml\right)\)
Đúng 2
Bình luận (0)
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml? A. 165,91 lít B. 163 lít C. 175,91 lít D. 153 lít
Đọc tiếp
Phải dùng bao nhiêu lít N2 và H2 (đktc) để điều chế 17 gam NH3. Biết hiệu suất chuyển hoán thành NH3 là 25%. Nếu dùng dung dịch HCl 20% (d = 1,1g/ml) để trung hòa lượng NH3 trên thì cần bao nhiêu ml?
A. 165,91 lít
B. 163 lít
C. 175,91 lít
D. 153 lít
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch HCl 1M để điều chế đủ khí Clo tác dụng với Fe tạo nên 16,25 gam FeCl3 ?
Xem chi tiết
\(n_{FeCl_3}=\dfrac{16.25}{162.5}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(......0.15......0.1\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.06...............0.48........................................0.15\)
\(m_{KMnO_4}=0.06\cdot158=9.48\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{0.48}{1}=0.48\left(l\right)=480\left(ml\right)\)
Đúng 3
Bình luận (2)
\(2Fe+ 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = \dfrac{3}{2}.\dfrac{16,25}{162,5} = 0,15(mol)\\ 2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O\\ n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,06(mol)\\ \Rightarrow m_{KMnO_4} = 0,06.158 = 9,48(gam)\\ n_{HCl} = \dfrac{16}{4}n_{Cl_2} = 0,48(mol)\\ \Rightarrow V_{dd\ HCl} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml)\)
Đúng 1
Bình luận (0)
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch axit clohiđric 1M để điều chế khí clo tác dụng với sắt, tạo nên 16,25g FeCl3?
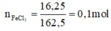
Phương trình hóa học của phản ứng:
3Cl2 + 2Fe → 2FeCl3
Theo pt: 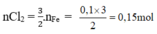
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Theo pt:
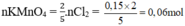
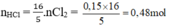
mKMnO4 cần = 0,06. 158 = 9,48g
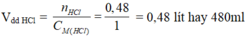
Đúng 0
Bình luận (0)