đốt cháy hoàn toàn 6,72 lít khí c2h2
a, viết phương trình phản ứng xảy ra
b, tính khối lượng và thể tích CO2 thu được
c, cho toàn bộ lượng CO2 thu được đi qua dung dịch Ca(OH)2 dư.Tính khối lượng chất rắn thu được
đốt cháy hoàn toàn 6,72l khí C2H4 ở điều kiện têu chuẩn
a)viết phương trình phản ứng xảy ra.
b)tính khối lượng CO2.
c)cho toàn bộ lượng CO2 thu được đi qua dung dịch Ca(OH)2 dư.tính khối lượng chất rắn thu được .
\(n_{C_2H_4}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(C_2H_4+3O_2\underrightarrow{^{t^0}}2CO_2+2H_2O\)
\(0.3....................0.6\)
\(m_{CO_2}=0.6\cdot44=26.4\left(g\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(n_{CaCO_3}=n_{CO_2}=0.6\left(mol\right)\)
\(m_{CaCO_3}=0.6\cdot100=60\left(g\right)\)
Đốt cháy hoàn toàn 4,48 lít khí C2H4 ở điều kiện tiêu chuẩn. a, viết phương trình phản ứng xảy ra. b, tính khối lượng CO2 thu được sau phản ứng. c, dẫn toàn bộ lượng CO2 thu được đi qua dung dịch CaOH2 dư thu được m gam kết tủa. Tính giá trị của m
a, \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b, \(n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{CO_2}=2n_{C_2H_4}=0,4\left(mol\right)\Rightarrow m_{CO_2}=0,4.44=17,6\left(g\right)\)
c, \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(n_{CaCO_3}=n_{CO_2}=0,4\left(mol\right)\Rightarrow m_{CaCO_3}=0,4.100=40\left(g\right)\)
Câu 1: Đốt cháy hoàn toàn 6,72l khí C2H2
a, viết phương trình pahrn ứng xảy ra
b, tính khối lượng CO2 thu được
c, cho toàn bộ lượng CO2 thu được đi qua dung dịch CH(OH)2 dư. Tính khối lượng chất rắn thu được
Câu 2: hãy xác định công thức của một loại oxit sắt, biết rằng:
a, khi cho 32g oxit sắt này tác dụng hoàn toàn với cacbon oxit thì thu được 22,4g oxit chất rắt, biết khối lượng mol phân tử của oxit sắt là 160g/ mol
b, chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư, tính khối lượng kết tủa thu được.
Câu 1:
a, \(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
b, \(n_{C_2H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{CO_2}=2n_{C_2H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{CO_2}=0,6.44=26,4\left(g\right)\)
c, \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,6\left(mol\right)\Rightarrow m_{CaCO_3}=0,6.100=60\left(g\right)\)
Câu 2:
a, Gọi CTHH cần tìm là FexOy.
Ta có: \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
Mà: mFe + mO = 32 ⇒ mO = 32 - 22,4 = 9,6 (g)
\(\Rightarrow n_O=\dfrac{9,6}{16}=0,6\left(mol\right)\)
⇒ x:y = 0,4:0,6 = 2:3
→ CTHH có dạng (Fe2O3)n
\(\Rightarrow n=\dfrac{160}{56.2+16.3}=1\)
Vậy: Oxit sắt là Fe2O3
b, PT: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=\dfrac{3}{2}n_{Fe}=0,6\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,6.100=60\left(g\right)\)
-Có 3 bình đựng chất khí CO2, CH4, C2H4. Bằng phương pháp hóa học hãy nhận biết ba chất trên. Viết phương trình phản ứng
-Đốt cháy hoàn toàn 6,72 lít khí C2H4
a)Viết phương trình sảy ra
b) Tính khối lượng CO2 thu được
c) Cho toàn bộ lượng CO2 thu được đi qua dung dịch Ca(OH)2 dư. Tính khối lượng chất rắn thu được
- Trích một ít các chất làm mẫu thử:
+ Dẫn các khí qua dd Br2 dư:
* Không hiện tượng: CO2, CH4 (1)
* dd nhạt màu dần: C2H4
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
+ Dẫn các khí còn lại ở (1) qua dd Ca(OH)2 dư:
* Không hiện tượng: CH4
* Kết tủa trắng: CO2
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
-
a) C2H4 + 3O2 --to--> 2CO2 + 2H2O
b) \(n_{C_2H_4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> \(n_{CO_2}=0,6\left(mol\right)\)
=> \(m_{CO_2}=0,6.44=26,4\left(g\right)\)
c)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,6------->0,6
=> \(m_{CaCO_3}=0,6.100=60\left(g\right)\)
Đốt cháy hoàn toàn 9,2 gam rượu etylic nguyên chất ở nhiệt độ cao. a, Viết phương trình phản ứng xảy ra. b, Tính thể tích khí CO2¬ thu được (ở đktc) và khối lượng H2O tạo thành. c, Dẫn sản phẩm thu được đi qua dung dịch nước vôi trong dư. Tính khối lượng kết tủa CaCO3 thu được sau phản ứng.
a) $C_2H_5OH + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
b) $n_{C_2H_5OH} = \dfrac{9,2}{46} = 0,2(mol)$
Theo PTHH :
$n_{CO_2} = 2n_{C_2H_5OH} = 0,4(mol) \Rightarrow V_{CO_2} = 0,4.22,4 = 8,96(lít)$
$n_{H_2O} = 3n_{C_2H_5OH} = 0,6(mol) \Rightarrow m_{H_2O} = 0,6.18 = 10,8(gam)$
c) $CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,4(mol)$
$m_{CaCO_3} = 0,4.100 = 40(gam)$
đốt cháy hòa tan 13,44 lít khí C2H6(ở đktc) a, tính khối lượng CO2 thu được b, cho toàn bộ lượng CO2 thu được đi qua dung dịch Ca(OH)2 dư . tính khối lượng chất rắn thu được
`C_2H_6+(7/2)O_2->2CO_2+3H_2O` (to)
0,6-------------------------1,2 mol
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
1,2--------------------------1,2mol
`n_(C_2H_6)=((13,44)/22.4=0,6 mol`
`=>m_(CO_2)=1,2.44=52,8g`
=>`m_(CaCO_3)=1,2.100=12g`
Đốt cháy hoàn toàn 11,2 lít khí Metan (CH4).
a. Viết phương trình phản ứng xảy ra
b. Tính thể tích Oxi cần dùng để đốt cháy lượng khí trên?
c. Dẫn toàn bộ khí sinh ra qua dung dịch nước vôi trong Ca(OH)2 dư thì thu được bao nhiêu gam kết tủa?
Thể tích các khí đo ở điều kiện tiêu chuẩn
(Cho biết : C=12; O=16; Ca=40; H=1; Br=80)
a, \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH:
CH4 + 2O2 --to--> CO2 + 2H2O
0,5--->1------------->0,5
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,5----->0,5
b, \(V_{O_2}=1.22,4=22,4\left(l\right)\)
c, \(m_{CaCO_3}=0,5.100=50\left(g\right)\)
\(n_{NaOH}=2.0,03=0,06\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=2.0,02=0,04\left(mol\right)\)
\(n_{CaCO3}=\dfrac{3}{100}=0,03\left(mol\right)\)
Thứ tự các pthh :
\(C+O_2-t^o->CO_2\) (1)
\(CO_2+Ca\left(OH\right)_2-->CaCO_3+H_2O\) (2)
\(CO_2+2NaOH-->Na_2CO_3+H_2O\) (3)
\(CO_2+Na_2CO_3-->2NaHCO_3\) (4)
\(CO_2+CaCO_3-->Ca\left(HCO_3\right)_2\) (5)
Vì \(n_{CaCO3}< n_{Ca\left(OH\right)2}\left(0,03< 0,04\right)\) => Có 2 giá trị của CO2 thỏa mãn
TH1: CO2 thiếu ở pứ 2 => Chỉ xảy ra pứ (1) và (2) => Không có pứ hòa tan kết tủa
Theo pthh (2) : \(n_{CO_2}=n_{CaCO3}=0,03\left(mol\right)\)
Bảo toản C : \(n_C=n_{CO2}=0,03\left(mol\right)\)
=> m = 0,03.12 = 0,36 (g)
TH2 : CO2 dư ở pứ (2) ; (3); (4), đến pứ (5) thì thiếu => Có pứ hòa tan kết tủa
Xét pứ (2); (3); (4) ; (5) :
\(\Sigma n_{CO2}=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+n_{Na2CO3}+n_{CaCO3\left(tan\right)}\)
\(=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+\dfrac{1}{2}n_{NaOH}+\left(n_{CaCO3\left(sinh.ra\right)}-n_{CaCO3thu.duoc}\right)\)
\(=n_{Ca\left(OH\right)2}+n_{NaOH}+\left(n_{Ca\left(OH\right)2}-0,03\right)\)
\(=2n_{Ca\left(OH\right)2}+n_{NaOH}-0,03\)
\(=2.0,04+0,06-0,03\)
\(=0,09\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,09\left(mol\right)\)
\(\Rightarrow m=0,09.12=1,08\left(g\right)\)
bạn ơi, bạn sửa cho mình TH2 từ đoạn :
\(n_{CO2}=2.0,04+0,06-0,03=0,11\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,11\left(mol\right)\)
=> mC = 0,11.12 = 1,32 (g)
p/s: sorry nhé, mình tính nhầm số mol co2 nên mới sai
Hỗn hợp khí A gồm C2H2, CH4 và H2. Dẫn m gam hỗn hợp A vào bình kín chứa chất xúc tác Ni, rồi đun nóng. Sau một thời gian thu được hỗn hợp khí B gồm CH4, C2H4, C2H6, C2H2 và H2. Dẫn toàn bộ lượng khí B vào dung dịch brom ( dư) thấy khối lượng bình đựng brom tăng 4,1 gam và thoát ra hỗn hợp khí D. Đốt cháy hoàn toàn D cần dùng 9,52 lít khí O2 (đktc), thu được sản phẩm cháy gồm CO2 và 8,1 gam H2O.
Viết các phương trình phản ứng xảy ra và tính m.
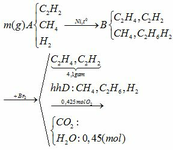
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)