Trong tự nhiên Magie có 2 đồng vị : 24Mg và 25Mg, trong đó Mg24 chiếm 69%.Tính thành phần phần trăm 25Mg trong MgCl2 ( Biết NTKTB của Clo là 35,5)
Giúp e vss ạ . Cảm ơn nhiều
Tính phần trăm khối lượng của đồng vị 24Mg trong MgCl2, biết trong tự nhiên Mg có 2 đồng vị là 24Mg(98%) và 25Mg
\(\overline{NTK}_{Mg}=\dfrac{24.98\%+25.2\%}{100\%}=24,02\left(đ.v.C\right)\\ \%m_{\dfrac{^{24}Mg}{MgCl_2}}=98\%.\dfrac{24,02}{24,02+35,5.2}\approx24,733\%\)
Trong tự nhiên, magnesium có ba đồng vị bền là 24Mg, 25Mg và 26Mg. Đồng vị 26Mg chiếm thành phần phần trăm số nguyên tử là 11%. Biết nguyên tử khối trung bình của Mg là 24,32.
a) Tính thành phần phần trăm số nguyên tử của đồng vị 24Mg.
b) Tính số nguyên tử 26Mg có trong 1 mol MgCl2.
a) Đặt %24Mg là x
-->%25Mg là (100 - x - 11)
\(\overline{M}=\dfrac{x.24+\left(100-x-11\right).25+11.26}{100}=24,32\)
\(\Rightarrow x=\%^{24}Mg=79\%\)
b) ta có : \(n_{Mg}=n_{MgCl2}=1\left(mol\right)\Rightarrow n_{26_{Mg}}=1.11\%=0,11\left(mol\right)\)
Số nguyên tử : \(0,11.6,022.10^{-3}=6,6022.10^{-4}\)(nguyên tử)
Trong tự nhiên magie có 3 đồng vị bền 24Mg chiếm 78,99%, 25Mg chiếm 10,00% và 26Mg. Nguyên tử khối trung bình của Mg là
A. 24,00.
B. 24,11.
C. 24,32.
D. 24,89.
Đáp án C
Nguyên tử khối trung bình của Mg là
MMg = ( 24 . 78 , 99 + 25 . 10 + 26 . 11 , 01 ) / 100 = 24 , 3202
trong tự nhiên, nguyên tố clo có 2 đồng vị là 35Cl và 37Cl. Nguyên tử khối trung bình của Clo bằng 35,5. a) Tính phần trăm số nguyên tử của mỗi đồng vị trên?
b tính % khối lượng của cl35 có trong phân tử HCLO4 biết NTKtb của H+1 o=16,2
Mg có 3 đồng vị 24Mg, 25Mg và 26Mg. Clo có 2 đồng vị 35Cl và 37Cl. Có bao nhiêu loại phân tử MgCl2 khác tạo nên từ các đồng vị của 2 nguyên tố đó ?
A. 6.
B. 9.
C. 12.
D. 10.
Mg có 3 đồng vị 24Mg, 25Mg và 26Mg. Clo có 2 đồng vị 35Cl và 37Cl. Có bao nhiêu loại phân tử MgCl2 khác tạo nên từ các đồng vị của 2 nguyên tố đó
A. 6
B. 9
C. 12
D. 10
Nguyên tử Mg có ba đồng vị ứng với thành phần phần trăm về số nguyên tử như sau :
Đồng vị 24Mg 25Mg 26Mg
% 78,6 10,1 11,3
a. Tính nguyên tử khối trung bình của Mg.
b. Giả sử trong hỗn hợp nói trên có 50 nguyên tử 25Mg , thì số nguyên tử tương ứng của hai đồng vị còn lại là bao nhiêu ?
a, Ta có : \(A=78,6\)%\(.24+10,1\)%.\(25+11,3\)%.\(26=24,327\)
b, \(24Mg\) 25Mg 26Mg
78,6% 10,1% 11,3%
\(x\) <--- 25 nguyên tử <-- \(y\)
Nhân chéo : \(x=\dfrac{25.78,6}{10} = 196,5 \) nguyên tử
\(y=\dfrac{25.11,3}{10} ≈28 \) nguyên tử
Mg có 3 đồng vị bền: 24Mg ( chiếm 79,4%); 25Mg ( chiếm 9,2%) còn lại là đồng vị 26Mg.
a. Tính nguyên tử khối trung bình của Mg.
b. Hỏi mỗi khi có 460 nguyên tử đồng vị 25Mg thì có bao nhiêu nguyên tử 24Mg, bao nhiêu nguyên tử 26Mg?
Trong tự nhiên đồng vị C 37 l chiếm 24,23% số nguyên tử clo. Nguyên tử khối trung bình của clo bằng 35,5. Thành phần phần trăm về khối lượng của C 37 l có trong HClO4 là (với H 1 , O 16 ):
A. 9,82%.
B. 8,65%.
C. 8,56%
D. 8,92%
Phần trăm khối lượng của C 37 l trong HClO4 là:
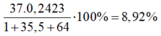
Đáp án D