Nhiệt phân hoàn toàn 27,3 gam hỗn hợp rắn X gồm NaNO3 và Ca(NO3)2 thu được hỗn hợp khí 6,72 lít (đktc)
1 viết phương trình hóa học các phản ứng xảy ra
2 tính thành phần trăm về khối lượng của mối muối trong hỗn hợp x
Nhiệt phân hoàn toàn 27,3 g một hỗn hợp rắn X gồm N a N O 3 và C u ( N O 3 ) 2 , thu được hỗn hợp khí có thể tích 6,72 lít (đktc).
1. Viết phương trình hoá học của các phản ứng xảy ra.
2. Tính thành phần % về khối lượng của mỗi muối trong hỗn hợp X.
1. Phương trình hoá học của các phản ứng:
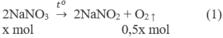
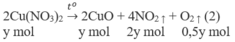
2. Đặt X và y là số mol của N a N O 3 và C u ( N O 3 ) 2 trong hỗn hợp X. Theo các phản ứng (1) và (2) số mol NO2 thu được là 2y mol và tổng số mol oxi là (0,5x + 0,5y) mol.
Biết khối lượng mol của hai chất N a N O 3 và Cu(NO3)2 tương ứng là 85 và 188 (g/mol), ta có hệ phương trình :
85x + 188y = 27,3 (a)
0,5x + 2y + 0,5y = 0,3 (b)
Giải hệ phương trình (a), (b) được : x = y = 0,1.
Phần trăm khối lượng của mỗi muối trong hỗn hợp X :
![]()
% m C u ( N O 3 ) 2 = 100% - 31,1% = 68,9%
Nhiệt phân hoàn toàn hỗn hợp gồm NaNO3; Al(NO3)3; Cu(NO3)2, thu được 10 gam chất rắn Y và hỗn hợp khí. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí (đktc) duy nhất thoát ra. Phần trăm khối lượng của NaNO3 trong hỗn hợp X là
A. 21,25%
B. 42,5%
C. 17,49%
D. 8,75%
Nhiệt phân hoàn toàn hỗn hợp X gồm NaNO3; Al(NO3)2; Cu(NO3)2 thu được 10 gam chất rắn Y và hỗn hợp khí Z. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí duy nhất thoát ra (đktc). Phần trăm khối lượng của NaNO3 trong hỗn hợp X là
A. 21,25%
B. 17,49%
C. 42,5%
D. 8,75%
Nhiệt phân hoàn toàn hỗn hợp X gồm NaNO3; Al(NO3)3; Cu(NO3)2 thu được 10 gam chất rắn Y và hỗn hợp khí Z. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí duy nhất thoát ra (đktc). Phần trăm khối lượng của NaNO3 trong hỗn hợp X là
A. 21,25%
B. 17,49%
C. 8,75%
D. 42,5%
Nhiệt phân hoàn toàn hỗn hợp X gồm NaNO3; Al(NO3)3; Cu(NO3)2 thu được 10 gam chất rắn Y và hỗn hợp khí Z. Hấp thụ khí Z vào 112,5 gam H2O được dung dịch axit có nồng độ 12,5% và có 0,56 lít một khí duy nhất thoát ra (đktc). Phần trăm khối lượng của NaNO3 trong hỗn hợp X là
A. 21,25%
B. 17,49%
C. 8,75%
D. 42,5%
1. Nhiệt phân hoàn toàn 308,2 gam hỗn hợp A gồm KMnO4 và KClO3 thu được khí B và chất rắn D. Nguyên tố Mangan chiếm 10,69% khối lượng của D. Viết các phương trình hóa học xảy ra và tính thành phần phần trăm theo khối lượng mỗi chất trong A.
2. Một loại đá vôi chứa 80% CaCO3, phần còn lại là tạp chất trơ. Nung a gam đá vôi một thời gian thu được chất rắn có khối lượng bằng 73,6% khối lượng đá vôi trước khi nung. Tính hiệu suất phản ứng (Biết chất rắn trơ không tham gia phản ứng phân hủy).
1)
Gọi số mol KMnO4, KClO3 là a, b (mol)
=> 158a + 122,5b = 308,2 (1)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------------------------->0,5a
2KClO3 --to--> 2KCl + 3O2
b------------------>1,5b
=> mO2 = (0,5a + 1,5b).32 = 16a + 48b (g)
mD = 308,2 - 16a - 48b(g)
\(m_{Mn}=\dfrac{\left(308,2-16a-48b\right).10,69}{100}=32,94658-1,7104a-5,1312b\left(g\right)\)
=> \(n_{Mn}=\dfrac{32,94658-1,7104a-5,1312b}{55}=0,6-\dfrac{1069}{34375}a-\dfrac{3207}{34375}\left(mol\right)\)
Mà \(n_{Mn}=n_{KMnO_4}=a\left(mol\right)\)
=> \(\dfrac{35444}{34375}a+\dfrac{3207}{34375}b=0,6\) (2)
(1)(2) => a = 0,4 (mol); b = 2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KMnO_4}=\dfrac{0,4.158}{308,2}.100\%=20,506\%\\\%m_{KClO_3}=\dfrac{2.122,5}{308,2}.100\%=79,494\%\end{matrix}\right.\)
2)
Giả sử nung 100 (g) đá vôi
=> \(m_{CaCO_3\left(bđ\right)}=\dfrac{80.100}{100}=80\left(g\right)\)
\(m_{rắn.sau.pư}=\dfrac{100.73,6}{100}=73,6\left(g\right)\)
=> mCO2 = 100 - 73,6 = 26,4 (g)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
0,6<----------------0,6
=> mCaCO3(pư) = 0,6.100 = 60 (g)
\(H\%=\dfrac{60}{80}.100\%=75\%\)
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy ra hoàn toàn.
Xác định kim loại M và tính thành phần phần trăm theo khối lượng của các chất có trong hỗn hợp X.
Bài 2.2. Hòa tan 25.95 gam hỗn hợp X gồm Zn và ZnO trong dung dịch HCl xảy ra hoàn toàn, thu được 3,36 lít khí (dktc). a. Viết phương trình hóa học của phản ứng xảy ra. b. Tỉnh thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp X. c.Tính khối lượng dung dịch HCI 12% đã dùng
\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ ZnO+2HCl\to ZnCl_2+H_2O\\ b,n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow n_{Zn}=0,15(mol)\Rightarrow m_{Zn}=0,15.65=9,75(g)\\ \Rightarrow \%_{Zn}=\dfrac{9,75}{25,95}.100\%=37,57\%\\ \Rightarrow \%_{ZnO}=(100-37,57)\%=62,43\%\\ c,n_{ZnO}=\dfrac{25,95-9,75}{81}=0,2(mol)\\ \Rightarrow n_{HCl}=2.0,15+2.0,2=0,7(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{0,7.36,5}{12\%}=212,92(g)\)
Cho 48,165 gam hỗn hợp X gồm NaNO3, Fe3O4, Fe(NO3)2 và Al tan hoàn toàn trong dung dịch chứa 1,68 mol KHSO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y chỉ chứa 259, 525 gam muối sunfat trung hòa và 3,136 lít hỗn hợp khí Z (đktc) gồm 2 khí trong đó có một khí hóa nâu trong không khí. Biết tỉ khối của Z so với He là 5,5. Phần trăm khối lượng của Al trong X có giá trị gần nhất với trị nào sau đây? Giả sử sự phân li của HSO4- thành ion coi là hoàn toàn.
A. 13,7.
B. 13,5.
C. 13,3.
D. 14,0.
Đáp án A
Khí gồm NO x mol và H2 y mol
x+y=0,14
30x+2y=5,5.4.0,14
=>x=0,1; y=0,04
BTKL: mH2O=mX+mKHSO4--(m muối+mNO+mH2)
=>mH2O=48,165+1,68.136-(259,525+0,1.30+0,04.2)=14,04 gam=>nH2O=0,78 mol
BTNT H: nHSO4-=4nNH4+ +2nH2 + 2nH2O=>nNH4+=0,01 mol
nH+=4nNO+2nH2+10nNH4+ + 2nO
=>nO=0,55 mol=>nFe3O4=0,1375 mol
BT e: 3nAl=3nNO+2nH2+8nNH4++2nFe3O4
=>nAl=0,245 mol
=>%mAl=13,7%