hòa tan 2,16 (g) Al vào trong dd HNO3 1M thu được 1.232 (l) hỗn hợp khí A gồm NO và N2O (đktc) tính tỉ khối A so với H2 ( không có sản phẩm khí nào khác )

Những câu hỏi liên quan
Hòa tan hoàn toàn 4,48 gam bột sắt vào lượng dư axit HNO3 thu được V lít khí (đktc) hỗn hợp khí gồm N2O và N2, không có sản phẩm khử khác. Tỉ khối của A so với H2 là 18,45. Viết ptpư, tính V
Gọi số mol N2O, N2 là a, b (mol)
Có: \(\overline{M}_A=\dfrac{44a+28b}{a+b}=18,45.2=36,9\left(g/mol\right)\)
=> 7,1a = 8,9b (1)
PTHH: 8Fe + 30HNO3 --> 8Fe(NO3)3 + 3N2O + 15H2O
\(\dfrac{8}{3}a\)<-------------------------------a
10Fe + 36HNO3 --> 10Fe(NO3)3 + 3N2 + 18H2O
\(\dfrac{10}{3}b\)<------------------------------b
=> \(\dfrac{8}{3}a+\dfrac{10}{3}b=\dfrac{4,48}{22,4}=0,2\) (2)
(1)(2) => \(\left\{{}\begin{matrix}a=\dfrac{89}{2370}\left(mol\right)\\b=\dfrac{71}{2370}\left(mol\right)\end{matrix}\right.\) => \(V=\left(\dfrac{89}{2370}+\dfrac{71}{2370}\right).22,4=\dfrac{1792}{1185}\left(l\right)\)
Đúng 2
Bình luận (0)
Hòa tan 4,59 gam Al bằng dung dịch HNO3 dư thu được hỗn hợp khí NO và N2O có tỉ khối hơi đối với hiđro bằng 16,75 (ngoài ra không có sản phẩm khử nào khác). Thể tích (đktc) NO và N2O thu được lần lượt là : A. 2,24 lít và 6,72 lít B. 2,016 lít và 0,672 lít C. 0,672 lít và 2,016 lít D. 1,972 lít và 0,448 lít
Đọc tiếp
Hòa tan 4,59 gam Al bằng dung dịch HNO3 dư thu được hỗn hợp khí NO và N2O có tỉ khối hơi đối với hiđro bằng 16,75 (ngoài ra không có sản phẩm khử nào khác). Thể tích (đktc) NO và N2O thu được lần lượt là :
A. 2,24 lít và 6,72 lít
B. 2,016 lít và 0,672 lít
C. 0,672 lít và 2,016 lít
D. 1,972 lít và 0,448 lít
Hòa tan 4,59 gam Al bằng dung dịch
H
N
O
3
dư thu được hỗn hợp khí NO và
N
2
O
có tỉ khối hơi đối với hiđro bằng 16,75 (ngoài ra không có sản phẩm khử nào khác). Thể tích NO và
N
2
O
ở đktc thu được lần lượt là A. 2,24 lít và 6,72 lít. B. 2,016 lít và 0,672 lít. C. 0,672 lít và 2,016 lít. D. 1,972 lít và 0,448 lít.
Đọc tiếp
Hòa tan 4,59 gam Al bằng dung dịch H N O 3 dư thu được hỗn hợp khí NO và N 2 O có tỉ khối hơi đối với hiđro bằng 16,75 (ngoài ra không có sản phẩm khử nào khác). Thể tích NO và N 2 O ở đktc thu được lần lượt là
A. 2,24 lít và 6,72 lít.
B. 2,016 lít và 0,672 lít.
C. 0,672 lít và 2,016 lít.
D. 1,972 lít và 0,448 lít.
Chọn B
Ta có: n A l = 0 , 17 (mol). Gọi = x mol, = y mol
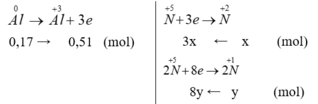
Bảo toàn số mol electron: 3x + 8y = 0,51 (1)
Mặt khác:
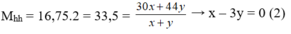
Giải (1) và (2) ta có: x = 0,09 (mol); y = 0,03 (mol)
⇒ V N O = 0 , 09 . 22 , 4 = 2 , 016 ( l ) , V N O 2 0 , 672 ( l )
Đúng 0
Bình luận (0)
Hòa tan m gam Cu vào dung dịch axit HNO3 thu được dung dịch muối Cu(NO3)2 và 3,36 lít hỗn hợp X gồm khí NO và NO2 (ở đktc, không có sản phẩm phụ nào khác). Biết tỉ khối hơi của hỗn hợp X so với khí H2 là 19. Tính khối lượng kim loại m?
Đọc tiếp
Hòa tan m gam Cu vào dung dịch axit HNO3 thu được dung dịch muối Cu(NO3)2 và 3,36 lít hỗn hợp X gồm khí NO và NO2 (ở đktc, không có sản phẩm phụ nào khác). Biết tỉ khối hơi của hỗn hợp X so với khí H2 là 19. Tính khối lượng kim loại m?
Hòa tan hoàn toàn 20,5 gam hỗn hợp Mg, Al, Zn trong dung dịch HNO3 thu được 4,48 lít hỗn hợp khí X gồm NO2, NO, N2O, N2 ở đktc, không có sản phẩm khử nào khác, trong đó NO2 và N2 có cùng số mol. Tỷ khối hơi của X so với H2 là 18,5. Khối lượng muối thu được khi cô cạn dung dịch sau phản ứng là A. 88,7 gam B. 119,7 gam C. 144,5 gam D. 55,7 gam
Đọc tiếp
Hòa tan hoàn toàn 20,5 gam hỗn hợp Mg, Al, Zn trong dung dịch HNO3 thu được 4,48 lít hỗn hợp khí X gồm NO2, NO, N2O, N2 ở đktc, không có sản phẩm khử nào khác, trong đó NO2 và N2 có cùng số mol. Tỷ khối hơi của X so với H2 là 18,5. Khối lượng muối thu được khi cô cạn dung dịch sau phản ứng là
A. 88,7 gam
B. 119,7 gam
C. 144,5 gam
D. 55,7 gam
Hòa tan hết 20,5 gam hỗn hợp Mg, Al, Zn trong dung dịch HNO3 thu được 4,48 lít hỗn hợp khí X gồm NO2, NO, N2O, N2 ở đktc, không còn sản phẩm khử nào khác, trong đó NO2 và N2 có cùng số mol. Tỷ khối hơi của X so với H2 là 18,5. Khối lượng muối thu được khi cô cạn dung dịch sau phản ứng là A.88,7 gam B. 119,7 gam C. 144,5 gam D. 55,7
Đọc tiếp
Hòa tan hết 20,5 gam hỗn hợp Mg, Al, Zn trong dung dịch HNO3 thu được 4,48 lít hỗn hợp khí X gồm NO2, NO, N2O, N2 ở đktc, không còn sản phẩm khử nào khác, trong đó NO2 và N2 có cùng số mol. Tỷ khối hơi của X so với H2 là 18,5. Khối lượng muối thu được khi cô cạn dung dịch sau phản ứng là
A.88,7 gam
B. 119,7 gam
C. 144,5 gam
D. 55,7
Chọn đáp án A
Vì nNO2=nN2 ta tưởng tượng như nhấc 1 O trong NO2 rồi lắp vào N2 như vậy X sẽ chỉ có hai khí là NO và N2O.Khi đó

![]()
=1,1(mol)
![]()
Đúng 0
Bình luận (0)
Cho 0,9 mol Al tan hết trong dung dịch HNO3 dư thu được V lít (đktc) hỗn hợp khí X gồm NO và N2O có tỉ khối hơi so với H2 là 20,25 (sản phẩm khử của N+5 chỉ có NO và N2O). Giá trị của V là A. 13,44. B. 8,96. C. 11,2. D. 6,72.
Đọc tiếp
Cho 0,9 mol Al tan hết trong dung dịch HNO3 dư thu được V lít (đktc) hỗn hợp khí X gồm NO và N2O có tỉ khối hơi so với H2 là 20,25 (sản phẩm khử của N+5 chỉ có NO và N2O). Giá trị của V là
A. 13,44.
B. 8,96.
C. 11,2.
D. 6,72.
Đáp án B
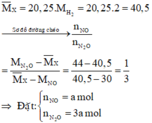
Sơ đồ phản ứng:
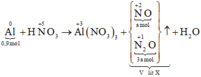
Các quá trình nhường, nhận electron:
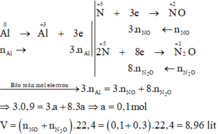
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp A gồm Al, Cu vào 100 ml dungdịch B chứa HNO3 2M và H2SO4 12 M rồi đun nóng thu được dung dịch C và 8,96 lít hỗn hợp khí D (đktc) gồm NO và SO2 (ngoài ra không có sản phẩm khử nào khác), tỉ khối của D so với H2 là 23,5. Tổng khối lượng chất tan trong C là A. 66,2 g. B. 129,6 g. C. 96,8 g. D. 115,2 g.
Đọc tiếp
Cho 18,2 gam hỗn hợp A gồm Al, Cu vào 100 ml dungdịch B chứa HNO3 2M và H2SO4 12 M rồi đun nóng thu được dung dịch C và 8,96 lít hỗn hợp khí D (đktc) gồm NO và SO2 (ngoài ra không có sản phẩm khử nào khác), tỉ khối của D so với H2 là 23,5. Tổng khối lượng chất tan trong C là
A. 66,2 g.
B. 129,6 g.
C. 96,8 g.
D. 115,2 g.
Hòa tan hoàn toàn m gam Al trong dung dịch HNO3 thì thu được 8,96 lít ( ở đktc) hỗn hợp khí A ( gồm NO và N2O) có tỉ khối dA/H2 = 20 . Tính m ?
\(n_{NO}=a\left(mol\right),n_{N_2O}=b\left(mol\right)\)
\(n_{hh}=a+b=\dfrac{8.96}{22.4}=0.4\left(mol\right)\left(1\right)\)
\(M_A=20.2=40\left(\dfrac{g}{mol}\right)\)
\(m_A=30a+44b=40\cdot0.4=16\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=\dfrac{4}{35},b=\dfrac{2}{7}\)
Bảo toàn e :
\(n_{Al}=\dfrac{\dfrac{4}{35}\cdot3+\dfrac{2}{7}\cdot8}{3}=0.87\left(mol\right)\)
\(m_{Al}=23.49\left(g\right)\)
Đúng 0
Bình luận (0)












