Cho 15,35g hổn hợp gồm Fe và Zn vào 250ml dd HNO3 dư thì thu được 4,48l khí NO(đktc) và dd muối X . Nung X đến khối lượng không đổi thu được b gam chất rắn :
a) Tính % khối lượng của từng kim loại
b) Tính giá trị b và nồng độ CM của HNO3
Hòa tan hoàn toàn 12,18 gam hỗn hợp gồm Mg, Fe, Zn trong dung dịch chứa x mol HNO3 và 0,47 mol NaHSO4, thu được 3,584 lít hỗn hợp khí Y gồm H2 và NO ở đktc có khối lượng 2 gam và dung dịch Z chỉ chứa muối trung hòa (trong Z không chứa muối Fe3+). Cho từ từ lượng dung dịch NaOH 1M đến dư thu được kết tủa T. Nung T đến khi khối lượng không đổi thì thu được 8,4 gam chất rắn. Phần trăm khối lượng của Zn trong hỗn hợp ban đầu là :
A. 47,32%
B. 49,47%
C. 53,37%
D. 56,86%
Hòa tan hoàn toàn 33,88 gam hỗn hợp X gồm Fe, Cu, Fe(NO3)2 và CuO (chứa 31,641% là khối lượng của oxi) vào dung dịch chứa 1,02 mol HNO3 (dùng dư), thu được dung dịch Y (không có muối amoni) và 7,76 gam hỗn hợp khí Z gồm NO và NO2. Cho 48 gam NaOH vào Y, thu được 34,58 gam kết tủa và dung dịch T. Cô cạn T và nung chất rắn khan đến khối lượng không đổi, thu được 77,0 gam rắn. Phần trăm số mol của kim loại Fe trong X gần nhất với
A. 8%
B. 15%
C. 22%
D. 31%
Chọn đáp án B
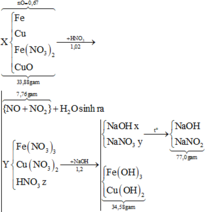
Ta có: 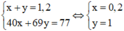
đặt z là nHNO3 dư, BTNT.H Þ nH2O sinh ra = 0,51 – 0,5z
BTNT.N Þ n N O 3 - trong muối của Y là 1 – z = nOH trong kết tủa
Þm Kim loại = 34,58 – 17x(1-z) gam
BTKL Þ 33,88 + 1,02x63 = 34,58 - 17x(l - z) + z + 62 + 7,76 + (0,51 - 0,5z)xl8 Þ z = 0,18

BTNT.N Þ nFe(NO3)2 = (0,09 + 0,11 + 1 -1,02)/2 = 0,09 Þ nFe = 0,14 - 0,09 = 0,05
Vậy %m Fe trong X ![]()
Cho m gam hỗn hợp X gồm (Zn, Fe) tác dụng hết với dung dịch HNO3 dư thu được ddA và hỗn hợp khí (NO, NO2). Cho dung dịch A tác dụng với dung dịch NaOH dư, thu được chất rắn B, nung chất rắn B trong chân không đến khối lượng không đổi được 16 gam chất rắn C. Khối lượng của Fe trong hỗn hợp X là
C là Fe2O3
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
=> nFe = 0,2 (mol)
=> mFe = 0,2.56 = 11,2 (g)
Hoà tan m gam hỗn hợp gồm 2 kim loại là Al và Fe trong dung dịch HCl dư thu được dd B và 14,56 lít H2 đktc . Cho dd B tác dụng với dd NaOH dư , kết tủa đem nung ngoài kk đến khối lượng không đổi được 16 gam chất rắn . Tính m
Cho 67 gam hỗn hợp X gồm Fe3O4 và kim loại A vào dung dịch HNO3 đến khi phản ứng kết thúc thu được 2,24 lít khí NO là sản phẩm khử duy nhất của nitơ (ở đktc), dung dịch Y và 13 gam kim loại A. Cho NH3 dư vào dung dịch Y thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi thu được 36 gam chất rắn. Kim loại A là:
A. Ag
B. Zn
C. Ni
D. Cu
Định hướng tư duy giải :
+ Các đáp đều cho các kim loại có khả năng tạo phức tan trong NH3.
Do đó, có ngay

Chú ý : Ta xem Cu làm hai nhiệm vụ là đẩy Fe3+ về Fe2+ và tạo ra NO.
Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và V lit (đktc) hỗn hợp khí B (gồm hai chất khí có tỉ lệ số mol 3:2). Cho 500 ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là
A. 12,20%
B. 13,56%
C. 20,20%
D. 40,69%.
Đáp án : B
Vì kim loại tan hết nên HNO3 dư
Khi X + KOH => thu được kết tủa
+) Giả sử KOH dư => chất rắn 16,0g gồm Fe2O3 ; CuO (*)
Khi đó T gồm KNO3 và KOH => Nung lên thành KNO2 và KOH với số mol lần lượt là x và y
=> 41,05 = 85x + 56y
Và nK = 0,5 = x + y
=> x = 0,45 mol ; y = 0,05 mol
Gọi số mol Fe và Cu trong A lần lượt là a và b mol
=> 56a + 64b = 11,6g
Và 80a + 80b = 16g (*)
=> a = 0,15 mol ; b = 0,05 mol
+) Nếu chỉ có Fe3+ và Cu2+ => nKOH < 3nFe + 2nCu ( Vô lí )
=> Trong X có Fe2+ : u mol và Fe3+ : v mol
=> HNO3 phải hết
=> u + v = 0 , 15 2 u + 3 v = 0 , 45 => u = 0 , 1 v = 0 , 05
Có nFe(NO3)3 = 0,05 mol
Ta thấy mN2 < mB < mNO2
=> 0,35.28 < mB < 46.0,7
=> 9,8 < mB < 32,2g
BTKL : 66,9g < mdd sau < 89,3g
=> 13,55% < %mFe(NO3)3 < 18,09%
Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4% sau khi kim loại tan hết thu được dung dịch X và V lít (đktc) hỗn hợp khí B (gồm hai chất khí có tỉ lệ số mol 3:2). Cho 500 ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là
A. 13,56%.
B. 20,20%.
C. 40,69%.
D. 12,20%.
Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và V lít (đktc) hỗn hợp khí B ( gồm hai chất khí có tỉ lệ số mol 3:2). Cho 500 ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là:
A. 12,20%.
B. 13,56%.
C. 40,69%
D. 20,20%.
Đáp án B
► Giả sử KOH không dư ||⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí!. ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ||⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
● Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g) || 16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16 ||⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
||⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
► nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol ||⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%
Hòa tan 11,6 gam hỗn hợp A gồm Fe và Cu
vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X và V lít (đktc) hỗn hợp khí B ( gồm hai chất khí có tỉ lệ số mol 3:2). Cho 500 ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16,0 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Nồng độ % của Fe(NO3)3 trong X là:
A. 12,20%.
B. 13,56%.
C. 40,69%.
D. 20,20%.
Đáp án B
Giả sử KOH không dư ⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí! ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g)
16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16
⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
-> nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol
⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%