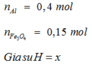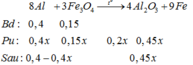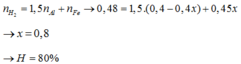Trộn 24 gam Fe2O3 với 10,8 gam Al rồi nung ở nhiệt độ cao, hỗn hợp sau phản ứng hòa tan vào dung dịch NaOH dư thu được 5,376 lít khí ( đktc). Tính hiệu suất của phản ứng nhiệt nhôm.

Những câu hỏi liên quan
Trộn 24g Fe2O3 với 10,8g Al rồi nung ở nhiệt độ cao, hỗn hợp sau phản ứng hòa tan vào dd NaOH dư thu đc 5,376 lít khí (đktc). Hiệu suất của phản ứng nhiệt nhôm là ??
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư) thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là A. 80% B. 90% C. 70% D. 60%
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư) thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là
A. 80%
B. 90%
C. 70%
D. 60%
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là: A. 60%. B. 90%. C. 70%. D. 80%.
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%.
B. 90%.
C. 70%.
D. 80%.
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là: A. 60%. B. 90%. C. 70%. D. 80%.
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư), thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là:
A. 60%.
B. 90%.
C. 70%.
D. 80%.
Giải thích:
nAl = 0,4 mol ; nFe3O4 = 0,15 mol
Giả sử H = x
![]()
Bd: 0,4 0,15
Pu: 0,4x 0,15x 0,2x 0,45x
Sau: 0,4 – 0,4x 0,45x
nH2 = 1,5nAl + nFe → 0,48 = 1,5(0,4 – 0,4x) + 0,45x
→ x = 0,8
→ H = 80%
Đáp án D
Đúng 0
Bình luận (0)
Trộn 10,8 gam bột Al với 34,8 gam bột
F
e
3
O
4
rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch
H
2
S
O
4
loãng (dư), thu được 10,752 lít khí
H
2
(đktc). Tính hiệu suất của phản ứng nhiệt nhôm.
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột F e 3 O 4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H 2 S O 4 loãng (dư), thu được 10,752 lít khí H 2 (đktc). Tính hiệu suất của phản ứng nhiệt nhôm.
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư) thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là A. 80%. B. 90%. C. 70%. D. 60%.
Đọc tiếp
Trộn 10,8 gam bột Al với 34,8 gam bột Fe3O4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hoà tan hoàn toàn hỗn hợp rắn sau phản ứng bằng dung dịch H2SO4 loãng (dư) thu được 10,752 lít khí H2 (đktc). Hiệu suất của phản ứng nhiệt nhôm là
A. 80%.
B. 90%.
C. 70%.
D. 60%.
Đáp án A
![]()
8Al + 3Fe3O4 9Fe + 4Al2O3
![]()
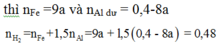
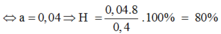
Đáp án A
Đúng 0
Bình luận (0)
Trộn 10,8 gam bột nhôm với 34,8 gam bột
Fe
3
O
4
rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hỗn hợp rắn sau phản ứng bằng dung dịch
H
2
SO
4
loãng dư thu được 10,752 lít
H
2
(đktc). Giả sử
Fe
3
O...
Đọc tiếp
Trộn 10,8 gam bột nhôm với 34,8 gam bột Fe 3 O 4 rồi tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí. Hòa tan hỗn hợp rắn sau phản ứng bằng dung dịch H 2 SO 4 loãng dư thu được 10,752 lít H 2 (đktc). Giả sử Fe 3 O 4 chỉ bị khử thành Fe. Hiệu suất phản ứng nhiệt nhôm là
A. 80%
B. 90%
C. 70%
D. 60%
Hỗn hợp X gồm Al,
F
e
2
O
3
có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí (giả sử chỉ xảy ra phản ứng khử
F
e
2
O
3
thành Fe). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít khí
H...
Đọc tiếp
Hỗn hợp X gồm Al, F e 2 O 3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm trong điều kiện không có không khí (giả sử chỉ xảy ra phản ứng khử F e 2 O 3 thành Fe). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít khí H 2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là:
A. 45%
B. 50%
C. 71,43%
D. 75%
2Al + F e 2 O 3 → A l 2 O 3 + 2Fe
Sau phản ứng cho hỗn hợp rắn tác dụng với dd NaOH thấy có khí thoát ra, suy ra có Al dư.
Vậy hỗn hợp rắn: Fe, A l 2 O 3 , Al (dư) và F e 2 O 3 (nếu dư).
Theo định luật bảo toàn khối lượng, ta có:
m X = m r ắ n tan + m r ắ n k h ô n g tan
= 21,67 - 12,4 = 9,27g
Mà m r ắ n tan = m A l d u + m A l 2 O 3
2Al + 2NaOH + 2 H 2 O
→ 2 N a A l O 2 + 3 H 2 1
Theo PTHH (1), ta có:
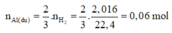
⇒ m A l d u = 0,06.27 = 1,62g
⇒ m A l 2 O 3 p u = m r a n tan - m A l d u
= 9,27-1,62=7,65 g
⇒ n A l 2 O 3 p u = 0,075mol
⇒ n A l p u = n F e s p = 2 n A l 2 O 3 p u
= 0,075.2 = 0,15 mol
Ta có:
m ran khong tan = mFe (sp) = mFe2O3(neu dư)
⇒ m F e 2 O 3 (neu dư)=12,4-0,15.56 = 4g
⇒ n F e 2 O 3 dư = 4/160 = 0,025 mol
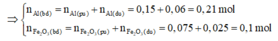
Giả sử phản ứng hoàn toàn thì Al sẽ dư → Tính hiệu suất phản ứng nhiệt nhôm theo F e 2 O 3 .
⇒ H = 0,075.100/0,1 = 75%
⇒ Chọn D.
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí (giả thiết chỉ xảy ra phản ứng Al khử Fe2O3 thành kim loại). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là A. 45% B. 50% C. 80% D. 75%.
Đọc tiếp
Hỗn hợp X gồm Al, Fe2O3 có khối lượng 21,67 gam. Tiến hành phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí (giả thiết chỉ xảy ra phản ứng Al khử Fe2O3 thành kim loại). Hòa tan hỗn hợp chất rắn sau phản ứng bằng dung dịch NaOH dư thu được 2,016 lít H2 (đktc) và 12,4 gam chất rắn không tan. Hiệu suất của phản ứng nhiệt nhôm là
A. 45%
B. 50%
C. 80%
D. 75%.
Gọi nAl=x mol và nFe2O3 = y mol
Fe2O3 + 2Al → Al2O3 + 2Fe
Đầu(mol) y x
Do chất rắn sau +NaOH tạo khí nên dư Al
=> nH2=1,5nAl => 0,06= x-a mX= 160y + 27x = 21,67
m rắn không tan = mFe2O3 + mFe = 160(y – ½ a) + 56a=12,4
Giải hệ : x=0,21mol ; y=0,1mol ; a =0,15mol.
Tính hiệu suất theo Fe2O3 => %H= (0,075/0,1) .100%= 75%
=>D
Đúng 0
Bình luận (0)