Cho 15,06 gam hỗn hợp gồm Fe và kim loại M có hoá trị không đổi . Chia thành hai phần bằng nhau :
Phần 1 : Hoà tan bằng dd HCl dư được 3,696 lít khí H2
Phần 2 : tác dụng với HNO3 loãng thu được 3,36 lít khí NO duy nhất
Xác định kim loại M ?
Hỗn hợp X gồm Fe và Kim loại R ( hoá trị không đổi ) Chia 18,88 g hỗn hợp X thành 2 phần bằng nhau
Phần 1 : cho vào dd Hcl dư thu được 2,24 l khí (đktc)
Phần 2: Tác dụng hết với HNO3 loãng thu được 3,136 l khí NO duy nhất (đktc)
Xác định R
sao ra đc Cu vậy bạn
trả lời liều vừa thui bài này sai đề bài rồi vì lúc giải gệ phương trình ra âm mà
Xin lỗi nha! Mik đang lơ tơ mơ về môn hóa nên tính lộn
Chia m gam hỗn hợp 2 kim loại X và Y có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 hoà tan hết trong dung dịch H2SO4 loãng thu được 1,792 lít khí H2 (đktc). Phần 2 nung trong oxi đến khối lượng không đổi thu được 2,84 gam hỗn hợp oxit. Giá trị của m là:
A. 1,56 gam.
B. 2,20 gam.
C. 3,12 gam.
D. 4,40gam.
Chia m gam hỗn hợp 2 kim loại X và Y có hoá trị không đổi thành 2 phần bằng nhau. Phần 1 hoà tan hết trong dung dịch H2SO4 loãng thu được 1,792 lít khí H2 (đktc). Phần 2 nung trong oxi đến khối lượng không đổi thu được 2,84 gam hỗn hợp oxit. Giá trị của m là:
A. 1,56 gam
B. 2,20 gam
C. 3,12 gam
D. 4,40gam
Chia hỗn hợp gồm 2 kim loại X, Y có hoá trị không đổi thành 2 phần bằng nhau:
+ Phần 1: Hoà tan hoàn toàn trong dung dịch hỗn hợp gồm HCl và H2SO4 được 3,36 lít H2 (đktc).
+ Phần 2: Hoà tan hoàn toàn trong dung dịch HNO3 thu được V lít NO duy nhất (đktc). Giá trị của V là:
A. 2,24 lít.
B. 3,36 lít.
C. 4,48 lít.
D. 5,60 lít.
Đáp án A
Vì hai kim loại X, Y đều có hóa trị không đổi và khối lượng hai phần bằng nhau nên ở hai phần, số mol electron mà kim loại nhường bằng nhau.
Khi đó
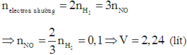
Chia 2m gam hỗn hợp X gồm hai kim loại có hoá trị không đổi thành 2 phần bằng nhau. Cho phần 1 tan hết trong dung dịch HCl (dư) thu được 2,688 lít H2. Nung nóng phần 2 trong oxi (dư) thu được 4,26 gam hỗn hợp oxit. Giá trị của m là
A. 4,68
B. 1,17
C. 3,51
D. 2,34.
Chọn đáp án D
BTE Þ nO = nH2 Þ m = mOxit - mO = 4,26 - 0,12x16 = 2,34
Chia m gam hỗn hợp X gồm hai kim loại Cu, Fe thành hai phần bằng nhau.
Phần 1: Tác dụng hoàn toàn với HNO 3 đặc, nguội thu được 2,24 khí NO 2 (đktc).
Phần 2: Tác dụng hoàn toàn với dung dịch H 2 SO 4 loãng, dư thu được 4,48 lít khí (đktc) Giá trị của m là (Cho Cu = 64; Fe = 56)
A. 4,96.
B. 28,8.
C. 4,16.
D. 17,6.
Chọn B
Phần I. Cho X tác dụng với HNO 3 đặc, nguội chỉ có Cu phản ứng.
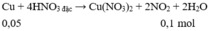
Phần II. Cho X tác dụng với H 2 SO 4 loãng, dư chỉ có Fe phản ứng
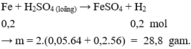
Chia m gam hỗn hợp A gồm hai kim loại Cu, Fe thành hai phần bằng nhau.
- Phần 1: tác dụng hoàn toàn với HNO3 đặc nguội thu được 0,672 lít khí.
- Phần 2: tác dụng hoàn toàn với dung dịch H2SO4 loãng dư thu được 0,448 lít khí.
Giá trị của m là (biết các thể tích khí được đo ở đktc):
A. 4,96 gam.
B. 8,80 gam
C. 4,16 gam.
D. 17,6 gam.
Đáp án C
P1 : Chỉ có Cu phản ứng được với HNO3 đặc nguội
Bảo toàn e : 2nCu = nNO2 = 0,03 mol
P2 : Chỉ có Fe phản ứng với H2SO4 loãng dư
=> nFe = nH2 = 0,02 mol
=> m = 2. (0,015.64 + 0,02.56) = 4,16g
Chia m gam hỗn hợp A gồm hai kim loại Cu, Fe thành hai phần bằng nhau.
- Phần 1: tác dụng hoàn toàn với HNO3 đặc nguội thu được 0,672 lít khí.
- Phần 2: tác dụng hoàn toàn với dung dịch H2SO4 loãng dư thu được 4,48 lít khí.
Giá trị của m là (biết các thể tích khí được đo ở đktc)
A. 4,96 gam
B. 8,80 gam
C. 4,16 gam
D. 17,6 gam
Chọn đáp án C
Phần 1: tác dụng với HNO3 đặc, nguội ⇒ Fe không phản ứng, sản phẩm khử là NO2 (do dùng HNO3 đặc).
⇒ Bảo toàn electron có: 2nCu = nNO2 = 0,03 mol ⇒ nCu = 0,015 mol.
Phần 2: tác dụng với H2SO4 loãng ⇒ Cu không phản ứng, chỉ có Fe phản ứng:
Fe + H2SO4 → FeSO4 + H2↑ ||⇒ nFe = 0,02 mol.
Theo đó, m = 2 × (0,015 × 64 + 0,02 × 56) = 4,16 gam (tránh quên × 2 do chia đôi)
Chia m gam hỗn hợp A gồm hai kim loại Cu, Fe thành hai phần bằng nhau.
- Phần 1: tác dụng hoàn toàn với HNO3 đặc nguội thu được 0,672 lít khí.
- Phần 2: tác dụng hoàn toàn với dung dịch H2SO4 loãng dư thu được 4,48 lít khí.
Giá trị của m là (biết các thể tích khí được đo ở đktc):
A. 4,96 gam
B. 8,80 gam
C. 4,16 gam
D. 17,6 gam
Phần 1: tác dụng với HNO3 đặc, nguội ⇒ Fe không phản ứng, sản phẩm khử của N + 5 là NO2 (do dùng HNO3 đặc).
⇒ Bảo toàn electron có: 2nCu = n NO 2 = 0,03 mol
⇒ nCu = 0,015 mol.
Phần 2: tác dụng với H2SO4 loãng ⇒ Cu không phản ứng, chỉ có Fe phản ứng:
Fe + H2SO4 → FeSO4 + H2↑
⇒ nFe = n H 2 = 0,02 mol.
Theo đó, m = 2 × (0,015 × 64 + 0,02 × 56) = 4,16 gam
Đáp án C