cho 1 mol N2 tác dụng với lượng H2 dư thì thu được 1,5 mol NH3 . Tính hiệu suất của phản ứng

Những câu hỏi liên quan
Cho lượng dư N2 tác dụng với 6,72 lít khí H2(đktc). Biết hiệu suất của phản ứng là 25%, thu được m(gam) NH3. Giá trị của m
$n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$n_{H_2\ pư} = 0,3.25\% = 0,075(mol)$
\(N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3\)
Theo PTHH :
$n_{NH_3} = \dfrac{2}{3}n_{H_2\ pư} = 0,05(mol)$
$m = 0,05.17 = 0,85(gam)$
Đúng 2
Bình luận (0)
Cho lượng dư N2 tác dụng với 10,08 lít khí H2(đktc). Biết hiệu suất của phản ứng là 37%, thu được V lít NH3(đktc). Giá trị của m
$n_{H_2} = \dfrac{10,08}{22,4} = 0,45(mol)$
$n_{H_2\ pư} = 0,45.37\% = 0,1665(mol)$
$N_2 + 3H_2 \buildrel{xt,t^,p}\over\rightleftharpoons 2NH_3$
$n_{NH_3} = \dfrac{3}{2}n_{H_2}= 0,111(mol)$
$V = 0,111.22,4 = 2,4864(lít)$
Đúng 1
Bình luận (0)
Cho V lít (đktc) hỗn hợp N2 và H2 có tỉ lệ mol 1:4 vào bình kín và đun nóng. Sau phản ứng thu được 1,5 mol NH3. Biết hiệu suất phản ứng là H= 25%. Giá trị của V là:
A. 42 lít
B. 268,8 lít
C. 336 lít
D. 448 lít
Đáp án B
![]()
Do 1 1 > 4 3 → Hiệu suất tính theo N 2
Đặt số mol N2 ban đầu là x mol
→ nH2 ban đầu= 4x mol;
Do hiệu suất phản ứng là 25% nên
nN2 pứ= 25%.x= 0,25x mol
![]()
Ban đầu x 4x mol
Phản ứng 0.25x 0.75x 0.5x mol
Sau pứ 0.75x 3.25x 0.5x mol
Sau phản ứng nNH3= 0,5x= 1,5 suy ra x=3 mol
→V= 22,4. (x+3x)= 22,4.4.3=268,8 lít
Đúng 0
Bình luận (0)
Cho V lít (đktc) hỗn hợp khí
N
2
và
H
2
có tỉ lệ mol 1:4 vào bình kín và nung nóng. Sau phản ứng thu được 1,5 mol
NH
3
. Biết hiệu suất phản ứng là H 25%. Giá trị của V là A. 42 lít. B. 268,8 lít. C. 336 lít. D. 448 lít.
Đọc tiếp
Cho V lít (đktc) hỗn hợp khí N 2 và H 2 có tỉ lệ mol 1:4 vào bình kín và nung nóng. Sau phản ứng thu được 1,5 mol NH 3 . Biết hiệu suất phản ứng là H = 25%. Giá trị của V là
A. 42 lít.
B. 268,8 lít.
C. 336 lít.
D. 448 lít.
Chọn C
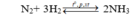
Giả sử phản ứng xảy ra với H = 100% → N 2 hết →Hiệu suất tính theo N 2 .
Đặt số mol N 2 ban đầu là x mol, n N 2 ban đầu = 4x mol;
Do hiệu suất phản ứng là 25% nên n N 2 pứ = 25%.x = 0,25x mol
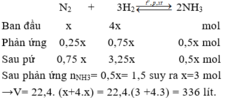
Đúng 1
Bình luận (0)
Cho 0,2 mol N2 tác dụng với 0,6 mol H2 thì thu được 0,6 mol hỗn hợp N2, H2, NH3. Hiệu suất của phản ứng tổng hợp NH3 là:
A.25%
B.75%
C.50%
D.80%
C
N2+3 H2 -> 2 NH3
0.2 0.6 0.4
x 3x 2x
x+3x+2x=0.6
x=0.1
H=(0.1*2)*100/0.4=50%
N2 + 3H2 ⇌ 2NH3
nban đầu 0,2___0,6
np ứng___x——>3x——->2x
nsau pứ. (0,2-x) (0,6-3x) 2x
sau phản ứng thu đc 0,6 mol N2, H2 và NH3
=> (0,2-x)+ (0,6-3x) + 2x = 0,6
=> x = 0,1
=> N2 dư ít hơn H2 (0,1<0,3).
=> Hiệu suất tính theo N2
=> H =0,1/0,2x100% =50%
1. cho 2 mol N2 phản ứng với 6 mol H2 .Tính lượng NH3 thu được biết H% phản ứng là 20%.
2.Tính khối lượng NH3 thu được khi cho 10l N2 tác dụng 35l H2 biết hiệu suất phản ứng là 20% .Các khí đo ở (đkc)?
3. Cho 4L N2 và 14l H2 vào bình phản ứng hỗn hợp khí thu được sau phản ứng có thể tích bằng 16,4l (các khí đo ở cùng điều kiện t°,p ) tính thể tích NH3 sinh ra và hiệu suất phản ứng ?(1,6 lít; 20%)
Đọc tiếp
1. cho 2 mol N2 phản ứng với 6 mol H2 .Tính lượng NH3 thu được biết H% phản ứng là 20%.
2.Tính khối lượng NH3 thu được khi cho 10l N2 tác dụng 35l H2 biết hiệu suất phản ứng là 20% .Các khí đo ở (đkc)?
3. Cho 4L N2 và 14l H2 vào bình phản ứng hỗn hợp khí thu được sau phản ứng có thể tích bằng 16,4l (các khí đo ở cùng điều kiện t°,p ) tính thể tích NH3 sinh ra và hiệu suất phản ứng ?(1,6 lít; 20%)
Câu 1 câu 2 giống nhau nên tui làm câu 1 thôi nha
\(N_2+3H_2\rightarrow2NH_3\)
\(H=20\%\Rightarrow n_{N_2}=2.0,2=0,4\left(mol\right);n_{H_2}=6.0,2=1,2\left(mol\right)\)
=> Tính theo N2
\(\Rightarrow m_{NH_3}=2.n_{N_2}.17=13,6\left(g\right)\)
3/ \(N_2+3H_2\rightarrow2NH_3\)
\(V--3V--2V\)
Thể tích còn lại sau phản ứng bao gồm N2 dư, H2 dư và NH3
\(\Rightarrow V_{N_2}-V+V_{H_2}-3V+2V=16,4\Rightarrow V=0,8\left(l\right)\) \(\Rightarrow V_{NH_3}=2.0,8=1,6\left(l\right)\)
\(\Rightarrow H=\frac{V}{V_{N_2}}=\frac{0,8}{4}=20\%\)
Đúng 0
Bình luận (0)
cho 1,86g hỗn hợp kim loại Mg và Al vào dung dịch HNO3 loãng , dư thì thu được 560ml khí N2O (đktc)
a. Viết phương trình phản ứng xảy ra
b. Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
bài 5: trong công nghiệp người ta điều chế nh3; bằng phản ứng sau n₂ + 3h₂⇌ 2nh3a) tính khối nh3 thu được nếu cho 224 lit khí n2 (đktc) tác dụng với một lượng dư h2. biết hiệu suất phản ứng là 45%.b) tính khối lượng h, và khối lượng nợ cần để điều chế được 17 kg nh3, biết hiệu suất phản ứng là 40%.c) cho 448 lit nz tác dụng với 448 lit hz sẽ thu được bao nhiêu kg nh3, biết hiệu suất phản úng là 39%, thể tích các khí đo ở đktc.d) cho 112 lit khí n2 (đktc) tác dụng với lượng dư h2 thì thu được 168...
Đọc tiếp
bài 5: trong công nghiệp người ta điều chế nh3; bằng phản ứng sau
n₂ + 3h₂\(⇌\) 2nh3
a) tính khối nh3 thu được nếu cho 224 lit khí n2 (đktc) tác dụng với một lượng dư h2. biết hiệu suất phản ứng là 45%.
b) tính khối lượng h, và khối lượng nợ cần để điều chế được 17 kg nh3, biết hiệu suất phản ứng là 40%.
c) cho 448 lit nz tác dụng với 448 lit hz sẽ thu được bao nhiêu kg nh3, biết hiệu suất phản úng là 39%, thể tích các khí đo ở đktc.
d) cho 112 lit khí n2 (đktc) tác dụng với lượng dư h2 thì thu được 168 lit khí nh3 (đktc). tính hiệu suất phản ứng. (cho m: n = 14, h =1 )
Thuỷ phân hỗn hợp gồm 0,02 mol saccarozơ và 0,01 mol mantozơ một thời gian thu được dung dịch X (hiệu suất phản ứng thuỷ phân mội chất đều là 75%). Khi cho toàn bộ X tác dụng với một lượng dư AgNO3 trong NH3 thì lượng Ag thu được là A. 0,090 mol B. 0,12 mol C. 0,095 mol D. 0,06 mol
Đọc tiếp
Thuỷ phân hỗn hợp gồm 0,02 mol saccarozơ và 0,01 mol mantozơ một thời gian thu được dung dịch X (hiệu suất phản ứng thuỷ phân mội chất đều là 75%). Khi cho toàn bộ X tác dụng với một lượng dư AgNO3 trong NH3 thì lượng Ag thu được là
A. 0,090 mol
B. 0,12 mol
C. 0,095 mol
D. 0,06 mol
Đáp án : C
Saccarozo -> Glucozo + Fructozo
0,02.75% -> 0,015 -> 0,015 mol
Mantozo -> 2Glucozo
0,01.75% -> 0,015 mol
Vạy sau thủy phân có : 0,03 mol glucozo ; 0,015 mol fructozo và 0,0025 mol mantozo có thể phản ứng tráng bạc
=> nAg = 2(nGlucozo + nFructozo + nmantozo) = 0,095 mol
Đúng 0
Bình luận (0)
Thuỷ phân hỗn hợp gồm 0,02 mol saccarozơ và 0,01 mol mantozơ một thời gian thu được dung dịch X (hiệu suất phản ứng thủy phân mỗi chất đều là 75%). Khi cho toàn bộ X tác dụng với một lượng dư dung dịch
A
g
N
O
3
trong
N
H
3
thì lượng
A
g
thu được là A. 0,095 mol B. 0,090 mol C. 0,12 mol D. 0,06 mol
Đọc tiếp
Thuỷ phân hỗn hợp gồm 0,02 mol saccarozơ và 0,01 mol mantozơ một thời gian thu được dung dịch X (hiệu suất phản ứng thủy phân mỗi chất đều là 75%). Khi cho toàn bộ X tác dụng với một lượng dư dung dịch A g N O 3 trong N H 3 thì lượng A g thu được là
A. 0,095 mol
B. 0,090 mol
C. 0,12 mol
D. 0,06 mol

















