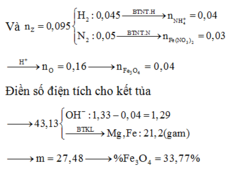
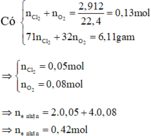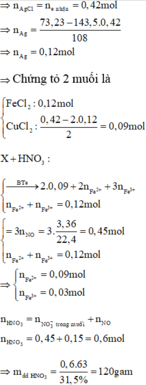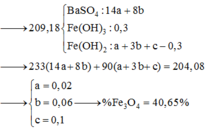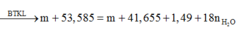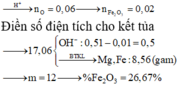hòa tan hết 14,2 gam x gồm fe, mg, fe(no3)2 bằng 100g h2s0o4 15,68% thu dc đ y chứa 23,36 gam hh muối chung hòa và 3,82 gam hh khí z .cho naoh dư vào dd y ,thu được kết tủa T(không có khí bay ra ).nung t trong không khí đến khối lượng không đổi ,thu được 11,6 gam chất rắn . biết các phản ứng xẩy ra hoàn toàn . tính nồng độ phần trăm muối sắt 2