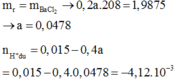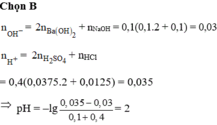Trộn 500ml dung dịch X gồm H2SO4 0.05M với 500ml dung dịch Ba(OH)2 aM. Thu được dung dịch Y có pH =12. Tính giá trị của a

Những câu hỏi liên quan
Trộn 200ml dung dịch Ba(OH)2 aM với 300ml dung dịch H2SO4 có pH1 thu được m gam kết tủa và 500ml dung dịch có pH2. Giá trị của a và m lần lượt là: A. 0,125M và 5,825 gam B. 0,1 M và 4,66 gam C. 0,0625M và 2,9125 gam D. 0,125M và 3,495 gam
Đọc tiếp
Trộn 200ml dung dịch Ba(OH)2 aM với 300ml dung dịch H2SO4 có pH=1 thu được m gam kết tủa và 500ml dung dịch có pH=2. Giá trị của a và m lần lượt là:
A. 0,125M và 5,825 gam
B. 0,1 M và 4,66 gam
C. 0,0625M và 2,9125 gam
D. 0,125M và 3,495 gam
Đáp án C
nBa(OH)2 = 0,2.a mol; nOH-= 0,4a mol
dung dịch H2SO4 có pH = 1 nên [H+] = 10-1 M
→nH+ = [H+].Vdd = 0,3.10-1 = 0,03 mol, nSO4(2-) = 0,015 mol
H2SO4→ 2H++ SO42-
0,03 →0,015 mol
Ba(OH)2→ Ba2++ 2OH-
0,2a→ 0,2a 0,4a
H+ + OH- → H2O
0,4a 0,4a
Dung dịch sau phản ứng có pH = 2 nên axit dư
nH+ dư = 0,03-0,4a
[H+] dư = nH+ dư/ Vdd = (0,03-0,4a)/0,5 = 10-2 suy ra a = 0,0625 M
Ba2++ SO42- → BaSO4
0,0125 0,015 0,0125 mol
mBaSO4 = 2,9125 gam
Đúng 0
Bình luận (0)
Trộn 200ml dung dịch HCl 0,1M và H2SO4 0,05M với 300ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và 500ml dung dịch có pH 13. Vậy a và m có giá trị lần lượt là: A. 0,15M ; 2,33g B. 0,15M ; 10,485g C. 0,3M ; 4,66g D. 0,2M ; 6,99g
Đọc tiếp
Trộn 200ml dung dịch HCl 0,1M và H2SO4 0,05M với 300ml dung dịch Ba(OH)2 aM thu được m gam kết tủa và 500ml dung dịch có pH =13. Vậy a và m có giá trị lần lượt là:
A. 0,15M ; 2,33g
B. 0,15M ; 10,485g
C. 0,3M ; 4,66g
D. 0,2M ; 6,99g
Đáp án A
nH+ = 0,2.0,1 + 0,2.2.0,05 = 0,04
Sau phản ứng thu được 500ml dung dịch có pH =13 ⇒ nOH- lúc sau = 0,05
⇒ nBa =1/2 nOH- ban đầu = 0,045 ⇒ a = 0,045 ÷ 0,3 = 0,15
nH2SO4 = 0,2.0,05 = 0,01< n Ba = 0,045 ⇒ n↓ = n H2SO4 = 0,01 mol
⇒ m↓ = 2,33g
Đáp án A.
Đúng 0
Bình luận (0)
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 a mol/l thu được 500ml dung dịch có pH 12. Giá trị của a là: A. 0,05M B. 0,055M C. 0,075M D.0,5M
Đọc tiếp
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 a mol/l thu được 500ml dung dịch có pH =12. Giá trị của a là:
A. 0,05M
B. 0,055M
C. 0,075M
D.0,5M
Trộn 100ml dung dịch có PH =1 gồm hcl và h2so4 loãng với 100ml dung dịch NAOH aM thu được 200 ml dung dịch 500ml dd co PH=12. Gia trị của a là
DD HCl + H2SO4: pH=1=>[H+]=0,1M => nH+=0,1*0,1=0,01mol
DD NaOH: nOH-=a*0,1 mol
pH sau pứ =12=> môi trường bazo => [OH- dư]=10-2 M=0,01M
=> nOH- dư=0,01*0,2=nOH--nH+
<=>0,002=a*0,1-0,01 => Giải ra a=...
Đúng 1
Bình luận (0)
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
Đọc tiếp
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
![]()
![]()
![]()
![]()
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là A.
2
,
5
.
10
-
3
M
;
13
B.
2
,
5
.
10...
Đọc tiếp
Trộn 300ml dung dịch HCl 0,05M với 200ml dung dịch Ba(OH)2 nồng độ a mol/l thu được 500ml dung dịch có pH = x. Cô cạn dung dịch sau phản ứng thu được 1,9875 gam chất rắn. Giá trị của a và x lần lượt là
A. 2 , 5 . 10 - 3 M ; 13
B. 2 , 5 . 10 - 3 M ; 12
C. 0 , 05 M ; 13
D. 0 , 05 M ; 12
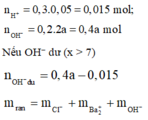
→ 0,015.35,5 + 0,2a.137 + 17(0,4a - 0,015) = 1,9875
→ a = 0,05 M

Đáp án D
Đúng 0
Bình luận (0)
trộn 100ml dung dịch naoh 0.2M với 400ml dung dịch ba(oh)2 0.1 thu được dung dịch a a] tính Ph dung dịch a b]cho 500ml dung dịch hcl 0.3m vào 500ml dung dịch a thu được dung dịch b.tính ph dung dịch b
a, \(n_{OH^-}=0,2.0,1+0,1.2.0,4=0,1\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]=\dfrac{0,1}{0,5}=0,2M\)
\(\Rightarrow\left[H^+\right]=5.10^{-14}M\)
\(\Rightarrow pH\approx13,3\)
Đúng 0
Bình luận (0)
b, \(n_{H^+}=0,15\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=0,05\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,05}{1}=0,05M\)
\(\Rightarrow pH\approx1,3\)
Đúng 0
Bình luận (0)
Trộn V lít dung dịch A gồm HCl 0.75M và H2SO4 0,25M với 2V lít dung dịch B gồm NaOH 0,5M và Ba(OH)2 aM thu được dung dịch C có pH = 7 và một lượng kết tủa.Tính giá trị của V.
Trộn 100 ml dung dịch X (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch Y (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch Z. Giá trị pH của dung dịch Z là: A. 1. B. 2. C. 6. D. 7
Đọc tiếp
Trộn 100 ml dung dịch X (gồm Ba(OH)2 0,1M và NaOH 0,1M) với 400 ml dung dịch Y (gồm H2SO4 0,0375M và HCl 0,0125M) thu được dung dịch Z. Giá trị pH của dung dịch Z là:
A. 1.
B. 2.
C. 6.
D. 7