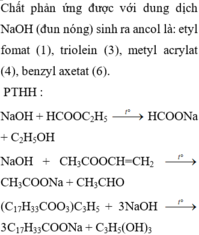
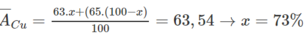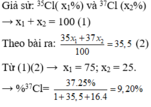Đồng có 2 đồng vị là 2963Cu và 2965Cu , nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm khối lượng của đồng vị 2963Cu trong CuCl2 ( với Clo là đồng vị 1735Cl )

Những câu hỏi liên quan
Câu 1. Nguyên tử khối trung bình của đồng bằng 63,546. Đồng tồn tại trong tự nhiên dưới hai dạng đồng vị 2963Cu và 2965Cu . Tính tỉ lệ % số nguyên tử đồng 2963Cu tồn tại trong tự nhiên.Câu 2: Trong tự nhiên Brom tồn tại chủ yếu dưới hai đồng vị 7935Br và 3581Br . Biết nguyên tử khối trung bình của Brom là 79,9862. Tính phần trăm của đồng vị 7935Br.Loại 2: Cho nguyên tử khối trung bình và số khối của từng đồng vị thứ nhất để tính số khối đồng vị thứ hai. Câu 1: Trong tự nhiên Ag tồn tại chủ yếu...
Đọc tiếp
Câu 1. Nguyên tử khối trung bình của đồng bằng 63,546. Đồng tồn tại trong tự nhiên dưới hai dạng đồng vị 2963Cu và 2965Cu . Tính tỉ lệ % số nguyên tử đồng 2963Cu tồn tại trong tự nhiên.
Câu 2: Trong tự nhiên Brom tồn tại chủ yếu dưới hai đồng vị 7935Br và 3581Br . Biết nguyên tử khối trung bình của Brom là 79,9862. Tính phần trăm của đồng vị 7935Br.
Loại 2: Cho nguyên tử khối trung bình và số khối của từng đồng vị thứ nhất để tính số khối đồng vị thứ hai.
Câu 1: Trong tự nhiên Ag tồn tại chủ yếu dưới dạng hai đồng vị trong đó 107Ag chiếm 56%. Biết nguyên tử khối trung bình của Ag là 107,88. Tính số khối của đồng vị còn lại.
Câu 2: Khối lượng nguyên tử trung bình của antimon là 121,76. Antimon có 2 đồng vị, biết đồng vị 12151Sb chiếm 62%. Tìm số khối của đồng vị thứ 2.
Câu 3: Nguyên tử khối trung bình của nguyên tố R là 79,91; R có 2 đồng vị. Biết 79Z R chiếm
54,5%. Tính nguyên tử khối của đồng vị thứ 2?
Loại 3: Cho số khối và % các đồng vị để tính số khối trung bình.
Câu 1: Cho biết các đồng vị thuộc nguyên tố Argon: 4018Ar (99,63%); 3618 Ar (0,31%); 3818Ar (0,06%). Tính nguyên tử khối trung bình của Ar.
Câu 2: Tính khối lượng nguyên tử trung bình của niken, biết rằng trong tự nhiên, các đồng vị của niken tồn tại như sau:
58
Đồng vị 28Ni 6028Ni 2861Ni 6228Ni 6428Ni
Thành phần % 68,27 26,10 1,13 3,59 0,91 Tính nguyên tử khối trung bình của Ni.
Câu 3: Trong tự nhiên, gali có hai đồng vị là 69 Ga (60,1%) và 71Ga (39,9%). Tính nguyên tử khối trung bình của Ga.
Câu 4: Bo có 2 đồng vị: 105 B (18,89%) và 115 B (81,11%). Nguyên tử khối trung bình của nguyên tố Bo là bao nhiêu?
Câu 5: (vận dụng) Một nguyên tố X gồm hai đồng vị là X1 và X2. Đồng vị X1 có tổng số hạt là 18. Đồng vị X2 có tổng số hạt là 20. Biết rằng % các đồng vị trong X bằng nhau và các loại hạt trong X1 cũng bằng nhau. Tính nguyên tử khối trung bình của X?
Loại 4: Cho số khối của các đồng vị để từ đó thành lập công thức của các hợp chất
Câu 1: Oxi có 3 đồng vị 168 O; 178 O; 188 O và hiđro có hai đồng vị bền là 11H và 21 H. Hỏi có thể có bao nhiêu loại phân tử nước có thành phần đồng vị khác nhau?
Câu 2: Oxi có ba đồng vị là: 168 O; 178 O; 188 O và cacbon có hai đồng vị là: 126 C và 136 C. Hỏi có thể có bao nhiêu loại phân tử khí cacbonic có thành phần đồng vị khác nhau?
Câu 3: Cho hai đồng vị hiđro và hai đồng vị của clo với tỉ lệ phần trăm số nguyên tử chiếm trong tự nhiên như sau: 11H; 21 H và clo: 1735 Cl; 3717 Cl. Có thể có bao nhiêu loại phân tử HCl khác nhau tạo nên từ hai loại đồng vị của hai nguyên tố đó.
Đồng có 2 đồng vị bền là
Cu
29
63
và
Cu
29
65
. Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm của đồng vị . Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm của đồng vị
Đọc tiếp
Đồng có 2 đồng vị bền là Cu 29 63 và Cu 29 65 . Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm của đồng vị . Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm của đồng vị
Đồng có 2 đồng vị là
C
63
u
và
C
65
u
. Khối lượng nguyên tử trung bình của đồng là 63,54. Thành phần phần trăm số nguyên tử của đồng vị
C
65
u
A. 20%. B. 70%. C. 73%. D. 27%
Đọc tiếp
Đồng có 2 đồng vị là C 63 u và C 65 u . Khối lượng nguyên tử trung bình của đồng là 63,54. Thành phần phần trăm số nguyên tử của đồng vị C 65 u
A. 20%.
B. 70%.
C. 73%.
D. 27%
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Thành phần % khối lượng của 63Cu trong CuCl2 là (cho Cl 35,5) A. 12,64%. B. 26,77%. C. 27,00%. D. 34,18%.
Đọc tiếp
Trong tự nhiên đồng có 2 đồng vị là 63Cu và 65Cu. Nguyên tử khối trung bình của đồng là 63,54. Thành phần % khối lượng của 63Cu trong CuCl2 là (cho Cl = 35,5)
A. 12,64%.
B. 26,77%.
C. 27,00%.
D. 34,18%.
Đáp án D
Giả sử % nguyên tử 65Cu và 63Cu trong tự nhiên lần lượt là x, y.
Ta có hpt
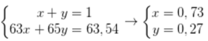
Phần trăm khối lượng của 63Cu trong CuCl2 là
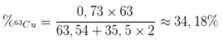
Đúng 0
Bình luận (0)
Đồng có 2 đồng vị : và , nguyên tử khối trung bình của nguyên tố Cu là 63,54.a. Tính phần trăm số nguyên tử của từng đồng vị của nguyên tố Cu.b. Tính phần trăm khối lượng của đồng vị chứa trong CuSO4. ( với O là đồng vị , S là đồng vị )c. Tính số nguyên tử của đồng vị có trong 35,77 gam Cu2O.Câu 10. Viết cấu hình electron của các nguyên tử có phân lớp ngoài cùng là 4s1
Đọc tiếp
Đồng có 2 đồng vị : và , nguyên tử khối trung bình của nguyên tố Cu là 63,54.
a. Tính phần trăm số nguyên tử của từng đồng vị của nguyên tố Cu.
b. Tính phần trăm khối lượng của đồng vị chứa trong CuSO4. ( với O là đồng vị , S là đồng vị )
c. Tính số nguyên tử của đồng vị có trong 35,77 gam Cu2O.
Câu 10. Viết cấu hình electron của các nguyên tử có phân lớp ngoài cùng là 4s1
trong tự nhiên đồng có 2 đồng vị 63cu và 65cu .Nguyên tử khối trung bình của Cu là 63,54. a,Tính phần trăm số nguyên tử mỗi loại đồng vị b.Tính thành phần phần trăm theo khối lượng của 65Cu trong CuSO
a)
Gọi thành phần phần trăm của hai đồng vị 63Cu ,65Cu lần lượt là a,b
Ta có :
a + b = 100%
63a + 65b = 63,54
Suy ra a = 0,73 = 73% ; b = 0,27 = 27%
b) Thành phần phần trăm khối lượng của 65Cu trong CuSO4 là :
\(\dfrac{65.27\%}{63,54 + 32 + 16.4 }.100\% = 11\%\)
Đúng 2
Bình luận (0)
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có hai đồng vị là
C
35
l
và
C
37
l
Thành phần phần trăm về khối lượng của
C
17
35
l
chứa trong
H
C
l
O
4
(với hiđro là đồng vị
H
1...
Đọc tiếp
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có hai đồng vị là C 35 l và C 37 l Thành phần phần trăm về khối lượng của C 17 35 l chứa trong H C l O 4 (với hiđro là đồng vị H 1 1 , oxi là đồng vị O 8 16 ) là
A. 9,40%
B. 8,95%
C. 9,67%
D. 9,20%
Trong tự nhiên, nguyên tố đồng có hai đồng vị là C 29 63 u và C 29 65 u . Nguyên tử khối trung bình của đồng là 63,54. Thành phần phần trăm tổng số nguyên tử của đồng vị là
A. 27%.
B. 50%.
C. 73%.
D. 54%.
Đồng có hai đồng vị bền 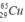 và
và 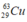 Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị
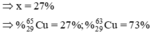
Nguyên tử khối trung bình của đồng là 63,54. Tính thành phần phần trăm số nguyên tử của mỗi đồng vị
Gọi x là thành phần % của đồng vị 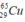
Ta có:
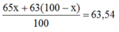
Đúng 0
Bình luận (0)
Đồng có 2 đồng vị bền là: 65Cu , 63Cu . Nguyên tử khối trung bình của đồng là 63,54.
Thành phần phần trăm của đồng vị 65Cu là