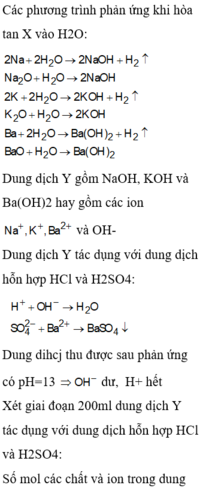
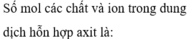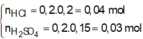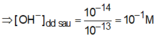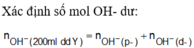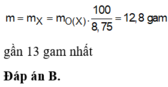Hòa tan hết 1 lượng Na vào dung dịch HCl 10% thu được 46,88g dung dịch gồm NaCl và NaOH và 1,568 lít H2 (đktc). Tính nồng độ % NaCl trong dung dịch

Những câu hỏi liên quan
Hòa tan hết một lượng Na vào dung dịch HCl 10% thu được 46,88 gam dung dịch gồm NaCl và NaOH và 1,568 lít H 2 (đktc). Nồng độ % NaCl trong dung dịch thu được là
A. 14,97
B. 12,48
C. 12,68
D. 15,38
Hòa tan hết một lượng Ma vào dung dịch HCl 10% , thu được 46,88 gam dung dịch gồm NaCl và NaOH và 1,568 lít khí H2(đktc).
Nồng độ % của Nacl trong dung dịch là bn ?
Hòa tan hết một lượng Na vào dung dịch HCl 3,65% thu được 103,3 gam dung dịch gồm NaCl và NaOH và 1,68 lít H 2 (đktc). Nồng độ % NaCl trong dung dịch thu được là
A. 5,66
B. 12,48
C. 6,24
D. 7,84
1. (1,5 điểm) Hòa tan hết 36,1 gam hỗn hợp A gồm Fe và Al vào 200 mL dung dịch HCl (dùng vừa đủ).
Sau phản ứng thu được dung dịch B và 21,28 lít khí H2 (đktc). Hãy tính:
a. Khối lượng mỗi chất trong hỗn hợp A ban đầu.
b. Tính nồng độ dung dịch HCl đã dùng.
c. Tính nồng độ mol/l của chất tan trong dung dịch B.
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a_____2a______a_____a (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
b_____3b_______b_____\(\dfrac{3}{2}\)b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+27b=36,1\\a+\dfrac{3}{2}b=\dfrac{21,28}{22,4}=0,95\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,5\cdot56=28\left(g\right)\\m_{Al}=8,1\left(g\right)\end{matrix}\right.\)
b+c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{HCl}=2a+3b=1,9\left(mol\right)\\n_{FeCl_2}=0,5\left(mol\right)\\n_{AlCl_3}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{1,9}{0,2}=9,5\left(M\right)\\C_{M_{FeCl_2}}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\C_{M_{AlCl_3}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Hòa tan hết m gam hỗn hợp X gồm: Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400ml dung dịch có pH 13. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây? A. 12. B. 14. C. 15. D. 13.
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm: Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400ml dung dịch có pH = 13. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 12.
B. 14.
C. 15.
D. 13.
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200 ml dung dịch Y với 200 ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400 ml dung dịch có pH 13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây? A. 15 B. 14 C. 12 D. 13
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200 ml dung dịch Y với 200 ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400 ml dung dịch có pH = 13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây?
A. 15
B. 14
C. 12
D. 13
Đáp án : D
nH+ = nHCl + 2nH2SO4 = 0,1 mol
Dung dịch sau có pH = 13 => COH- = 0,1M => nOH- = 0,04 mol
=> nOH (Y) = 0,14 mol = ånKL.(số điện tích)
Lại có : 2nH2 = nOH ( do các kim loại tạo ra) = 0,14 mol với 400 ml Y
=> Với 200 ml dung dịch Y có nOH tạo ra do kim loại = 0,07 mol
=> nOH tạo ra do oxit = 0,07 mol = ånKL(oxit).(số điện tích) = 2nO (bảo toàn điện tích)
=> nO = 0,035 mol
Để tạo 400 ml Y thì nO = 0,035.2 = 0,07 mol
=> m = 12,8g
Đúng 0
Bình luận (0)
Hòa tan hết m gam hỗn hợp X gồm:
N
a
,
N
a
2
O
,
K
,
K
2
O
,
B
a
...
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm: N a , N a 2 O , K , K 2 O , B a v à B a O , trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400ml dung dịch Y và 1 , 568 l í t H 2 ( đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm H C l 0 , 2 M v à H 2 S O 4 0 , 15 M thu được 400ml dung dịch có pH = 13. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 12
B. 14
C. 15
D. 13
Đáp án D
Xử lý dữ kiện 200ml dung dịch Y:
![]()
![]()
⇒ n O H - d u = 0 , 4 . 0 , 1 = 0 , 04 m o l
![]()
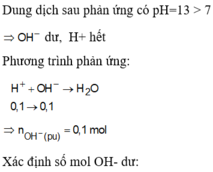
⇒ dung dịch Y chứa 0 , 28 m o l O H -
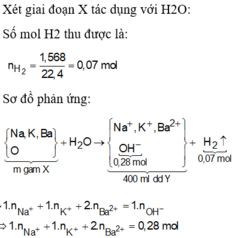
Dễ thấy n O H - = 2 n H 2 + 2 n O / o x i t
![]()
![]()
Đúng 0
Bình luận (0)
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng, vào nước thu được 400ml dung dịch Y và 1,568 lít khí H2 (đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400ml dung dịch có pH13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây? A. 12. B. 13. C. 14. D. 15.
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng, vào nước thu được 400ml dung dịch Y và 1,568 lít khí H2 (đktc). Trộn 200ml dung dịch Y với 200ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400ml dung dịch có pH=13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây?
A. 12.
B. 13.
C. 14.
D. 15.
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng, vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200 ml dung dịch Y với 200 ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400 ml dung dịch có pH 13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây? A. 12. B. 13. C.. 14. D. 15.
Đọc tiếp
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng, vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200 ml dung dịch Y với 200 ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400 ml dung dịch có pH =13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây?
A. 12.
B. 13.
C.. 14.
D. 15.
Chọn B.
Dung dịch sau có pH = 13 nên sau phản ứng còn dư kiềm: nOH-dư = 0,1.0,4 = 0,04 mol.
⇒ n O H - Y = 0,04+0,2.(0,2+0,2.0,15)=0,14 mol
Quy đổi X tương đương với hỗn hợp gồm: Na (x mol), K (y mol), Ba (z mol), O (t mol).
⇒ l6t = 8,75% m.
Theo định luật bảo toàn electron, ta có: x + y + z = 2t + 2 n H 2
⇒ t = (2.0,14 - 2.0,07) : 2 = 0,07 mol ⇒ m = 12,8 ≈ 13 gam.
Đúng 0
Bình luận (0)