Một hỗn hợp gồm 3 đồng vị .đồng vị 1 chứa 12n chiếm 78,6% số nguyên tử .Đồng vị 2 chứa 13n chiếm 10%.Đồng vị 3 chứa 14n .Nguyên tử lượng trung bình của 3 đồng vị này là 24,328u .Tìm số hiệu nguyên tử và viết ký hiệu của mỗi đồng vị

Những câu hỏi liên quan
Một hỗn hợp gồm 3 đồng vị đồng vị ( I ) chứa 12n chiếm 78,6% số nguyên tử. Đồng vị ( II) chứa 13n chiếm 10%. Đồng vị ( III ) chứa 14n. Nguyên tử lượng trung bình của 3 đồng vị này là 24,328. Tìm số hiệu nguyên tử và viết ký hiệu của mỗi đồng vị.
Hh gồm 3 đồng vị . đồng vị 1 chứa 12n Chiếm 78.6% số ngtu . đòng vị 2 chứa 13n chiếm 10% . đồng vị 3 chứa 14n . nguyên tử khối tb của 3 đồng vị là 24,328u. Tìm số hiệu ngtu và viết ký hiệu của một đồng vị
Nguyên tố R có 3 đồng vị .Đồng vị thứ nhất chứa 12 nơtron, chiếm 78,6%.Đồng vị thứ hai chứa 13 nơtron,chiếm 10/5.Đồng vị thứ 3 chứa 14 nơtron, chiếm 11,4% về số nguyên tử.Biết nguyên tử khối trung bình của R là 24,348.Tính số khối mỗi đồng vị và viết kí hiệu mỗi đồng vị
Đọc tiếp
Nguyên tố R có 3 đồng vị .Đồng vị thứ nhất chứa 12 nơtron, chiếm 78,6%.Đồng vị thứ hai chứa 13 nơtron,chiếm 10/5.Đồng vị thứ 3 chứa 14 nơtron, chiếm 11,4% về số nguyên tử.Biết nguyên tử khối trung bình của R là 24,348.Tính số khối mỗi đồng vị và viết kí hiệu mỗi đồng vị
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là: A. 27,28,32. B. 26,27, 34. C. 28,29,30. D. 29,30,28.
Đọc tiếp
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là:
A. 27,28,32.
B. 26,27, 34.
C. 28,29,30.
D. 29,30,28.
Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
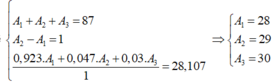
Đúng 0
Bình luận (0)
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là: A. 27,28,32. B. 26,27, 34. C. 28,29,30. D. 29,30,28.
Đọc tiếp
Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số nơtron trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là:
A. 27,28,32.
B. 26,27, 34.
C. 28,29,30.
D. 29,30,28.
Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
Ta có hệ
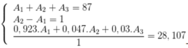
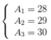
Đúng 0
Bình luận (0)
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là A. 30,56%. B. 29,92%. C. 31,03%. D. 30,55%.
Đọc tiếp
Trong tự nhiên kali gồm 3 đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị 79Br và 81Br với nguyên tử khối trung bình của Br là 79,92. Thành phần % khối lượng của 39K trong KBr là
A. 30,56%.
B. 29,92%.
C. 31,03%.
D. 30,55%.
Đáp án D
%41K = 100 - 93,26 - 0,012 = 6,728%.
Khối lượng nguyên tử trung bình của K là:
MK = 39 x 0,9326 + 40 x 0,00012 + 41 x 0,06728 = 39,13468.
Khối lượng nguyên tử trung bình của Br là:
MBr = 79,92.
Thành phần phần trăm của 39K trong KBr là
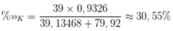
Đúng 0
Bình luận (0)
Nguyên tử khối trung bình của Mg là 24,327. Số khối các đồng vị lần lượt là 24, 25, 26. Phần trăm số nguyên tử của đồng vị 1 là 78,6%. Tìm % số nguyên tử mỗi đồng vị.
Phần trăm đồng vị thứ nhất \(^{24}Mg\) là 78,6%.
Gọi phần trăm đồng vị \(^{25}Mg\) và \(^{26}Mg\) lần lượt là a và b.
\(\Rightarrow\left\{{}\begin{matrix}78,6\%+a\%+b\%=100\%\\24\cdot78,6\%+25\cdot a\%+26\cdot b\%=24,327\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}a=10,1\%\\b=11,3\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Đồng có 2 đồng vị : và , nguyên tử khối trung bình của nguyên tố Cu là 63,54.a. Tính phần trăm số nguyên tử của từng đồng vị của nguyên tố Cu.b. Tính phần trăm khối lượng của đồng vị chứa trong CuSO4. ( với O là đồng vị , S là đồng vị )c. Tính số nguyên tử của đồng vị có trong 35,77 gam Cu2O.Câu 10. Viết cấu hình electron của các nguyên tử có phân lớp ngoài cùng là 4s1
Đọc tiếp
Đồng có 2 đồng vị : và , nguyên tử khối trung bình của nguyên tố Cu là 63,54.
a. Tính phần trăm số nguyên tử của từng đồng vị của nguyên tố Cu.
b. Tính phần trăm khối lượng của đồng vị chứa trong CuSO4. ( với O là đồng vị , S là đồng vị )
c. Tính số nguyên tử của đồng vị có trong 35,77 gam Cu2O.
Câu 10. Viết cấu hình electron của các nguyên tử có phân lớp ngoài cùng là 4s1
Brom trong tự nhiên là hỗn hợp 2 đồng vị: đồng vị 1 có số khối 79 chiếm 50,7% ; đồng vị 2 có số khối 81 chiếm 49,3%. Tính nguyên tử khối trung bình của brom.
Nguyên tử khối trung bình:
\(\overline{A}=\dfrac{50,7\cdot79+49,3\cdot81}{100}=79,986\approx80\)
Đúng 1
Bình luận (1)













