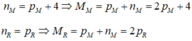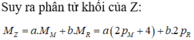Tổng số hạt bằng 126 số nơtron nhiều hơn số proton là 12 hạt .Tìm số lượng mỗi hạt

Những câu hỏi liên quan
Hợp chất Y có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số nơtron nhiều hơn số proton là 4 hạt . Trong hạt nhân X, số nơtron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Tìm AM và AX .
A. 26 và 16 B. 65 và 16 C. 56 và 32 D. 39 và 32
Tìm số lượng mỗi loại hạt cấu tạo nên nguyên tử, biết :
a) Tổng số hạt bằng 126, số nơtron nhiều hơn số proton là 12 hạt
b) Nguyên tử X có tổng số hạt bằng 60, trong đó số hạt nơtron số hạt proton
c) Tổng số hạt trong nguyên tử là 40. Số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt.
d) Nguyên tử của nguyên tố X có tổng số hạt là 28 hạt. Số hạt không mang điện nhiều hơn hạt mang điện tích dương 1 hạt.
e) Tổng số hạt mang điện và số hạt không mang điện là 34, trong đó số hath ma...
Đọc tiếp
Tìm số lượng mỗi loại hạt cấu tạo nên nguyên tử, biết :
a) Tổng số hạt bằng 126, số nơtron nhiều hơn số proton là 12 hạt
b) Nguyên tử X có tổng số hạt bằng 60, trong đó số hạt nơtron = số hạt proton
c) Tổng số hạt trong nguyên tử là 40. Số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt.
d) Nguyên tử của nguyên tố X có tổng số hạt là 28 hạt. Số hạt không mang điện nhiều hơn hạt mang điện tích dương 1 hạt.
e) Tổng số hạt mang điện và số hạt không mang điện là 34, trong đó số hath mang điện gấp 1,833 lần số hạt không mang điện.
f) Nguyên tử của nguyên tố X có tổng số hạt ( p , e , nơtron ) = 180; trong đó tổng số hạt mang điện chiếm 58,59 tổng số hạt. Tìm tên Nguyên tử X
a) \(\left\{{}\begin{matrix}2p+n=126\\p-n=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=e=46\\n=34\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}2p+n=60\\p-n=0\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\)
c)\(\left\{{}\begin{matrix}2p+n=40\\2p-n=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\)
Chúc bạn hok tốt
Đúng 0
Bình luận (0)
Ta có : p+n + e= 126 hay 2p + n =126
Vì số nơtron nhiều hơn số proton là 12 hạt
=> 2p - n = 12
\(\Rightarrow\left\{{}\begin{matrix}2p+n=126\\p-n=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}2p=46\\n=34\end{matrix}\right.hay\left\{{}\begin{matrix}p=e=46\\n=34\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Ta có p+n + e = 60 hay 2p+ n =60
Vì trong đó số hạt nơtron = số hạt proton
=> p -n =0
\(\Rightarrow\left\{{}\begin{matrix}2p+n=60\\p-n=20\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}2p=20\\n=20\end{matrix}\right.hay\left\{{}\begin{matrix}p=e=20\\n=20\end{matrix}\right.\)Còn lại tương tự nhé
Đúng 0
Bình luận (0)
Bài 8: Tổng số hạt proton, nơtron, electron trong 2 nguyên tử kim loại A và B là 142 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 42, số hạt mang điện của B nhiều hơn A là 12. Tính số proton mỗi loại.
p: hạt proton=electron
n: hạt notron
Hạt mang điện của B nhiều hơn A:
Từ 3 phương trình trên:
Đúng 0
Bình luận (2)
I) Toán tìm số hạt đủ dữ kiện.
+ Xác định số hạt p, n, e cấu tạo nên nguyên tử:
1. Tổng số hạt là 34, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
2. Tổng số hạt là 126, số nơtron nhiều hơn số e là 12 hạt.
1) \(\left\{{}\begin{matrix}p+e+n=34\\p+e=n+10\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}2p+n=34\\2p=n+10\end{matrix}\right.\)
\(\Rightarrow2n+10=34\Rightarrow n=12\)
\(\Rightarrow p=e=\dfrac{n+10}{2}=11\)
2) \(\left\{{}\begin{matrix}p+e+n=126\\n=e+12\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}2p+n=126\\n=p+12\end{matrix}\right.\)
\(\Rightarrow3p+12=126\Rightarrow p=38\)
\(\Rightarrow\left\{{}\begin{matrix}e=p=38\\n=p+12=50\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Nguyên tử M có số nơtron nhiều hơn số proton là 1 và số hạt mang điện nhiều hơn số hạt không mang điện là 10.
a) Xác định số proton trong hạt nhân (điện tích hạt nhân) của M.
b) Biết proton và nơtron có cùng khối lượng và bằng 1đvC. Tính khối lượng nguyên tử của X.
c) Vẽ sơ đồ đơn giản của nguyên tử nguyên tố M. X là nguyên tố nào? Kí hiệu hoá học của M.
Nguyên tử M có số notron nhiều hơn số proton là 1 => nM - pM = 1 => - pM+nM=1 (1) Số hạt ko mang điện nhiều hơn số hạt mang điện là 10 => 2pM-nM = 10 (2) Giai (!) (2) suy ra : pM=3 (Li) X là Li. Bài dễ mà bạn :P chi tiết rồi đó
Đúng 0
Bình luận (0)
Tổng số hạt proton Nơtron electron trong hai nguyên tử kim loại a và b là 142 trong số đó hạt mang điện nhiều hơn hạt không mang điện là 42 số hạng mang điện của B nhiều hơn A 12 tính số Proton mỗi loại
Ta có: P = E (Do nguyên tử trung hòa về điện.)
- Tổng số hạt trong A và B là 142.
⇒ 2PA + NA + 2PB + NB = 142 (1)
- Trong đó hạt mang điện nhiều hơn hạt không mang điện là 42.
⇒ 2PA + 2PB - (NA + NB) = 42
⇒ NA + NB = 2PA + 2PB - 42 (2)
Thay (2) vào (1) được 4PA + 4PB = 184 (3)
- Số hạt mang điện của B nhiều hơn A là 12.
⇒ 2PB - 2PA = 12 (4)
Từ (3) và (4) ⇒ PA = 20, PB = 26
Đúng 2
Bình luận (0)
Câu 7: Nguyên tử của một nguyên tố R có tổng số các loại hạt proton, electron, nơtron bằng 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22
hạt. Tìm điện tích hạt nhân của R.
Câu 8: Tổng số các hạt proton, electron, nơtron của một nguyên tử X là 28. Số hạt
mang điện nhiều hơn số hạt không mang điện là 8. Tìm điện tích hạt nhân của X.
Câu 9: Nguyên tử của một nguyên tố X có tổng số các loại hạt proton, electron, nơtron bằng 115. Trong đó số hạt mang điện nhiều hơn số hạt khô...
Đọc tiếp
Câu 7: Nguyên tử của một nguyên tố R có tổng số các loại hạt proton, electron, nơtron bằng 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt. Tìm điện tích hạt nhân của R. Câu 8: Tổng số các hạt proton, electron, nơtron của một nguyên tử X là 28. Số hạt mang điện nhiều hơn số hạt không mang điện là 8. Tìm điện tích hạt nhân của X. Câu 9: Nguyên tử của một nguyên tố X có tổng số các loại hạt proton, electron, nơtron bằng 115. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 25 hạt. Viết kí hiệu nguyên tử của X. Câu 10: Khối lượng của nguyên tử nguyên tố X là 27u. Số hạt không mang điện nhiều hơn số hạt mang điện là dương là 1. Viết kí hiệu nguyên tử của X. Câu 11: Tính nguyên tử khối trung bình của nguyên tố Oxi, biết Oxi có 3 đồng vị : 99,757% 816O; 0,039% 817O; 0,204% 818O
Câu 10: Mỗi phân tử XY, có tổng các hạt proton, nơtron, electron bằng 178; trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 54, số hạt mang điện của X ít hơn số hạt mang điện của Y là 12. Hãy viết kí hiệu nguyên tử của X,Y.
\(\left\{{}\begin{matrix}2P_X+2P_Y+N_X+N_Y=178\\\left(2P_X+2P_Y\right)-\left(N_X+N_Y\right)=54\\2P_Y-2P_X=12\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}2P_X+2P_Y=116\\N_X+N_Y=62\\2P_Y-2P_X=12\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P_X=E_X=Z_X=26\\P_Y=E_Y=Z_Y=32\\N_X+N_Y=62\end{matrix}\right.\)
Em xem đề có thiếu chỗ nào không.
Đúng 1
Bình luận (2)
Hợp chất Z tạo bởi 2 nguyên tố M, R có công thức MaRb trong đó R chiếm 6,667% khối lượng. Trong hạt nhân nguyên tử M có số nơtron nhiều hơn số proton 4 hạt; còn trong hạt nhân R có số nơtron bằng số proton; tổng số hạt proton trong Z là 84 và a+b4. Khối lượng phân tử Z là A. 67 B. 161 C. 180 D. 92
Đọc tiếp
Hợp chất Z tạo bởi 2 nguyên tố M, R có công thức MaRb trong đó R chiếm 6,667% khối lượng. Trong hạt nhân nguyên tử M có số nơtron nhiều hơn số proton 4 hạt; còn trong hạt nhân R có số nơtron bằng số proton; tổng số hạt proton trong Z là 84 và a+b=4.
Khối lượng phân tử Z là
A. 67
B. 161
C. 180
D. 92