X là dung dịch HCl 0,04M
Y là dung dịch hỗn hợp gồm NaOH 0,02M và Ba(OH)2 0,01M
a/ Hãy tính pH của dung dịch X và pH của dung dịch Y .
b/ Hãy tính pH của dung dịch thu được khi trộn 300 ml dd X với 200 ml dd Y .
HELP ME !!!!!111
X là dung dịch HCl 0,04M
Y là dung dịch hỗn hợp gồm NaOH 0,02M và Ba(OH)2 0,01M
a/ Hãy tính pH của dung dịch X và pH của dung dịch Y
b/ Hãy tính pH của dung dịch thu được khi trộn 300ml dung dịch X với 200 ml dung dịch Y
a)
- Dung dịch X:
HCl → H+ + Cl-
0,04M → 0,04M
→ [H+] = 0,04M
→ pH = -log[H+] = -log(0,04) ≈ 1,4
- Dung dịch Y:
NaOH → Na+ + OH-
0,02M ______0,02M
Ba(OH)2 → Ba2+ + 2OH-
0,01M_________0,02M
→ [OH-] = 0,02 + 0,02 = 0,04M
→ pOH = -log[OH-] = -log(0,04) ≈ 1,4
→ pH = 14 - pOH = 14 - 1,4 ≈ 12,6
b)
300 ml X có: nH+ = nHCl = 0,3.0,04 = 0,012 mol
200 ml Y có: nOH- = nNaOH + 2nBa(OH)2
= 0,2.0,02 + 2.0,2.0,01 = 0,008 mol
PT ion: H+ +OH- → H2O
Bđ:__0,012__0,008
Pư: __0,008__0,008
Sau:__0,004 ___0
→ [H+] =\(\frac{0,004}{0,3+0,2}\) = 0,008M
→ pH = -log(0,008) ≈ 2,1
Tính pH của dung dịch thu được khi trộn 300 ml dung dịch HCl 0,025M với 100 ml dung dịch hỗn hợp NaOH 0,01M + Ba(OH)2 0,02M .
Cho dung dịch X là dung dịch HCl 0,01M . Dung dịch Y là dung dịch Ba(OH)2 0,005M
a/ Tính pH của dung dịch X và pH của dung dịch Y .
b/ Trộn 300 ml dd X với 200 ml dd Y thu được 500 ml dd Z . Tính pH của dd Z .
A là dung dịch HCl 0,01M ; B là dung dịch hỗn hợp gồm NaOH 0,01M và Ba(OH)2 0,015M .
a/ Hãy tính pH của dung dịch A và pH của dung dịch B .
b/ Hãy tính pH của dung dịch thu được khi trộn 300ml dung dịch A với 100 ml dung dịch B .
HELP ME !!!!!
Trộn 250ml dung dịch hỗn hợp gồm H2SO4 0,005M và HCl 0,01M với 200ml dung dịch hỗn hợp gồm NaOH 0,001M và Ba(OH)2 0,0005M thu được dung dịch X. Dung dịch X có pH là:
A. 12,3
B. 1,18
C. 11,87
D. 2,13
Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 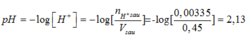
Tính pH của các dung dịch sau :
a.Trộn 100 ml dung dịch HCl 0,12M với 100 ml dung dịch H2SO4 0,04M. Tính pH của dung dịch X thu được .
b. Trộn 100 ml dung dịch KOH 0,12M với 100 ml dung dịch Ba(OH)2 0,04M. Tính pH của dung dịch thu được .
a) \(n_{H^+}=n_{HCl}+2n_{H_2SO_4}=0,1\cdot0,12+0,1\cdot0,04=0,016\)
\(C_M=\dfrac{0,016}{0,2}=0,08M\)
\(\Rightarrow pH=-log\left(0,08\right)=1,1\)
b) \(n_{OH^-}=n_{KOH}+2n_{Ba\left(OH\right)_2}=0,012+2\cdot0,004=0,02\)
\(C_M=\dfrac{0,02}{0,2}=0,1\)
\(\Rightarrow pH=-log\left(\dfrac{10^{-14}}{0,1}\right)=13\)
Trộn 300ml dung dịch hỗn hợp H2SO4 0,04M và HNO3 0,02M với 300 ml dung dịch hỗn hợp NaOH 0,04M và Ba(OH)2 0,02M . Tính pH của dung dịch thu được .
HELP ME !!!!
Trộn 100 ml dung dịch hỗn hợp gồm H2SO4, 0,05M và HCL 0,1M với 100 ml dung dịch hỗn hợp NaOH 0,2M và Ba(OH)2 0,1M, được dung dịch X. Tính giá trị pH của dung dịch X và tính khối lượng kết tủa thu được.
`100mL=0,1L`
`n_{H^+}=0,1.0,05.2+0,1.0,1=0,02(mol)`
`n_{SO_4^{2-}}=0,1.0,05=0,005(mol)`
`n_{OH^-}=0,1.0,2+0,1.0,1.2=0,04(mol)`
`n_{Ba^{2+}}=0,1.0,1=0,01(mol)`
`Ba^{2+}+SO_4^{2-}->BaSO_4`
Do `0,01>0,005->` Tính theo `SO_4^{2-}`
`n_{BaSO_4}=n_{SO_4^{2-}}=0,005(mol)`
`->m_↓=0,005.233=1,165(g)`
`H^{+}+OH^{-}->H_2O`
Do `0,02<0,04->OH^-` dư
`n_{OH^{-}\ pu}=n_{H^+}=0,02(mol)`
`->n_{OH^{-}\ du}=0,04-0,02=0,02(mol)`
Trong X: `[OH^-]={0,02}/{0,1+0,1}=0,1M`
`->pH=14-pOH=14+lg[OH^-]=13`
Trộn 200 ml dung dịch HCl 0,025M với 300 ml dung dịch Ba(OH)2 0,01M, sau đó thêm vào 500 ml H2O thu được dung dịch A.
a) Tính pH của dung dịch A.
b) Tính cho 100 ml dung dịch FeSO4 0,02M vào dung dịch A. Tính khối lượng kết tủa thu được
a, \(n_{H^+}=0,025.0,2=0,005\left(mol\right)\)
\(n_{OH^-}=0,01.2.0,3=0,006\left(mol\right)\)
\(\Rightarrow n_{OH^-dư}=0,001\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]_{dư}=\dfrac{0,001}{1}=10^{-3}\)
\(\Rightarrow\left[H^+\right]=10^{-11}\)
\(\Rightarrow pH=11\)
b, \(n_{Fe^{2+}}=n_{SO_4^{2-}}=0,02.0,1=0,002\left(mol\right)\)
\(n_{Ba^{2+}}=0,01.0,3=0,003\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{BaSO_4\downarrow}=n_{SO_4^{2-}}=0,002\left(mol\right)\\n_{Fe\left(OH\right)_2\downarrow}=n_{OH^-dư}=0,001\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{\downarrow}=0,002.233+0,001.90=0,556\left(g\right)\)