N.tử của n.tố X có 16 p trog hạt nhân, trả lời câu hỏi sau:
a)Tên và kí hiệu của X
b)Số e trog n.tử của n.tố X
c)N.tử X nặng gấp b.nh lần n.tử Hydro, n.tử Ôxi
Mik đag cần gấp giúp mik nhóa!!!
Tổng số hạt trong n.tử n.tố A là 49.Trong đó,số hạt mang điện nhiều hơn số ko mang điện là 15.Xác định số proton,notron,electron có trong n.tử A
lập hai hệ pt dựa vào dữ kiện đầu bài
ta có
p+n+e=116 mà p=e <=> 2p+n=49 (1)
vì số hạt mang điện nhiều hơn số hạt không mang điện là 15
=> (p+e)-n=15 mà p=e <=> 2p-n=15 (2)
từ (1) (2) => giải hệ bấm máy tính
=>p=16,n=17,e=16
Vì tổng số hạt trong ntử ntố A là 49 nên ta có: p + n + e =49
mà số p = số e => 2p + n = 49 (1)
Mặt khác: số hạt mang điện nhiều hơn số hạt không mang điện là 15 nên ta có : p+e-n=15 . mà p=e => 2p - n = 15 (2)
Từ (1) và (2) => 2p = \(\dfrac{49+15}{2}\) = 32 => p = e = 32/2 = 16
Thay p vào (1) ta được : 2.16 +n = 49=> 32+n=49 =>n=49-32=17
Vậy p=e=16; n=17
Gọi số hạt p, e, n trong nguyên tử nguyên tố A lần lượt là p, e ,n
Theo bài ra, ta có:
\(\left\{{}\begin{matrix}p+e+n=49\\p+e=15+n\end{matrix}\right.\)
Vì số p = số e nên p + e = 2p
\(\rightarrow\left\{{}\begin{matrix}2p+n=49\left(1\right)\\2p=15+n\left(2\right)\end{matrix}\right.\)
Thay (2) vào (1), ta có:
\(15+n+n=49\)
\(\rightarrow15+2n=49\)
\(\rightarrow2n=34\)
\(\rightarrow n=17\) thay vào (2)
\(\rightarrow p=16=e\)
Phân tử hợp chất A gồm 1 nguyên tử nguyên tố C liên kết với 1 nguyên tử O và năng bằng 2 lần nguyên tử Ca
a) Tính PTK hợp chất A
b) Tính N.tử khối của X , cho biết tên và kí hiệu hoá học của N.tố X
Nguyên tử nguyên tố X đâu bạn ?
X mình lại ghi nhầm thành C ạ
a) Theo đề bài, ta có: A=2.NTKCa
<=> A=2.40=80 đvC
b) Công thức dạng chung của hợp chất A là: XO
Mà PTK của A bằng 80
<=> 1.NTKX+1.16=80 đvC
<=> NTKX =64
Vậy X thuộc nguyên tố Đồng (Cu)
1) viết cấu hình của n.tử X biết tổng số e trên các p lớp p=7
2) viết c.hình của n.tử Y biết Y có 4 lớp e và 7e lớp ngoài cùng
3) viết c.hình của M3+ biết n.tử M có 13e
4) viết cấu hình của Y2- biết n.tử Y có 16e
A, B là hai n.tử của hai n.tố cách nhau 5 n.tố. tổng số hiệu nguyên tử của A và B là 28 ( ZA < ZB)
a) Xác định A và B và vị trí của A,B trong BTH
b) Viết ct oxit cao nhất và ct hidroxit t/ứng của A,B
a) Ta có : \(\left\{{}\begin{matrix}Z_B-Z_A=6\\Z_A+Z_B=28\end{matrix}\right.\)
⇔ \(\left\{{}\begin{matrix}Z_A=11\\Z_B=17\end{matrix}\right.\)
⇒ A là Natri (Na) , B là Clo (Cl)
+Cấu hình electron của A : \(1s^22s^22p^63s^1\)
số thứ tự : 11, chu kì : 3 , nhóm : IA
+Cấu hình electron của B : \(1s^22s^22p^63s^23p^5\)
số thứ tự : 17 , chu kì : 3 , nhóm : VIIA
b) -Công thức oxit cao nhất của A : \(Na_2O\)
Công thức hidroxit tương ứng : NaOH
- Công thức oxit cao nhất của B : \(Cl_2O_7\)
Công thức hidroxit tương ứng : \(HClO_4\)
Lập CTHH của những hợp chất tạo bởi 1 n.tố va nhóm n.tử sau :
+,Kẽm có hóa trị 2 và nhóm SO4
CTDC:\(Zn^{II}_x\left(SO4\right)^{II}_y\)
Theo quy tắc hóa trị ta có
\(x.II=y.II=>\frac{x}{y}=\frac{II}{II}=\frac{1}{1}\)
CTHH:ZnSO4
Lấy 4,08g hỗn hợp 2 kim loại Xvà Y phân tích thấy trong đó có chứa 42.10^21 n.tử , biết số n.tử Y gấp 2,5 lần số n.tử X và tỉ lệ n.tử X và Y là 8:7
a, tìm 2 kim loại X và Y
b, đem 2 kim loại X và Y trên cho t/dụng với khí A thu đc 2 chất rắn X1 và Y1, 2 chất này bị khử bởi khí B, khí B này đc điều chế = cách cho Y t/dụng vs dd HCl . Tìm cthh của các chất A,B,X1,Y1 và viết các pthh xảy ra.
tổng số mol của X và Y = (42✖ 10^21)/(6✖ 10^23)=0.07mol
gọi số mol của X là a , số mol của Y là b
vì số nguyên tử Y gấp 2.5 lần số nguyên tử X nên 2.5a=b
tổng số mol của X và Y là 0.07 nên a+b=0.07(1)
thay b=2.5a vào (1) ta được 3.5a=0.07➡ a=0.02 mol➡ b=0.05 mol
vì tỉ lệ nguyên tử X và Y là 8:7 nên MX=8MY/7(2)
vì tổng số gam X và Y là 4.08 nên 0.02✖MX+0.05✖MY=4.08(3)
thay (2) vào (3) tìm được MX =56, MY =64
vậy X là Cu , Y là Fe
Fe +2HCl➡ FeCl2+H2
➡ khí B là H2
vì B có tính khử oxit nên X1 và Y1 là oxit
➡ X1 là CuO , Y1 là FeO➡ A là khí Oxi
nguyên tử nguyên tố A có 12 proton có 2 electron ở lớp ngoài cùng, nguyên tử này nặng băng 3/2 n.tử Oxi.
a) vẽ sơ đồ
b) tính nguyên tử nguyên tố A
c) Hạt nhân n.tử A có bn nơtron
giúp em câu c) thui Hai câu kia em piết rồi
Cation M2+ có cấu hình e phân lớp ngoài cùng là 4p6.
a) Viết cấu hình e n.tử M ( Cho biết vị trí của M trong HTTH Gọi tên M
b) Anion X3- có cấu hình e giống của M2+, X là n.tố nào?
Nguyên tử Y có tổng số hạt là 46 hạt. Biết rằng trong hạt nhân nguyên tử có tổng số hạt ko quá 32 hạt. Tìm tên nguyên tử Y và vẽ sơ đồ cấu tạo n.tử
Nguyên tử Y có tổng số hạt là 46 hạt : \(2Z+N=46\)
=> N= 46 - 2Z
Biết rằng trong hạt nhân nguyên tử có tổng số hạt ko quá 32 hạt.
=> Z+N \(\le\) 32
=> \(Z+46-2Z\le32\)
=> \(-Z\le-14\)
=> \(Z\ge14\) (1)
Mặt khác ta có : \(Z\le N\le1,5Z\)
=> \(Z\le46-2Z\le1,5Z\)
=> \(13,14\le Z\le15,3\) (2)
Từ (1), (2) =>\(\left[{}\begin{matrix}Z=14\\Z=15\end{matrix}\right.\Rightarrow\left[{}\begin{matrix}N=18\left(loại\right)\\N=16\left(chọn\right)\end{matrix}\right.\)
=> Z=15 , N=16
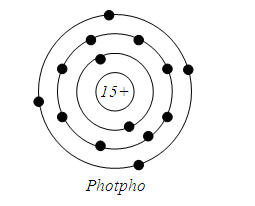
Vậy Y là Photpho (P)
Cấu hình e : 1s22s22p63s23p3