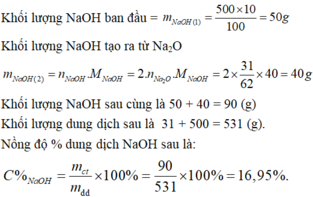Cho 31 gam Na2O vào 500 gam dung dịch NaOH 10%. Tính nồng độ % của dung dịch NaOH tạo ra (Na = 23, H = 1, O = 16).

Những câu hỏi liên quan
Cho 31 gam Na2O vào 500 gam dung dịch NaOH 10%. Tính nồng độ % của dung dịch NaOH tạo ra (Na = 23, H = 1, O = 16).
\(Na_2O+H_2O\rightarrow2NaOH\)
Khối lượng NaOH ban đầu:
\(m_{NaOH}=\dfrac{500.10}{100}=50g\)
Khối lượng NaOH được tạo ra từ Na2O:
\(m_{NaOH}=2.n_{Ca_2O}.M_{NaOH}=2.\dfrac{31}{62}.40=40g\)
Khối lượng NaOH sau cùng là: 50 + 40 = 90g
Khối lượng dd sau: 31 + 500 = 531g
Nồng độ % dd NaOH:
\(C\%_{NaOH}=\dfrac{90}{531}.100\%=16,95\%\)
Đúng 1
Bình luận (0)
Cho 31 gam Na2O vào 500 gam dung dịch NaOH 10%. Tính nồng độ % của dung dịch NaOH tạo ra (Na = 23, H = 1, O = 16).
Cho 31 gam Na2O vào 500 gam dung dịch NaOH 100/0 . Tính nồng dộ phần trăm của dung dịch NaOH tạo ra
\(n_{Na_2O}=\dfrac{31}{62}=0.5\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(0.5........................1\)
\(m_{NaOH}=1\cdot40+500\cdot10\%=90\left(g\right)\)
\(m_{dd_{NaOH\left(sau\right)}}=31+500=531\left(g\right)\)
\(C\%_{NaOH}=\dfrac{90}{531}\cdot100\%=16.9\%\)
Đúng 2
Bình luận (1)
\(n_{Na_2O}=\dfrac{31}{62}=0,5\left(mol\right)\)
\(n_{NaOH\left(bd\right)}=\dfrac{500.10}{100.40}=1,25\left(mol\right)\)
PTHH: Na2O + H2O --> 2NaOH
_______0,5----------------->1__________(mol)
nNaOH(sau pư) = 1,25 + 1 = 2,25 (mol)
\(C\%_{NaOH}=\dfrac{2,25.40}{31+500}.100\%=16,95\%\)
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
Cho 23 gam Na vào 500 ml dung dịch NaOH 10% (d = 1,2 gam/ml). Tính nồng độ % của dung dịch mới.
\(n_{Na}=\dfrac{23}{23}=1\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(1......................1.............0.5\)
\(m_{NaOH}=500\cdot1.2\cdot10\%=60\left(g\right)\)
\(m_{NaOH}=1\cdot40+60=100\left(g\right)\)
\(m_{dd_{NaOH}}=23+500\cdot1.2-0.5\cdot2=622\left(g\right)\)
\(C\%_{NaOH}=\dfrac{100}{622}\cdot100\%=16.07\%\)
Đúng 2
Bình luận (0)
hòa tan hết 12,4 gam Natri oxit (Na2O) vào nước thu được 500ml dung dịch NaOH Tính nồng độ mol của dung dịch bazơ thu được. (Biết Na=23, O=16
\(n_{Na_2O}=\dfrac{12,4}{62}=0,2mol\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,2 \(\rightarrow\) 0,2 \(\rightarrow\) 0,4
\(C_{M_{NaOH}}=\dfrac{0,4}{\dfrac{500}{1000}}=0,8M\)
Đúng 1
Bình luận (0)
Cho 6,2 gam Na2O tác dụng với H2O thu được 0.5 lít dung dịch NaOH . a. Tính nồng độ mol của dung dịch NaOH thu được ? b. Tính khối lượng HCl dùng để trung hoà lượng NaOH trên ? ( Cho biết : Na = 23 ; O = 16 ; H = 1 ; Cl = 35,5 ) . .
Cho 6,2 gam Na2O tác dụng với H2O thu được 0.5 lít dung dịch NaOH .
a. Tính nồng độ mol của dung dịch NaOH thu được ?
b. Tính khối lượng HCl dùng để trung hoà lượng NaOH trên ?
( Cho biết : Na = 23 ; O = 16 ; H = 1 ; Cl = 35,5 ) . .
Xem chi tiết
\(n_{Na_2O}=\dfrac{6.2}{62}=0.1\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(0.1.........................0.2\)
\(C_{M_{NaOH}}=\dfrac{0.2}{0.5}=0.4\left(M\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(0.2.............0.2\)
\(m_{HCl}=0.2\cdot36.5=7.3\left(g\right)\)
Chúc em học tốt !!!
Đúng 2
Bình luận (0)
Trung hòa 0,4 mol dung dịch HCl bằng 80 gam dung dịch NaOH nồng độ a%. Tính nồng độ a của dung dịch NaOH? (Biết Na = 23; H = 1; O = 16; Cl = 35,5), giúp mình ạ
PTHH: HCl + NaOH --> NaCl + H2O
______0,4<--0,4
=> mNaOH = 0,4.40 = 16(g)
=> \(C\%NaOH=\dfrac{16}{80}.100\%=20\%\)
Đúng 2
Bình luận (0)
Trung hoà 200 gam dung dịch NaOH nồng độ 10% bằng 100 gam dung dịch HCl. Nồng độ phần trăm chất tan trong dung dịch sau phản ứng là (Cho biết: Cl=35,5; Na=23; H=1; O=16)
\(m_{NaOH}=\dfrac{200.10}{100}=20\left(g\right)=>n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right)\)
PTHH: NaOH + HCl --> NaCl + H2O
______0,5-------------->0,5
=> mNaCl = 0,5.58,5 = 29,25(g)
mdd sau pư = 200 + 100 = 300 (g)
=> \(C\%\left(NaCl\right)=\dfrac{29,25}{300}.100\%=9,75\%\)
Đúng 3
Bình luận (1)