X có tổng số các loại hạt 13. Hạt mang điện nhiều hơn hạt không mang điện là 3. Xác định A và Z của X? Giúp em vs mọi ng ạ 😭

Những câu hỏi liên quan
mọi người giải giúp em bài này với ạ . Em cảm ơn nhiều ạ
nguyên tử của nguyên tố X có số khối là 63.Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 24 hạt
a. Xác định số p,n,e của X
b.tính tổng số hạt có các loại có trong 15.75g X
a) \(\left\{{}\begin{matrix}A=Z+N=63\\2Z-N=24\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}Z=29=P=E\\N=34\end{matrix}\right.\)
=> X là \(^{63}_{29}Cu\)
b) Ta có : \(n_{^{63}_{24}Cu}=\dfrac{15,75}{63}=0,25\left(mol\right)\)
Trong 15,75g có số nguyên tử Cu là : \(0,25.6.10^{23}=1,5.10^{23}\)(nguyên tử)
Vậy trong 15,75g có tổng số hạt là :
\(\left(2Z+N\right).1,5.10^{23}=\left(29.2+34\right).1,5.10^{23}=138.10^{23}\left(hạt\right)\)
Đúng 2
Bình luận (0)
* Nguyên tử X:
A=P+N=63 (1)
Mặt khác: 2P-N=24 (2)
Từ (1), (2) ta lập hệ pt:
\(\left\{{}\begin{matrix}P+N=63\\2P-N=24\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=29=E=Z\\N=34\end{matrix}\right.\)
a) X có 29p, 29e, 34n
b) Tổng số hạt có trong 15,75 gam X:
Số P=Số E= (15,75/63) x 29= 7,25 (sấp sỉ 7 hạt nhá)
Số N=(15,75/63) x 34= 8,5 (hạt)
Đúng 1
Bình luận (0)
Mọi người giúp em bài này với ạ. Em cảm ơn
1. Nguyên tử X có tổng số proton, nơtron, electron là 116 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 24. Xác định số hạt từng loại.
từ đề bài ta có:
1.p+n+e=116 mà số p= số e=)2p+n=116
2.hạt mạng điện là e và p=)2p-n=24
ta cộng cái trên cái dưới ra 4p=140=)p=35
từ đó suy ra số các hạt khác
Đúng 2
Bình luận (0)
Ta có: Tổng số proton, nơtron, electron là 116 ➩ e+p+n=116
Số hạt mang điện nhiều hơn số hạt không mang điện là 24 ➩ (e+p)-n=24
Vì e=p ➩\(\left\{{}\begin{matrix}\text{ e+p+n = (e+p)+n = 2p+n = 116 }\\(e+p)-n=2p-n=24\end{matrix}\right.\)
➩\(\left\{{}\begin{matrix}2p=\left(116+24\right):2\\n=\left(116-24\right):2\end{matrix}\right.\)
➩\(\left\{{}\begin{matrix}2p=70\\n=46\end{matrix}\right.\)
➩\(\left\{{}\begin{matrix}e=p=70:2=35\\n=46\end{matrix}\right.\)
Đúng 2
Bình luận (0)
. Hợp chất X2Y6 có tổng số các loại hạt là 392, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 120 hạt. Số khối của X ít hơn số khối của Y là 8. Tổng số hạt trong X3+ nhiều hơn của Y- là 13.a) Xác định X, Y.
Đọc tiếp
. Hợp chất X2Y6 có tổng số các loại hạt là 392, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 120 hạt. Số khối của X ít hơn số khối của Y là 8. Tổng số hạt trong X3+ nhiều hơn của Y- là 13.
a) Xác định X, Y.
Có: P = E (Do nguyên tử trung hòa về điện.)
- Tổng số hạt trong X2Y6 là 392
⇒ 2.(2PX + NX) + 6.(2PY + NY) = 392 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 120 hạt.
⇒ 2.2PX + 6.2PY - 2NX - 6NY = 120 (2)
- Số khối của X ít hơn số khối của Y là 8.
⇒ PY + NY - (PX + NX) = 8 (3)
- Tổng số hạt trong X3+ ít hơn Y- là 16.
⇒ (2PY + NY + 1) - (2PX + NX - 3) = 16 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_X=E_X=13\\N_X=14\\P_Y=E_Y=17\\N_Y=18\end{matrix}\right.\)
⇒ X là Al, Y là Cl.
Đúng 2
Bình luận (2)
1, một ng tử có tổng các loại hạt là 40 hạt mang điện nhiều hơn hạt ko mang điện xác định tên ng tử
2, một ng tử có tổng các loại hạt là 60 hạt mang điện gấp đôi hạt ko mang điện xác định tên ng tố
3, một ng tử có tổng các loại là 13 xác định tên ng tử biết (1 <hoặc= nơtron/proton <hoặc= 1,5)
Giúp mik các bạn ơi
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y 3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định ngu...
Đọc tiếp
1:Tổng số hạt cơ bản của nguyên tử nguyên tố X là 36.Trong đó số hạt mang điện gấp đôi số hạt không mang điện.Xác định số hiệu nguyên tử và số khối của nguyên tử X?
2:Tổng số hạt trong nguyên tử là Y là 54 hạt,trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a)Xác định các loại hạt trong Y b)Xác định đơn vị điện tích hạt nhân của Y c)Viết kí hiệu nguyên tử Y
3:Nguyên tử R có tổng số hạt là 115.Số hạt mang điện nhiều hơn số hạt không mang điện là 25.Xác định nguyên tử R từ đó suy ra STT của R?
-Mình cần rất gấp,các bạn giúp mình với!-
1. Ta có tổng số hạt cơ bản của nguyên tố X là 36 , suy ra
p + e + n = 36 => 2p + n = 36
Số hạt mang điện gấp đôi số hạt không mang điện : 2p = 2n => p = n
Vậy : 3p = 36 => p = 12 => số p = số e = số z = 12
Số khối : A = p + n = 12 + 12 = 24
Đúng 2
Bình luận (3)
2.
a, Ta có tổng số hạt cơ bản là 54 hạt.
=> p+e+n=54 => 2p+n=54(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 14
=> 2p-n=14(2)
Từ (1) và (2) ta có hệ pt:
2p-n=14
2p+n=54
<=> p=17
n=20
Vậy e=17, p=17, n=20
b, số hiệu nguyên tử Z=17
c, kí hiệu: Cl
Đúng 2
Bình luận (1)
3.
Ntử R có tổng số hạt cơ bản là 115
=> p+e+n=115
=>2p+n=115(1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 25
=> 2p-n=25(2)
Từ (1)&(2) => ta có hệ phương trình
=>2p+n=115
2p-n=25
<=>p=35
n=45
=> e=35, p=35, n=45
=> R là Br
STT của Br là 35
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
. Nguyên tử Z số hạt mang điện nhiều hơn số hạt không mang điện là 12 và trong hạt nhân số hạt không mang điện nhiều hơn số hạt mang điện là 1. Xác định số lượng các loại hạt cấu tạo nguyên tử Z.
13. Một nguyên tử Z có tổng số hạt là 155. Trong đó số hạt mang điện nhiều hơn tổng số hạt không mang điện là 33 hạt. Xác định số khối của Z.
(Anh làm tóm tắt nha)
Theo đề, ta có HPT:
\(\left\{{}\begin{matrix}2p+n=155\\2p-n=33\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2n=122\\2p-n=33\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}n=61\\p=47\end{matrix}\right.\)
Vậy p = e = 47 hạt, n = 61 hạt
Ta có số khối của nguyên tử là:
n + p = 61 + 47 = 108 (đvC)
Đúng 2
Bình luận (4)
Một nguyên tử M có tổng số hạt các loại bằng 58. Số hạt mang điện tích nhiều hơn số hạt không mang điện là 18. Tìm số khối
Giải :
Ta có :
p + n + e = 58
-> 2Z + n = 58 (1)
Ta lại có : 2Z - n = 18 (2)
Từ (1) và (2) ta có hpt :
2Z + n = 58
2Z - n = 18
=> Z = 19 , n = 20
Số khối A = Z + n = 19 + 20 = 39
-> Đó là Kali ( K)
Đúng 3
Bình luận (0)
Nãy mình làm sai ạ :( mang điện tích 2Z còn mang điện tích dương chỉ có Z thôi nhé
Tổng số hạt : p + e + n = 155
Ta có : 2Z + n = 155 (1)
Lại có : 2Z - n = 33 (2)
Từ (1) và (2) ta có hpt và giải ra ta đc : Z = 47 , n = 61
Số khối A = Z + n = 47 + 61 = 108
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Tổng số hạt proton, nơtron, electron trong 2 nguyên tử kim loại X và Y là 142, trong đó tổng số hạt mang điện nhiều hơn tổng sô hạt không mang điện là 42. Số hạt mang điện của nguyên tử Y nhiều hơn của X là 12.Xác định hai kim loại X và Y.
Kí hiệu : P X , P Y và N X , N Y lần lượt là số proton và số nơtron của nguyên tử X và Y.
Theo đề bài ta lập được hệ phương trình đại số :
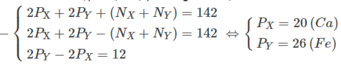
Đúng 1
Bình luận (1)
Ai giúp mình vs
Một nguyên tử Y có tổng số hạt là 82. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22.
Tìm ký hiệu của nguyên tử Y
Một nguyên tử X có tổng số hạt là 115 trong đó số hạt mang điện gấp 14/9 lần không mang điện. Xác định ký
hiệu của nguyên tử X
Cảm ơn mn
Nguyên tử Y:
\(\left\{{}\begin{matrix}P+N+E=82\\P=E\\\left(P+E\right)-N=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+E=82\\2P-N=22\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=26\\N=30\end{matrix}\right.\)
Kí hiệu: \(^{56}_{26}Fe\)
* Nguyên tử X:
\(\left\{{}\begin{matrix}P+N+E=115\\P=E\\P+E=\dfrac{14}{9}N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=115\\2P-\dfrac{14}{9}N=0\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=35\\N=45\end{matrix}\right.\)
Kí hiệu: \(^{80}_{35}Br\)
Đúng 1
Bình luận (0)
1/ Theo đề ta có:\(S=2Z+N=82\)(1)
\(2Z-N=22\)(2)
từ (1) và(2)\(\Rightarrow Z=26;N=30\)
A=Z+N=26+30=56
Vậy kí hiệu nguyên tử Y là\(^{56}_{26}Fe\)
2/Theo đề ta có:\(S=2Z+N=115\)(1)
\(2Z=\dfrac{14}{9}N\Leftrightarrow2Z-\dfrac{14}{9}N=0\)(2)
Từ (1) và (2)\(\Rightarrow Z=35;N=45\)
A=Z+N=35+45=80
Vậy kí hiệu nguyên tử X là \(^{80}_{35}Br\)
Đúng 0
Bình luận (0)

























