Dẫn 36 gam hỗn hợp khí gồm ( CO , H2 ) đi từ từ qua 139,2 gam bột Fe3O4 đun nóng ở nhiệt độ cao, thu được m gam sắt và 74,4 gam hỗn hợp ( CO2 , H2O ). Tính khối lượng dắt thu được.

Những câu hỏi liên quan
Dẫn 36 gam hỗn hợp khí gồm
(
C
O
,
H
2
)
đi từ từ qua 139,2 gam bột
F
e
3
O
4
đun nóng ở nhiệt độ cao, thu được m gam sắt và 74,4 gam hỗn hợp
(
C
O
2
,
H
2
O
)
. Tính khối lượng sắt thu được.
Đọc tiếp
Dẫn 36 gam hỗn hợp khí gồm ( C O , H 2 ) đi từ từ qua 139,2 gam bột F e 3 O 4 đun nóng ở nhiệt độ cao, thu được m gam sắt và 74,4 gam hỗn hợp ( C O 2 , H 2 O ) . Tính khối lượng sắt thu được.
PTHH:
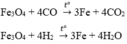
Áp dụng định luật bảo toàn khối lượng, ta có:
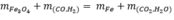
m_Fe=m=139,2+36-74,4=100,8 gam
Đúng 0
Bình luận (0)
Dẫn 36g hỗn hợp khí gồm CO và H2 đi từ từ qua139,2g bột sắt Fe3O4 đun nóng ở nhiệt độ caoo, thu dc m gam sắt và 74,4 g hỗn hợp CO2 và H2O. Tính khối lượng sắt thu dc sau phản ứng, biết phản ứng vừa đủ .
Fe3O4 + 4CO → 3Fe + 4CO2
Fe3O4 + 4H2 → 3Fe + 4H2O
Theo định luật bảo toàn khối lượng
=> mFe3O4 + mCO + H2 = mFe + mCO2 + H2O
=> 139,2 + 36 = mFe + 74,4
=> mFe = 100,8 ( gam )
=> Khối lượng Fe thu được sau phản ứng là 100,8 gam
Đúng 0
Bình luận (0)
PTHH :
Fe3O4 + 4CO -----> 3Fe + 4CO2
Fe3O4 + 4H2 -----> 3Fe + 4H2O
Phản ứng đủ
Theo Định luật BTKL ta có :
mFe3O4 + mhh (khí) - mCO2 - mH2O = mFe
=> 139,2 + 36 - 74,4 = mFe
=> 100,8 (g) = mFe
Vậy khối lượng sắt thu được sau phản ứng là 100,8 (g)
Đúng 0
Bình luận (0)
Câu 1:Dẫn từ từ 5,6 lít khí CO đi qua ống sứ đựng m gam hỗn hợp bột A gồm Fe,FeO, Fe2O3, Fe3O4 đun nóng thu được 12,32 gam Fe và hỗn hợp khí Y. Hỗn hợp khí Y có tỉ khối hơi so với H2 là 18,8. Tính giá trị m. Biết các phản ứng xảy ra hoàn toàn và các khí đều đo ở điều kiện tiêu chuẩn
\(n_{CO\left(bđ\right)}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(CO+O_{oxit}\rightarrow CO_2\)
\(n_{CO}=n_Y=0.25\left(mol\right)\)
\(M_Y=18.8\cdot2=37.6\left(\dfrac{g}{mol}\right)\)
Bảo toàn khối lượng :
\(m_A=37.6\cdot0.25+12.32-0.25\cdot28=14.72\left(g\right)\)
Đúng 2
Bình luận (1)
1) Người ta dẫn khí CO qua m gam hỗn hợp X đun nóng gồm Fe2O3 và Fe3O4 thu được 2,8 gam hỗn hợp Y gồm Fe, FeO, Fe2O3, Fe3O4 và khí CO2. Dẫn toàn bộ khí CO2 thu được ở trên
qua dung dịch nước vôi trong dư được 7 gam kết tủa. Tính m?
\(m_{\text{kết tủa}}=m_{CaCO_3}=7\left(g\right)\\ \rightarrow n_{CaCO_3}=\dfrac{7}{100}=0,07\left(mol\right)\)
PTHH:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,07<--------------------0,07
\(O+CO\xrightarrow[]{t^o}CO_2\)
0,07<--------0,07
\(\rightarrow m_O=0,07.16=1,12\left(g\right)\)
Áp dụng ĐLBTNT:
\(m=m_X=m_Y+m_O=2,8+1,12=3,92\left(g\right)\)
Đúng 1
Bình luận (0)
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m A. 0,224 lít và 14,48 gam B. 0,672 lít và 18,46 gam C. 0,112 lít và 12,28 gam D. 0,448 lít và 16,48 gam
Đọc tiếp
Thổi từ từ V lít hỗn hợp khí (đktc) gồm CO và H2 đi qua ống đựng 16,8 gam hỗn hợp 3 oxit CuO, Fe3O4, Al2O3 nung nóng, phản ứng hoàn toàn. Sau phản ứng thu được m gam chất rắn và một hỗn hợp khí nặng hơn khối lượng của hỗn hợp V là 0,32 gam. Tính V và m
A. 0,224 lít và 14,48 gam
B. 0,672 lít và 18,46 gam
C. 0,112 lít và 12,28 gam
D. 0,448 lít và 16,48 gam
Đáp án D.
Ta có: mO = 0,32 (g) ⟹ nO = 0 , 32 16 = 0,02 (mol) nên số mol của hỗn hợp CO, H2 cũng bằng 0,02 (mol) ⟹ V = 0,02.22,4 = 0,448 (l).
Theo định luật bảo toàn khối lượng, m = 16,8 – 0,02.16 = 16,48 (g).
Đúng 0
Bình luận (0)
Cho hơi nước qua than nóng đỏ thu được 2,24 lít hỗn hợp khí X gồm
CO
2
, CO và
H
2
(đo ở đktc). Dẫn X qua hỗn hợp gồm CuO và
Al
2
O
3
dư nung nóng thu dược m gam chất rắn và hỗn hợp khí và hơi Y. Dẫn Y qua dung dịch
Ca
OH
2
dư, lọc bỏ kết tủa thấy khối lượng dung dị...
Đọc tiếp
Cho hơi nước qua than nóng đỏ thu được 2,24 lít hỗn hợp khí X gồm CO 2 , CO và H 2 (đo ở đktc). Dẫn X qua hỗn hợp gồm CuO và Al 2 O 3 dư nung nóng thu dược m gam chất rắn và hỗn hợp khí và hơi Y. Dẫn Y qua dung dịch Ca OH 2 dư, lọc bỏ kết tủa thấy khối lượng dung dịch giảm 1,16 gam. Khối lượng kim loại có trong m là
A. 5,12 gam
B. 1,44 gam
C. 6,4 gam
D. 2,7 gam
1. Dẫn khí H2 đi qua a gam hỗn hợp A gồm MgO, CuO,Fe3O4, Al2O3 đun nóng, thu được b gam hỗn hợp các chất ở trạng thái rắn( hỗn hợp B).Khí và hơi nước thoát ra được dẫn vào bình đựng dung dịch
PTHH: H2+ CuO-> Cu +H2O
4H2+ Fe3O4-> 3Fe +4H2O
khối lượng bình tăng=c =m(H2O)
n(H2)=n(H2O) = c/18 (mol)
áp dụng định luật bảo toàn khối lượng , ta có
mH2+ mA=mB+mH2O
<=> 2.c/18 +a=b+c
<=> a=b +8c/9
Đúng 2
Bình luận (1)
H2SO4 đặc, dư thấy khối lượng bình tăng c gam. Viết các PTHH có thể xảy ra và lập biểu thức giữa a,b,c
Đúng 0
Bình luận (0)
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp khí X gồm CO2, CO, H2. Toàn bộ lượng khí X vừa đủ khử hết 48 gam Fe2O3 thành Fe và thu được 10,8 gam H2O. Phần trăm thể tích CO2 trong hỗn hợp khí X là:
A. 14,28
B. 28,57
C. 13,24
D. 16,14
Đáp án A
C + H2O → t 0 CO + H2 (1)
0,3→ 0,3
C + 2H2O → t 0 CO2 + 2H2 (2)
0,15← (0,6-0,3)
CO2+ Ca(OH)2 → CaCO3+ H2O (3)
3CO + Fe2O3 → t 0 2Fe + 3CO2 (4)
0,3← (0,3-0,2)
3H2 + Fe2O3 → t 0 2Fe + 3H2O (5)
0,60 0,2← 0,6 mol
Ta có: n F e 2 O 3 = 0,3 mol; n H 2 O = 0,6 mol
Tính toán theo phương trình ta có: 0,3 mol CO; 0,15 mol CO2; 0,6 mol H2
→ % V C O 2 = % n C O 2 = n C O 2 n X . 100 % = 0 , 15 0 , 3 + 0 , 15 + 0 , 6 . 100 % = 14 , 28 %
Đúng 0
Bình luận (0)
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và
F
e
2
O
3
ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí
C
O
2
. Dẫn khí
C
O
2
sinh ra vào dung dịch
C
a
(
O
H
)
2
dư, thu được 35 gam kết tủa.Viết phản ứng xảy ra.Tính khối...
Đọc tiếp
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và F e 2 O 3 ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí C O 2 . Dẫn khí C O 2 sinh ra vào dung dịch C a ( O H ) 2 dư, thu được 35 gam kết tủa.
Viết phản ứng xảy ra.
Tính khối lượng mỗi kim loại tạo thành.
Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.


















