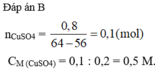Cho một cái đinh sắt nhúng vào trong 100ml dd CuSO4 1M.Sau một thời gian lấy đinh sắt lau khô khối lượng đinh sắt tăng 0,08g.Tính nồng độ mol của dung dịch sau pứ, coi như thể tích dd thay đổi ko đáng kể

Những câu hỏi liên quan
2.4/ Ngâm 1 đinh sắt sạch trg 200ml dd CuSO4. Sau phản ứng lấy đinh sắt ra có Cu tạo thành bám vào, rửa nhẹ, làm khô thấy khối lượng đinh tăng thêm 0,8g. Nồng độ mol/lít của dd CuSO4 trước phản ứng và lượng Cu bám vào đinh sắt là bao nhiêu ?
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là A. 2,8 gam. B. 7,0 gam. C. 3,5 gam. D. 5,6 gam.
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 2,8 gam.
B. 7,0 gam.
C. 3,5 gam.
D. 5,6 gam.
Ta có phản ứng: Fe + Cu2+ → Fe2+ + Cu↓
+ Đặt nFe pứ = a mol ⇒ nCu tạo thành = a mol.
⇒ mCu – mFe = 64a – 56a = 8a = 1 gam.
→ a = 0,125 ⇒ mFe đã pứ = 0,125×56 = 7 gam.
Đáp án B
Đúng 0
Bình luận (0)
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là A. 3,5 gam B. 7,0 gam C. 5,6 gam D. 2,8 gam
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 3,5 gam
B. 7,0 gam
C. 5,6 gam
D. 2,8 gam
Đáp án : B
Fe + Cu2+ -> Fe2+ + Cu
x -> x
mtăng = 64x – 56x = 1g => x = 0,125 mol
=> mFe pứ = 7g
Đúng 0
Bình luận (0)
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:
A. 3,5 gam.
B. 2,8 gam.
C. 7,0 gam.
D. 5,6 gam.
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là
A. 3,5 gam
B. 2,8 gam
C. 7,0 gam
D. 5,6 gam
Đáp án C
Fe + Cu2+ -> Fe2+ + Cu
.x -> x mol
=> mtăng = 64x – 56x = 1g => x = 0,125 mol
=> mFe pứ = 7g
Đúng 0
Bình luận (0)
Ngâm một đinh sắt đã được đánh sạch bề mặt vào 100 ml dung dịch CuSO4. Sau khi phản ứng hoàn toàn, lấy đinh sắt ra rửa nhẹ, sấy khô thấy khối lượng đinh sắt tăng thêm 1,6gam. Nồng độ mol ban đầu của dung dịch CuSO4 là: A. 1M B. 2M C. 3M D. 4M
Đọc tiếp
Ngâm một đinh sắt đã được đánh sạch bề mặt vào 100 ml dung dịch CuSO4. Sau khi phản ứng hoàn toàn, lấy đinh sắt ra rửa nhẹ, sấy khô thấy khối lượng đinh sắt tăng thêm 1,6gam. Nồng độ mol ban đầu của dung dịch CuSO4 là:
A. 1M
B. 2M
C. 3M
D. 4M
Đáp án B
Fe + Cu2+ → Fe2+ + Cu
Mol x → x
=> DmThanh KL(tăng) = mCu – mFe pứ = 64x – 56x = 1,6
=> x = 0,2 mol => nCuSO4 = nCu = 0,2 mol
=> CM(CuSO4) = 0,2 : 0,1 = 2M
Đúng 0
Bình luận (0)
Ngâm một đinh sắt sạch trong 200 ml dung dịch
C
u
S
O
4
sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch
C
u
S
O
4
đã dùng là: A. 0,3M. B. 0,5M. C. 0,4M. D. 0,25M.
Đọc tiếp
Ngâm một đinh sắt sạch trong 200 ml dung dịch C u S O 4 sau khi phản ứng kết thúc, lấy đinh sắt ra khỏi dung dịch rửa nhẹ làm khô nhận thấy khối lượng đinh sắt tăng thêm 0,8 gam. Nồng độ mol/lít của dung dịch C u S O 4 đã dùng là:
A. 0,3M.
B. 0,5M.
C. 0,4M.
D. 0,25M.
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:A. 2,8 gam. A. 2,8 gam. B. 7,0 gam. C. 3,5 gam. D. 5,6 gam.
Đọc tiếp
Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam. Khối lượng sắt đã phản ứng là:A. 2,8 gam.
A. 2,8 gam.
B. 7,0 gam.
C. 3,5 gam.
D. 5,6 gam.
Đáp án B
Ta có phản ứng: Fe + Cu2+ → Fe2+ + Cu↓
+ Đặt nFe pứ = a mol ⇒ nCu tạo thành = a mol.
⇒ mCu – mFe = 64a – 56a = 8a = 1 gam.
Û a = 0,125 ⇒ mFe đã pứ = 0,125×56 = 7 gam
Đúng 0
Bình luận (0)
nhúng một thanh sắt 8g vào 500ml dung dịch CuSO4 nồng độ 2M.Sau một thời gian lấy ra thấy thanh sắt nặng 8,8g. tính nồng độ mol của dung dịch sau phản ứng. Coi thể tích thay đổi không đáng kể
Gọi $n_{Fe\ pư} = a(mol)$
$Fe + CuSO_4 \to FeSO_4 + Cu$
$n_{Cu} = n_{Fe} = a(mol)$
Suy ra: $8 - 56a + 64a = 8,8 \Rightarrow a = 0,1(mol)$
$n_{FeSO_4} = n_{Fe} =a = 0,1(mol)$
$n_{CuSO_4\ dư} = 0,5.2 - 0,1 = 0,9(mol)$
$C_{M_{FeSO_4}} = \dfrac{0,1}{0,5} = 0,2M$
$C_{M_{CuSO_4}} = \dfrac{0,9}{0,5} = 1,8M$
Đúng 2
Bình luận (0)