Tính tỉ khối của hợp chất hữu cơ x số vs hiđrô bt khi hoá hơi 3g X thủ được thể tích hơi đúng bằng thể tích của 1,6g oxi trong cùng điều kiện
nN2 = \(\dfrac{2,8}{28}\)= 0,1 mol
4,6 gam X có thể tích bằng thể tích 2,8 gam nito => số mol của 4,6 gam X = số mol 2,8 gam nito = 0,1 mol
=> MX = \(\dfrac{4,6}{0,1}\) = 46 (g/mol)
Khi đốt cháy hoàn toàn 5,9 gam hợp chất hữu cơ A thu được 6,72 lít khí CO2(đkc); 1,12 lít khí N2 và 8,1g H2O. Mặt khác, khi hoá hơi 2,9 gam hợp chất hữu cơ A chiếm thể tích đúng bằng thể tích của 1,6g O2 ở cùng điều kiện. Tìm công thức phân tử hợp chất hữu cơ A.
Đốt cháy hoàn toàn 1,72 gam chất hữu cơ (E) thu được 3,52 gam CO2; 1,80 gam H2O và một lượng khí N2. Tìm công thức phân tử của E. biết khi hoá hơi 1,29 gam E thì thu được thể tích hơi đúng bằng thể tích 0,96 gam oxi trong cùng điều kiện
\(n_{CO_2}=\dfrac{3.52}{44}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_N=1.72-0.08\cdot12-0.1\cdot2=0.56\left(g\right)\)
\(n_N=\dfrac{0.56}{14}=0.04\left(mol\right)\)
\(M_E=\dfrac{1.29}{\dfrac{0.96}{32}}=43\left(đvc\right)\)
\(n_E=\dfrac{1.72}{43}=0.04\left(mol\right)\)
Số nguyên tử C : \(\dfrac{0.08}{0.04}=2\)
Số nguyên tử H : \(\dfrac{0.2}{0.04}=5\)
Số nguyên tử N : \(\dfrac{0.04}{0.04}=1\)
\(CT:C_2H_5N\)
\(n_{CO_2}=\dfrac{1.76}{44}=0.04\left(mol\right)\Rightarrow nC=0.04\left(mol\right)\Rightarrow m_C=0.04\cdot12=0.48\left(g\right)\)
\(n_{H_2O}=\dfrac{0.9}{18}=0.05\left(mol\right)\Rightarrow n_H=0.1\left(mol\right)\)
\(n_{N_2}=\dfrac{0.224}{22.4}=0.01\left(mol\right)\Rightarrow m_N=0.01\cdot28=0.28\left(g\right)\)
\(m_O=1.5-0.48-0.1-0.28=0.64\left(g\right)\)
\(n_O=\dfrac{0.64}{16}=0.04\left(mol\right)\)
\(Đặt:CTPT:C_xH_yO_zN_t\)
\(x:y:z:t=0.04:0.1:0.04:0.02=2:5:2:1\)
\(CTđơngiản:\left(C_2H_5O_2N\right)_n\)
\(M_X=\dfrac{1.5}{\dfrac{0.64}{32}}=75\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow75n=75\\ \Leftrightarrow n=1\\ CTPT:C_2H_5O_2N\)
Tiến hành pư este hoá hỗn hợp gồm glixerol và 2 axit : axit panmitic và axit stearic thu đc hợp chất hữu cơ X. Hoá hơi 59,6g X thu đc một thể tích đúng bằng thể tích của 2,8g khí nitơ ở cùng điều kiện. Tổng số nguyên tử cacbon trong 1 phân tử X?
Gọi CTHH của X là $(C_{15}H_{31}COO)_a(C_{17}H_{35}COO)_{b}C_3H_5(OH)_{3-a-b}$
Ta có :
$M_X = 255a + 283b+ 12.3 + 5 + 17(3-a-b)= \dfrac{59,6}{ \dfrac{2,8}{28}} = 596$
Suy ra a = b = 1 thì thỏa mãn
Vậy số nguyên tử C = 16 + 18 + 3 = 37
\(Đặt:CTHH:C_xH_yO_z\)
\(x:y:z=\dfrac{52.17}{12}:\dfrac{13.04}{1}:\dfrac{34.78}{16}=4.3475:13.04:2.17375=2:6:1\)
\(CTđơngiản:\left(C_2H_6O\right)_n\)
\(M_Y=\dfrac{9.2}{\dfrac{5.6}{28}}=46\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow46n=46\\ \Leftrightarrow n=1\)
\(Vậy:CTHH:C_2H_6O\)
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
\(M_Z = \dfrac{12}{\dfrac{14,2}{71}} = 60(đvC)\)
Số nguyên tử Cacbon = \(\dfrac{60.40\%}{12} = 2\)
Số nguyên tử Hidro = \(\dfrac{60.6,67\%}{1} = 4\)
Số nguyên tử Oxi = \(\dfrac{60.53,33\%}{16} = 2\)
Vậy CTPT của Z : C2H4O2
Phân tích 4,4 gam hợp chất hữu cơ Y thu được 8,8 gam CO2 và 3,6 gam H2O. Biết khi hóa hơi hoàn toàn 2,2 gam Y thì thu được thể tích bằng thể tích của 0,8 gam oxi trong cùng điều kiện. Lập công thức phân tử của chất Y:
A. C4H8O2
B. C2H6O2
C. C2H4O
D. C3H6
Theo đề bài ta có 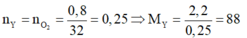
Vì sản phẩm cháy thu được CO2 và H2O nên Y chắc chắn chứa C, H, có thể có O.
Khối lượng các nguyên tố trong 4,4 gam chất Y là:
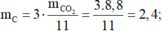
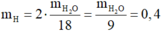
![]()
Gọi CTPT của chất Y là CxHyOz . ta có như sau:
Vậy ta có x = 4, y = 8 và z = 2
CTPT của Y là C4H8O2
Đáp án A.