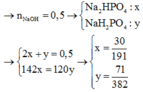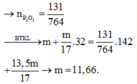Cho a (g) P2O5 vào 100 ml dung dịch natri hidroxit 3M. Kết thúc phản ứng dung dịch thu được 2 muối NaH2PO4 , Na2HPO4 . Tìm a

Những câu hỏi liên quan
Cho m gam P2O5 vào 300ml dung dịch NaOH 2M thì dung dịch sau phản ứng chỉ chứa 2 muối NaH2PO4 và Na2HPO4 có nồng độ mol bằng nhau. Giá trị của m là?
Cho x (g) P2O5 vào 100g nước thu được dung dịch A. Cho từ từ dung dịch A vào 125g dung dịch NaOH 16% người ta thu được dung dịch B.a. Viết thứ tự các phản ứng có thể xảy rab. x có giá trị trong khoảng giới hạn nào để dung dịch B có 2 muối là Na2HPO4 và NaH2PO4c. Xác định giá trị x để trong dung dịch B nồng độ phần trăm của 2 muối Na2HPO4 và NaH2PO4 bằng nhau.Ngoài lề: trên Hoc24 có ai học chuyên Hóa ko ạ, cho mình hỏi nên luyện đề sao cho hợp lí để thi Hóa.
Đọc tiếp
Cho x (g) P2O5 vào 100g nước thu được dung dịch A. Cho từ từ dung dịch A vào 125g dung dịch NaOH 16% người ta thu được dung dịch B.
a. Viết thứ tự các phản ứng có thể xảy ra
b. x có giá trị trong khoảng giới hạn nào để dung dịch B có 2 muối là Na2HPO4 và NaH2PO4
c. Xác định giá trị x để trong dung dịch B nồng độ phần trăm của 2 muối Na2HPO4 và NaH2PO4 bằng nhau.
Ngoài lề: trên Hoc24 có ai học chuyên Hóa ko ạ, cho mình hỏi nên luyện đề sao cho hợp lí để thi Hóa.
a)
$P_2O_5 + 3H_2O \to 2H_3PO_4$
$3NaOH + H_3PO_4 \to Na_3PO_4 + 3H_2O$
$2NaOH + H_3PO_4 \to Na_2HPO_4 + 2H_2O$
$NaOH + H_3PO_4 \to NaH_2PO_4 + H_2O$
b)
n P2O5 = x/142
=> n H3PO4 = 2n P2O5 = x/71(mol)
n NaOH = 125.16%/40 = 0,5(mol)
Để thu được hai muối Na2HPO4 , NaH2PO4 thì :
1 < n NaOH / n H3PO4 < 2
<=> 1 < 0,5 / (x / 71) < 2
<=> 1 < 35,5/x < 2
<=> x < 35,5 < 2x
<=> 17,75 < x < 35,5
c)
Để nồng độ phần trăm hai muối bằng nhau thì
m Na2HPO4 = m NaH2PO4 = y(gam)
=> n NaOH = 2n Na2HPO4 + n NaH2PO4 = 2y/142 + y/120 = 0,5
=> y = 22,3
Ta có :
n H3PO4 = n Na2HPO4 + n NaH2PO4 = y/142 + y/120 = x/71
=> x = 24,344(gam)
Đúng 1
Bình luận (0)
Rót 300ml dung dịch NaOH 1M vào 200 ml dung dịch H3PO4 1M .Sau phản ứng trong dung dịch tồn tại muối nào, khối lượng đứng bao nhiêu?
A.11g NaH2PO4 và 14,2 g Na2HPO4
B.12g NaH2PO4 và 14,2 g Na2HPO4
C.14,2 g Na2HPO4 và 16,4g Na3PO4
D.14,2g NaH2PO4 và 12 g Na2HPO4
2. Hoà tan hoàn toàn 6,3175 gam hỗn hợp muối gồm NaCl , KCl , MgCl2 vào nước rồi thêm vào đó 100 ml dung dịch AgNO3 1,2M. Sau phản ứng lọc tách được m gam kết tủa X và dung dịch Y. Cho 2 gam Mg vào dung dịch Y đến khi phản ứng kết thúc thu được a gam kết tủa Z và dung dịch T. Cho toàn bộ lượng kết tủa Z tác dụng với dung dịch HCl dư, sau phản ứng thấy khối lượng của Z giảm 1,844 gam. Thêm dung dịch NaOH dư vào dung dịch T, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 0,3 gam chất r...
Đọc tiếp
2. Hoà tan hoàn toàn 6,3175 gam hỗn hợp muối gồm NaCl , KCl , MgCl2 vào nước rồi thêm vào đó 100 ml dung dịch AgNO3 1,2M. Sau phản ứng lọc tách được m gam kết tủa X và dung dịch Y. Cho 2 gam Mg vào dung dịch Y đến khi phản ứng kết thúc thu được a gam kết tủa Z và dung dịch T. Cho toàn bộ lượng kết tủa Z tác dụng với dung dịch HCl dư, sau phản ứng thấy khối lượng của Z giảm 1,844 gam. Thêm dung dịch NaOH dư vào dung dịch T, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 0,3 gam chất rắn E. Tính m, a và thành phần phần trăm theo khối lượng mỗi muối có trong hỗn hợp ban đầu.
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần
m
17
mol oxi, sau phản ứng chỉ thu được P2O5 và
13
,
5
m
17
gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là A. 24,35 B. 11...
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần m 17 mol oxi, sau phản ứng chỉ thu được P2O5 và 13 , 5 m 17 gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là
A. 24,35
B. 11,66
C. 13,6
D. 11,9
Đáp án B.
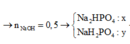
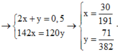
→ n P 2 O 5 = 131 764
→ B T K L m + m 17 . 32 → m = 11 , 66
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần
m
17
mol oxi, sau phản ứng chỉ thu được P2O5 và
13
,
5
m
17
gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là A. 24,35. B. 11,66. C. 13,...
Đọc tiếp
Đốt cháy hoàn toàn m gam hợp chất X của photpho cần m 17 mol oxi, sau phản ứng chỉ thu được P2O5 và 13 , 5 m 17 gam H2O. Cho toàn bộ sản phẩm cháy vào 125 gam dung dịch NaOH 16% thu được dung dịch B chỉ chứa hai muối NaH2PO4 và Na2HPO4 có nồng độ phần trăm bằng nhau. Giá trị của m là
A. 24,35.
B. 11,66.
C. 13,6.
D. 11,9.
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO2. Dẫn toàn bộ khí CO2 thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là A. 31,52. B. 15,76. C. 11,82. D. 27,58.
Đọc tiếp
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO2. Dẫn toàn bộ khí CO2 thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
A. 31,52.
B. 15,76.
C. 11,82.
D. 27,58.
Đáp án C
n C O 3 2 - = 0,2 mol; n H C O 3 - = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n H + = 2x.2 + 3x = 0,42 => x = 0,06 → n C O 2 = 2x + 3x = 0,3 mol.
Có n O H - = 0,36
Xét tỉ lệ T = n O H - n C O 2 thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n C O 3 2 - = 0,06; n H C O 3 - = 0,24
n B a 2 + = 0,08 → n B a C O 3 = 0,06 → m B a C O 3 = 11,82 gam.
Đúng 0
Bình luận (0)
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO. Dẫn toàn bộ khí CO thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là A. 11,82 B. 15,76 C. 27,58 D. 31,52
Đọc tiếp
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO. Dẫn toàn bộ khí CO thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
A. 11,82
B. 15,76
C. 27,58
D. 31,52
Chọn A.
n(CO32-) = 0,2 mol; n(HCO3-) = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32- và HCO32- đã phản ứng
→ n(H+) = 2x.2 + 3x = 0,42 => x = 0,06 → n(CO2) = 2x + 3x = 0,3 mol.
Có n(OH-) = 0,36
Xét tỉ lệ T = n(OH-) / n(CO2) thấy tạo ra đồng thời 2 muối CO32- và HCO3-.
→ n(CO32-) = 0,06; n(HCO3-) = 0,24
n(Ba2+) = 0,08 → n(BaCO3) = 0,06 → m(BaCO3) = 11,82 gam
Đúng 0
Bình luận (0)
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO2. Dẫn toàn bộ khí CO2 thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là A. 31,52. B. 15,76. C. 11,82. D. 27,58.
Đọc tiếp
Nhỏ từ từ đến hết 100 ml dung dịch chứa K2CO3 2M và KHCO3 3M vào 200 ml dung dịch HCl 2,1M, thu được khí CO2. Dẫn toàn bộ khí CO2 thu được vào 100 ml dung dịch chứa NaOH 2M và Ba(OH)2 0,8M, kết thúc các phản ứng thu được m gam kết tủa. Giá trị của m là
A. 31,52.
B. 15,76.
C. 11,82.
D. 27,58.
Đáp án C
n(CO32–) = 0,2 mol; n(HCO3–) = 0,3 mol.
→ tỉ lệ 2 : 3.
→ 2x và 3x là số mol CO32– và HCO32– đã phản ứng
→ n(H+) = 2x.2 + 3x = 0,42 => x = 0,06 → n(CO2) = 2x + 3x = 0,3 mol.
Có n(OH–) = 0,36
Xét tỉ lệ T = n(OH–) / n(CO2) thấy tạo ra đồng thời 2 muối CO32– và HCO3–.
→ n(CO32–) = 0,06; n(HCO3–) = 0,24
n(Ba2+) = 0,08 → n(BaCO3) = 0,06 → m(BaCO3) = 11,82 gam.
Đúng 0
Bình luận (0)