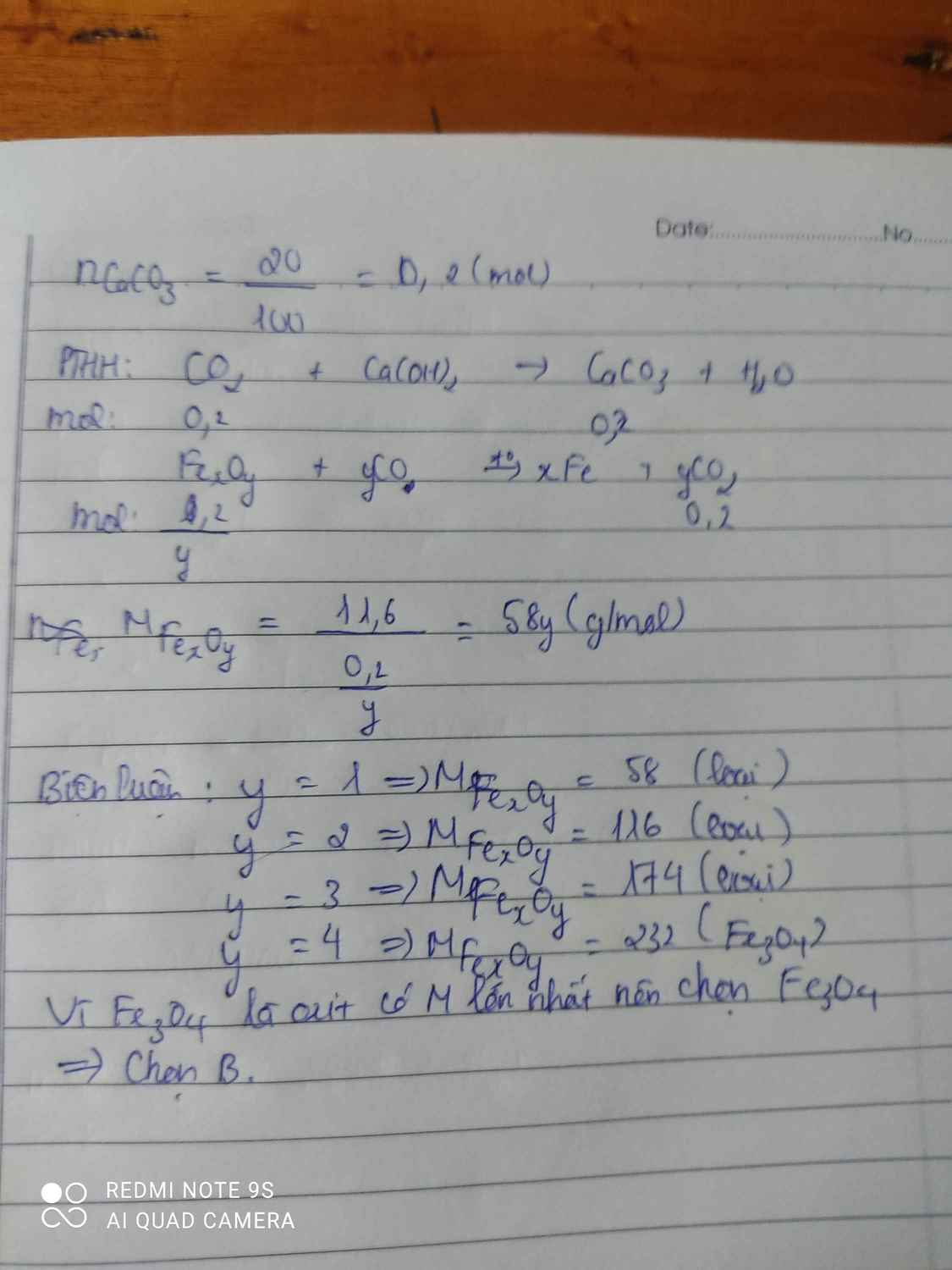10) Nung nóng 11,6g oxit sắt bằng khí CO nóng, dư đến khi thu được hoàn toàn sắt nguyên chất và lượng khí được hấp thụ bởi dd Ca(OH)2 dư thì tách ra 20g kết tủa. Xác định CTHH của oxit sắt

Những câu hỏi liên quan
Khử a(gam) một oxit Sắt bằng CO nóng dư,đến hoàn toàn thu được Fe và khí A.Hòa tan lượng Fe trên trong dung dịch H2 SO4 loãng dư lấy thoát ra 1,68 lít H2(ở đktc).Hấp thụ hoàn toàn bộ khí A bằng dung dịch Ca(OH)2 dư thu được 10 gam kết tủa trắng.Hãy xác định CTHH của oxit sắt và tính a?
hkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhkhk
Thổi luồng khí CO đến dư qua ống sứ chứa 18,56 gam oxit sắt, nung nóng. Sau khi kết thúc phản ứng, khí thoát ra khỏi ống sứ được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được 34,8 gam kết tủa. Công thức oxit sắt là A. Fe3O4 B. FeO. C. Fe2O3. D. Fe2O3 hoặc Fe3O4
Đọc tiếp
Thổi luồng khí CO đến dư qua ống sứ chứa 18,56 gam oxit sắt, nung nóng. Sau khi kết thúc phản ứng, khí thoát ra khỏi ống sứ được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư, thu được 34,8 gam kết tủa. Công thức oxit sắt là
A. Fe3O4
B. FeO.
C. Fe2O3.
D. Fe2O3 hoặc Fe3O4
Chọn C
Quá trình CO phản ứng với oxit chỉ là CO lấy đi O tạo CO2 nên số mol O bị lấy cũng chính bằng số mol CO2. Vì Ca(OH)2 dư ⟹ nCO2 = 34,8/100 = 0,348 = nO bị lấy
⟹ nFe trong oxit = (18,56 – 0,348×16)/56=0,232
⟹ n F e n O = 0 , 232 0 , 348 = 2 3 ⟹ Fe2O3
Đúng 0
Bình luận (0)
yCO+FexOy--t°--> yCO2+xFe
CO2+Ca(OH)2--->CaCO3+H2O nCaCO3=34,8/100=0,348(mol
Theopt2: nCO2=nCaCO3=0,348(mol)
Theo pt1:
nFexOy=1/y.nCO2=0,348/y (mol)
MFexOy=18,56/0,348/y=160y/3(g/mol)
=>56x+16y=160y/3
168x+48y=160y
168x=112y
=>x/y=112/168=2/3
Vậy công thức hoá học của Oxt sắt là Fe2O3
Đúng 0
Bình luận (0)
dùng CO dư thổi qua 8g bột oxit sắt nóng thu được Fe. khí thoát ra hấp thu bằng dung dịch Ca(OH)2 dư thu được 15g kết tủa . Xác định CTHH oxit sắt
\(xCO+Fe_2O_x\rightarrow2Fe+xCO_2\)
0,6mol \(\frac{0,3}{2x}\) \(\frac{0,3}{2}\) 0,15mol
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,15mol 0,15mol 0,15mol 0,15mol
\(n_{CaCO_3}=\frac{m}{M}=\frac{15}{100}=0,15mol\)
\(M_{Fe_2O_x}=\frac{m}{n}=\frac{8}{\frac{0,3}{2x}}=\frac{16x}{0,3}\)
Ta có phương trình:\(M_{Fe_2O_x}=56.2+16x=\frac{16x}{0,3}\)
Giải phương trình ta đc x=3
vậy công thức của Oxit sắt là: Fe2O3
Đúng 0
Bình luận (0)
Khử hoàn toàn 11,6g oxit sắt bằng CO ở nhiệt độ cao. Sản phẩm khí dẫn vào dung dịch Ca(OH)2 dư, tạo ra 20g kết tủa. Công thức của oxit sắt là:
a FeO
b Fe3O4
c Fe2O3
d Không xác định được
Cách khác:
\(Đặt.CTTQ: Fe_xO_y\left(x,y:nguyên,dương\right)\\ y=n_{CO}=n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\\ x=n_{Fe}=\dfrac{11,6-0,2.16}{2}=0,15\left(mol\right)\\ \Rightarrow x:y=0,15:0,2=3 :4\\ \Rightarrow x=3;y=4\\ \Rightarrow CTHH:Fe_3O_4\\ \Rightarrow B\)
Đúng 4
Bình luận (0)
vì Ca(OH)2 dư
=>CO2 dư ->n CO2= n CaCO3=0,2 mol
Bảo toàn O
=>n O (Oxit sắt ) = n CO2= 0,2 mol
->n Fe=\(\dfrac{11,6-0,2.16}{56}\)=0,15 mol
=>\(\dfrac{n_{Fe}}{n_O}\)=\(\dfrac{0,15}{0,2}=\dfrac{3}{4}\)
=>oxit là Fe3O4
Đúng 5
Bình luận (0)
Khử m gam một oxit sắt bằng CO nóng dư đến khi phản ứng hoàn toàn thu được Fe và khí A.Hòa toan hoàn toàn lượng sắt trên bằng HCl dư thì thoát ra 1,68 lít H2 đktc.Hấp thụ toàn bộ khí a vào Ca(OH)2 dư thì được 10g kết tủa.Tìm công thức của oxit sắt
n(H2)=1,68/22=0,075m0l
n(CaC03)=10/1O0=0,1m0l
gọi công thức oxit sát là FexOy
Ptpu:
Fex0y + yCO ===> xFe + yC02 (1)
Fe + 2HCL ===> FeCl2 + H2
0,075m0l <-----. . . . . . . . . . ---- 0,075m0l
C02 + Ca(0H)2 ===> CaC03 + H20
0,1m0l <-----. . . . . . . . . . 0,1m0l
Theo tỉ lệ số mol theo phương trình (1) ta co:
x/y=n(Fe)/n(C02)=0,075/0,1=3/4
Vay oxit sat can tim la oxit sat tu Fe304
Than yC02
0,15/x(m0l) <=== 0,15
Theobài thì khối lượng oxit sắt oh 2 p/u = nhau nên số mol = nhau hay (0,225/y)=(0,15/x)
<=>0,225x=0,15y
<=>x=2y/3
<=>x/y=2/3
Vậy oxit có công thức là Fe203
Đúng 1
Bình luận (3)
\(n_{H_2}=\dfrac{1,68}{22,4}=0,075mol\)
\(n_{CaCO_3}=\dfrac{10}{100}=0,1mol\)
- Gọi Công thức oxit là FexOy
FexOy+yCO\(\rightarrow\)xFe+yCO2(1)
Fe+2HCl\(\rightarrow\)FeCl2+H2(2)
- Theo PTHH (2) ta có: \(n_{Fe}=n_{H_2}=0,075mol\)
CO2+Ca(OH)2\(\rightarrow\)CaCO3+H2O(3)
-Theo PTHH (3): \(n_{CO_2}=n_{CaCO_3}=0,1mol\)
- Theo PTHH (1) ta có: \(\dfrac{0,075}{x}=\dfrac{0,1}{y}\rightarrow\dfrac{x}{y}=\dfrac{0,075}{0,1}=\dfrac{3}{4}\)
- Vậy oxit sắt là Fe3O4
Đúng 2
Bình luận (0)
Bạn ơi,là chia 22,4 nhé
Khử hoàn toàn 5,76 gam một oxit sắt bằng dòng khí CO dư thu được 4,48 lít Hỗn hợp khí A (đktc) .Hấp thụ khí A vào dung dịch chứa 6,96 gam Ca(OH)2 đến khi phản ứng kết thúc thì thu được m gam kết tủa trắng .lọc lấy kết tủa nung đến khối lượng không đổi thì thấy chất rắn giảm 3,52 gam.Xác định công thức của Oxit sắt và tính tỉ khối của A so với H2.
Lười gõ quá nên mình không làm chi tiết, không hiểu cái nào thì hỏi:v
Đặt CTHH của oxit sắt là \(Fe_xO_y\)
\(m_{giảm}=3,52\Rightarrow m_{CO_2}=3,52\left(g\right)\Rightarrow n_{CO_2}=\dfrac{3,52}{44}=0,08\left(mol\right)\)
\(\Rightarrow\dfrac{0,08}{y}=n_{Fe_xO_y}=\dfrac{5,76}{56x+16y}\)
\(\Rightarrow x:y=1:1\)
\(\Rightarrow CT:FeO\)
\(n_A=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow n_{CO}=0,2-0,08=0,12\left(mol\right)\)
\(\Rightarrow m_{CO}+m_{CO_2}=44.0,08+0,12.28=6,88\)
\(\Rightarrow d_{A/H_2}=\dfrac{6,88}{2}=3,44\)
Đúng 2
Bình luận (2)
Thổi 8,96 lít CO (đktc) qua 16 gam một oxit sắt nung nóng. Dẫn toàn bộ khí sau phản ứng qua dung dịch Ca(OH)2 dư, thấy tạo ra 30 gam kết tủa trắng CaCO3, các phản ứng xảy ra hoàn toàn.
1) Tính khối lượng Fe thu được.
2) Xác định công thức oxit sắt.
a) nCaCO3 = 0.3 (mol)
CO + O => CO2
=> nO = 0.3 (mol)
mFe = moxit - mO = 16 - 0.3*16 = 11.2 (g)
nFe = 11.2/56 = 0.2 (mol)
nFe : nO = 0.2 : 0.3 = 2 : 3
CT oxit : Fe2O3
Đúng 1
Bình luận (1)
nCO= 0,4(mol)
yCO + FexOy \(\rightarrow\) xFe + yCO2 (phản ứng có nhiệt độ) (1)
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O (2)
nCaCO3= nCO2(2) = nCO2(1) = 0,3(mol)
nCO2 = nCO = 0,3(mol) => CO dư (0,4-0,3=0,1(mol))
1, Áp dụng định luật bảo toàn khối lượng, ta có:
mCO + mFexOy = mFe + mCO2
=> mfe = mCO + mfexOy - mCO2
\(\Leftrightarrow\) mfe = 0,3.28+ 16 - 0.3.44 = 11,2 (g)
2, Áp dụng định luật bảo toàn nguyên tố Fe, ta có
nFe(sau phản ứng) = nfe(fexOy) = \(\dfrac{11,2}{56}\)= 0,2(mol)
=> mFe(FexOy) = 11,2(g) => mO(fexOy) = 16-11,2= 4,8(g)
=> ta có: \(\dfrac{56x}{16y}\) = \(\dfrac{11,2}{4,8}\)\(\Rightarrow\)\(\dfrac{x}{y}\)=\(\dfrac{2}{3}\)
Vậy công thức oxit sắt là Fe2O3
Thấy ok là phải tích cho tui đó nhá=.=
Đúng 1
Bình luận (1)
Nung nóng 18,56 gam hỗn hợp A gồm FeCO3 và một oixt sắt FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn, thu được khí CO2 và 16 gam một oxit sắt duy nhất. Cho khí CO2 hấp thụ hết vào dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Vậy công thức oxit FexOy là: A. FeO B. Fe3O4 C. Fe2O3 D. Fe2O3 hoặc FeO
Đọc tiếp
Nung nóng 18,56 gam hỗn hợp A gồm FeCO3 và một oixt sắt FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn, thu được khí CO2 và 16 gam một oxit sắt duy nhất. Cho khí CO2 hấp thụ hết vào dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Vậy công thức oxit FexOy là:
A. FeO
B. Fe3O4
C. Fe2O3
D. Fe2O3 hoặc FeO
Các oxit sắt, nung ngoài không khí đến khối lượng không đổi luôn tạo thành Fe2O3 16 gam oxit sắt duy nhất là Fe2O3.
Cách 1: Phương pháp đại số
Đặt số mol các chất trong 18,56 gam A F e C O 3 : n ; F e x O y : m
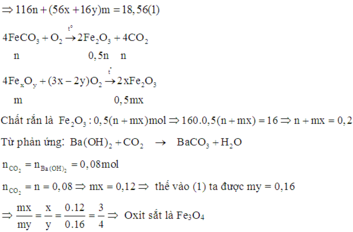
Cách 2: Phương pháp bảo toàn
Đặt số mol các chất trong 18,56 gam A F e C O 3 : n ; F e x O y : m
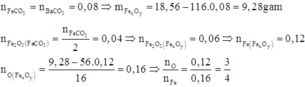
Cách 3: Bảo toàn nguyên tử C và O:
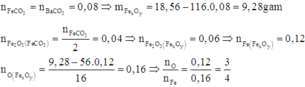
⇒ Oxit của sắt là Fe3O4
Cách 4: Bảo toàn nguyên tử và khối lượng:
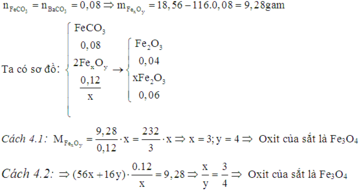
Đáp án B.
Đúng 0
Bình luận (0)
Nung nóng một thời gian hỗn hợp A gồm Al và một oxit sắt (Giả sử chỉ xảy ra phản ứng khử oxit thành kim loại) được m gam hỗn hợp B. Chia hỗn hợp B thành hai phần bằng nhau. Cho phần thứ nhất tác dụng hoàn toàn với dd KOH dư thu được 10,08 lít khí đktc và có 29,52 gam chất rắn không tan. Hòa tan hoàn toàn phần thứ 2 bằng dd H2SO4 đặc nóng, dư được 19,152 lít khí SO2 (sản phẩm khử duy nhất, đktc) và dung dịch C. Cho dd C tác dụng hoàn toàn với dd NH3 dư, lấy toàn bộ lượng kết tủa tạo thành đem nun...
Đọc tiếp
Nung nóng một thời gian hỗn hợp A gồm Al và một oxit sắt (Giả sử chỉ xảy ra phản ứng khử oxit thành kim loại) được m gam hỗn hợp B. Chia hỗn hợp B thành hai phần bằng nhau. Cho phần thứ nhất tác dụng hoàn toàn với dd KOH dư thu được 10,08 lít khí đktc và có 29,52 gam chất rắn không tan. Hòa tan hoàn toàn phần thứ 2 bằng dd H2SO4 đặc nóng, dư được 19,152 lít khí SO2 (sản phẩm khử duy nhất, đktc) và dung dịch C. Cho dd C tác dụng hoàn toàn với dd NH3 dư, lấy toàn bộ lượng kết tủa tạo thành đem nung đến khối lượng không đổi thu được 65,07 gam chất rắn. Xác định công thức của oxit sắt và tính giá trị của m.


Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3
Đúng 0
Bình luận (0)