Cho 104 g dung dịch BaCl2 10% vào 200g dung dịch H2SO4 Lọc bỏ kết tủa trung hòa dung dịch thu được phải dùng 250ml dung dịch NaOH 25% (D=1,28g/ml)
Tính khối lượng kết tủa
Tính C% H2SO4 đã dùng
Gấp lắm ạ......................please help meeee
Cho 104 g dd BaCl2 10% vào 200g g dd H2SO4 Lọc bỏ kết tủa trung hòa dung dịch thu được phải dùng 250ml dung dịch NaOH 25% (D=1,28g/ml)
Tính khối lượng kết tủa
Tính C% dung dịch H2SO4 đã dùng
Gấp
nBaCl2 = 0.05 mol
nNaOH = 2 mol
BaCl2 + H2SO4 --> BaSO4 + 2HCl
0.05_____0.05______0.05_______0.1
mBaSO4 = 0.05*233 = 11.65 g
NaOH + HCl --> NaCl + H2O
0.1_______0.1
2NaOH + H2SO4 --> Na2SO4 + H2O
2-0.1______0.95
mH2SO4 = 98 g
C%H2SO4 = 98/200*100% = 49%
nBaCl2 = 0.5 mol
nNaOH = 2 mol
BaCl2 + H2SO4 --> BaSO4 + 2HCl
0.5______0.5______0.5_______1
mBaSO4 = 0.5*233 = 116.5 g
NaOH + HCl --> NaCl + H2O
1_______1
2NaOH + H2SO4 --> Na2SO4 + H2O
1_________0.5
mH2SO4 = 98 g
C%H2SO4 = 98/200*100% = 49%
Cho 855g dung dịch Ba(OH)2 10% vào 200g dung dịch H2SO4. Lọc bỏ kết tủa được dung dịch X. Để trung hòa dd X phải dùng 125ml dung dịch NaOH 25% (D= 1,28g/ml).
a. Tính khối lượng kết tủa.
b. Tính nồng độ % H2SO4 trong dung dịch X
Cho 104 gam BaCl2 vào 200 gam dung dịch H2 SO4 Lọc bỏ kết tủa trung hòa dung dịch nước lọc cần dùng 250ml dung dịch NaOH 25% (D=1.28g/ml) tính nồng độ phần trăm của H2 SO4
Cho 200g dung dịch Ba(OH)2 10o/o vào 200g dung dịch H2SO4. lọc bỏ kết tủa, trung hòa nước lọc cần dùng 250ml NaOH 25 o/o d = 1,28. Tính nồng độ o/o của dung dịch H2SO4 ban đầu và nồng độ o/o của dung dịch sau phản ứng?
Em ko có tiền nên mong a , cj tham khảo(đây là 500 g dung dịch nên mong a, cj sửa 1 chút ạ)
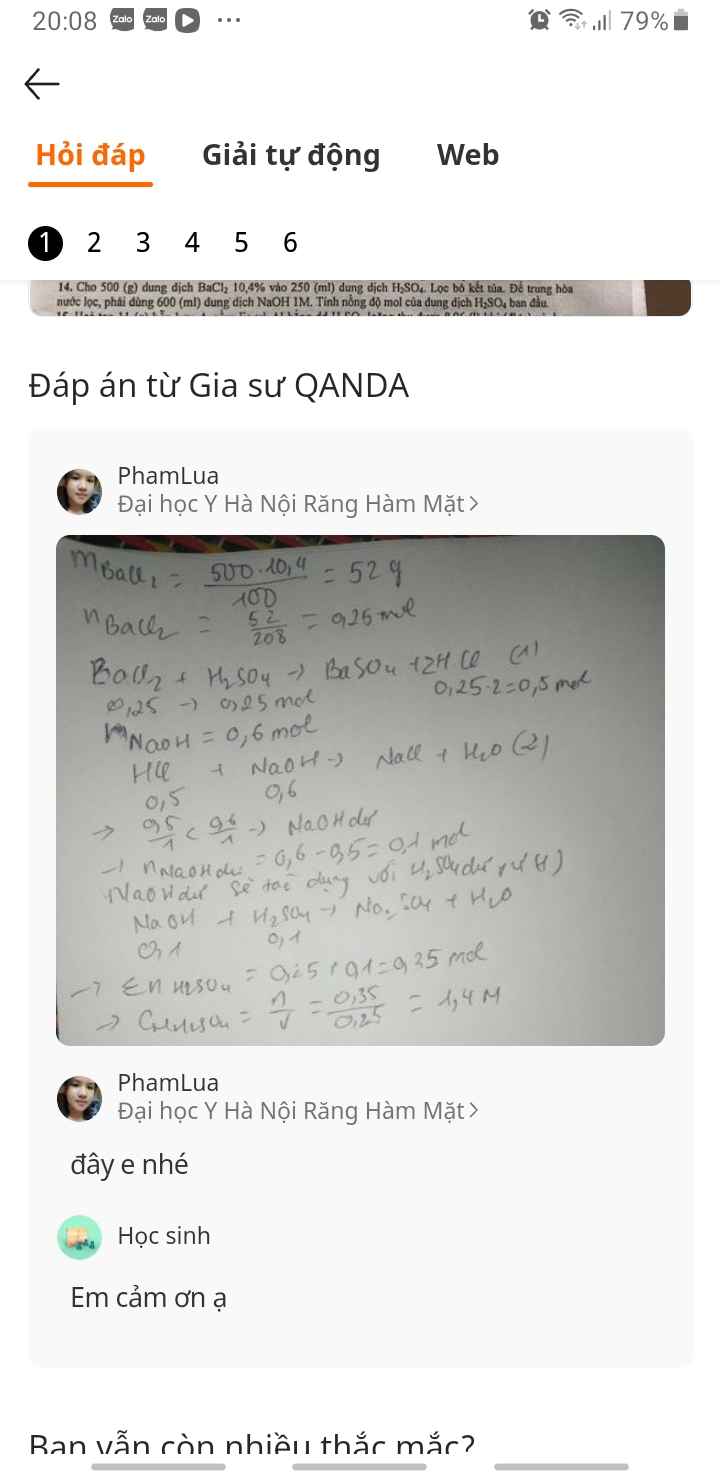
Cho 855g dung dịch BaCl2 vào 200g dung dịch H2SO4. Lọc bỏ kết tủa. Để trung hòa nước lọc dùng hết 125ml dung dịch NaOH 25% D=1,28g/ml. Tính nồng độ phần trăm của H2SO4 trong dung dịch ban đầu.
1. Cho 100 ml dung dịch H2SO4 1M vào dung dịch 200ml BaCl2 dư.
a. Tính khối lượng kết tủa thu được
b. Tính nồng độ dung dịch dịch BaCl2 đã dùng.
nH2SO4=1*0,1=0,1(mol)
PTHH:
BaCl2 + H2SO4 => BaSO4 + 2HCL
1 1 1 1 (mol)
0,1 0,1 0,1 0,1 (mol)
=> kết tủa thu đc là BaSO4
a, Theo PTHH:
nBaSO4=0,1 (mol) => mBaSO4=0,1*233=23,3 (g)
b, Theo PTHH: nBaCl2= 0,1 (mol)
=> CM= 0,1/0,2 = 0,5M
1.
a, \(n_{H_2SO_4}=0,1.1=0,1\left(mol\right)\)
PTHH: H2SO4 + BaCl2 → BaSO4 + 2HCl
Mol: 0,1 0,1 0,1
\(m_{BaSO_4}=233.0,1=23,3\left(g\right)\)
b, \(C_{M_{ddBaCl_2}}=\dfrac{0,1}{0,2}=0,5M\)
Cho 200g dung dịch Ba(NO3)2 13,05o/o vào 200g dung dịch H2SO4a%. lọc bỏ kết tủa, trung hòa nước lọc cần dùng 400ml NaOH 20 o/o d = 1,28. Tính nồng độ o/o của dung dịch H2SO4 ban đầu và nồng độ o/o của dung dịch sau phản ứng trung hòa?
Cho 208 gam dung dịch BaCl2 10% phản ứng hết với dung dịch H2SO4 8% thu được một kết tủa và một dung dịch. a) Phương trình hóa học. b) Tính khối lượng dung dịch H2SO4 cần dùng? c) Tính khối lượng kết tủa thu được sau phản ứng? d) Tính nồng độ % của dung dịch sau phản ứng? Ba = 137, H = 1, S = 32, O = 16, Cl = 35,5
\(n_{BaCl_2}=\dfrac{208.10\%}{208}=0,1\left(mol\right)\\ a,BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\\ 0,1............0,1..............0,1.............0,2\left(mol\right)\\ b,m_{ddH_2SO_4}=\dfrac{0,1.98.100}{8}=122,5\left(g\right)\\ c,m_{kt}=m_{BaSO_4}=0,1.233=23,3\left(g\right)\\ d,m_{ddsau}=208+122,5-23,3=307,2\left(g\right)\\ C\%_{ddHCl}=\dfrac{0,2.36,5}{307,2}.100\approx2,376\%\)
Cho một dung dịch có chứa 52g BaCl2 tác dụng hoàn toàn với dung dịch H2SO4 19,6%. a) Viết phương trình hóa học . b) Tính khối lượng dung dịch H2SO4 cần dùng c) Tính khối lượng chất kết tủa tạo thành d) Lọc toàn bộ kết tủa, phần dung dịch còn lại được cho vào dung dịch có chứa 8g NaOH. Hãy cho biết dung dịch sau phản ứng sẽ làm giấy quỳ tím thay đổi như thế nào? (Cho: Ba = 137; Cl = 35,5; H = 1; S = 32; O = 16; Na = 23)
a) \(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
b) \(n_{BaCl_2}=\dfrac{52}{208}=0,25\left(mol\right)\)
PTHH: \(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
0,25----->0,25------->0,25---->0,5
=> \(m_{H_2SO_4}=0,25.98=24,5\left(g\right)\)
=> \(m_{ddH_2SO_4}=\dfrac{24,5.100}{19,6}=125\left(g\right)\)
c) \(m_{BaSO_4}=0,25.233=58,25\left(g\right)\)
d)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Xét tỉ lệ \(\dfrac{0,5}{1}>\dfrac{0,2}{1}\) => NaOH hết, HCl dư
=> Quỳ tím chuyển màu đỏ